Asid karboksilat
- 4542
- 257
- Erick Krajcik
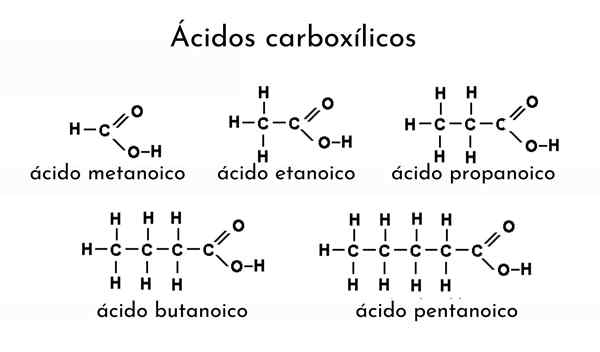
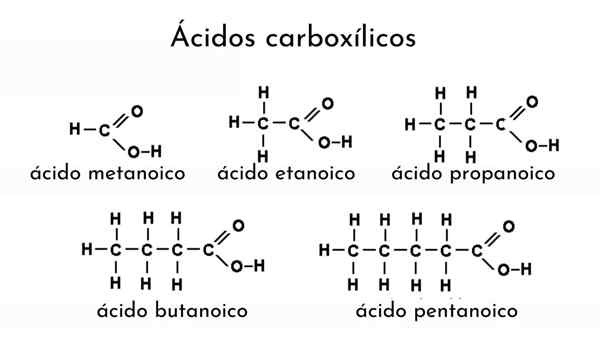 Contoh asid karboksilik
Contoh asid karboksilik Apakah asid karboksilik?
Dia Asid karboksilat Ia adalah istilah yang dikaitkan dengan mana -mana sebatian organik yang mengandungi kumpulan karboksil. Mereka juga boleh dipanggil asid organik, dan hadir dalam banyak sumber semula jadi. Contohnya, dari semut dan serangga lain seperti kumbang galeri, asid formik, asid karboksilik disuling.
Iaitu, anthill adalah sumber yang kaya dengan asid formik. Juga, asid asetik diekstrak dari cuka, bau mentega tengik adalah disebabkan oleh asid butyric, herba valeria mengandungi asid otak dan dari topi yang diperoleh asid capric, semua asid karboksilat ini.
Asid laktik memberikan rasa tidak enak susu masam, dan dalam beberapa lemak dan minyak asid lemak hadir. Contoh sumber semulajadi asid karboksilik tidak terhitung jumlahnya, tetapi semua nama yang ditetapkannya berasal dari kata -kata dalam bahasa Latin. Oleh itu, dalam bahasa Latin perkataan Formica bermaksud "semut".
Oleh kerana asid ini diekstrak dalam bab sejarah yang berbeza, nama -nama ini adalah perkara biasa, menyatukan budaya popular.
Formula
The Formula umum asid karboksilik ialah -r -cooh, atau lebih terperinci: R- (c = o) -oh. Atom karbon dikaitkan dengan dua atom oksigen, yang menyebabkan penurunan ketumpatan elektroniknya dan, akibatnya, beban separa positif.
Beban ini mencerminkan status pengoksidaan karbon dalam sebatian organik. Di mana -mana, karbon adalah seperti berkarat seperti dalam kes asid karboksilik, pengoksidaan ini berkadar dengan tahap kereaktifan.
Atas sebab ini kumpulan -cooh mempunyai dominasi terhadap kumpulan organik yang lain, dan mentakrifkan sifat berkarbonat utama dan rantaian berkarbonat utama kompaun.
Oleh itu, tidak ada derivatif asid amina (R-NH2), tetapi aminos berasal dari asid karboksilik (asid amino).
Nomenclature
Nama biasa yang berasal dari bahasa Latin untuk asid karboksilik tidak menjelaskan struktur kompaun, atau susunan atau pelupusan kumpulan atom mereka.
Memandangkan keperluan untuk penjelasan ini, tatanama sistematik IUPAC timbul untuk menamakan asid karboksilat.
Boleh melayani anda: bromin: sejarah, struktur, konfigurasi elektronik, sifat, kegunaanTatanama ini ditadbir oleh beberapa peraturan, dan beberapa daripadanya adalah:
Kaedah 1
Untuk menyebutkan asid karboksilik, nama alkana mesti diubah suai dengan menambahkan akhiran "ICO". Oleh itu, untuk etana (pilih3-Ch3) asid karboksilik yang sepadan adalah asid etanoik (CH3-COOH, asid asetik, sama cuka).
Contoh lain: untuk Cho3Ch2Ch2-Cooh El Alcano menjadi butana (CH3Ch2Ch2Ch3) dan, oleh itu, asid butanoik (asid butyric, sama mentega tengik) dilantik.
Kaedah 2
Kumpulan -cooh mentakrifkan rantaian utama, dan angka yang sepadan dengan setiap karbon dikira dari karbonil.
Contohnya, CHO3Ch2Ch2Ch2-COOH adalah asid pentanoik, mengira dari satu hingga lima karbon ke metil (pilih3). Sekiranya kumpulan metil lain dikaitkan dengan karbon ketiga, ia akan menjadi CHO3Ch2CH (Ch3) Ch2-COOH, sebagai tatanama yang dihasilkan sekarang: 3-methylpentanoic Acid.
Kaedah 3
Substituen didahului oleh bilangan karbon yang dihubungkan. Begitu juga, substituen ini boleh dua atau tiga pautan, dan tambahkan akhiran "ICO" sama dengan alkena dan alkin. Contohnya, CHO3Ch2Ch2CH = Chch2-COOH disebut sebagai asid (cis atau trans) 3- heptenoik.
Kaedah 4
Apabila rantaian R terdiri daripada cincin (φ). Asid disebut bermula dengan nama cincin dan berakhir dengan akhiran "carboxylic". Sebagai contoh, φ-COOH dinamakan sebagai asid benzecenocarboxylic.
Struktur asid karboksilat
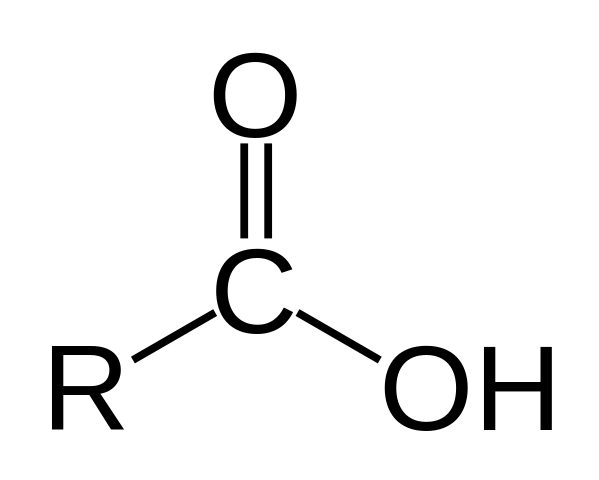 Struktur asid karboksilik. R adalah rantai hidrogen atau berkarbonat.
Struktur asid karboksilik. R adalah rantai hidrogen atau berkarbonat. Di bahagian atas, struktur umum asid karboksilik diwakili. Rantaian sampingan boleh panjang atau mempunyai semua jenis substituen.
Atom karbon mempunyai hibridisasi SP2, yang membolehkan anda menerima ikatan berganda dan menjana sudut pautan kira -kira 120º.
Oleh itu, kumpulan ini dapat diasimilasikan sebagai segitiga rata. Oksigen atas kaya dengan elektron, manakala hidrogen yang lebih rendah adalah miskin dalam elektron, menjadi hidrogen asid (penerima elektron). Ini dapat dilihat dalam struktur resonans ikatan berganda.
Hidrogen ditugaskan ke arah pangkalan, dan atas sebab ini struktur ini sepadan dengan sebatian asid.
Boleh melayani anda: AminaSifat asid karboksilat
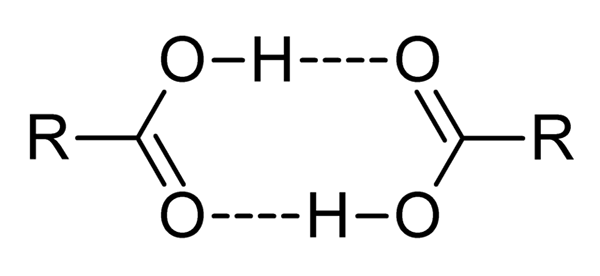
Asid karboksilik adalah sebatian kutub, bau yang sengit dan dengan kemudahan berinteraksi dengan berkesan antara satu sama lain oleh jambatan hidrogen, seperti yang digambarkan oleh imej unggul.
Apabila dua asid karboksilik berinteraksi dengan cara ini, dímeros terbentuk, beberapa stabil cukup untuk wujud dalam fasa gas.
Jambatan hidrogen dan diameter menyebabkan asid karboksilik mempunyai titik mendidih yang lebih tinggi daripada air. Ini kerana tenaga yang disediakan dalam haba mesti menguap bukan sahaja molekul, tetapi kepada dimer, juga dikaitkan dengan jambatan hidrogen ini.
Asid karboksilik kecil merasakan pertalian yang besar untuk pelarut air dan kutub. Walau bagaimanapun, apabila bilangan atom karbon lebih besar daripada empat, watak hidrofobik rantai R mendominasi dan menjadi tidak enak dengan air.
Dalam fasa pepejal atau cair, panjang rantai r dan substituen yang dimiliki memainkan peranan penting. Oleh itu, apabila rantai sangat panjang, mereka berinteraksi antara satu sama lain melalui daya penyebaran London, seperti dalam hal asid lemak.
Keasidan
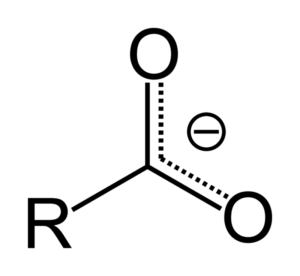
Apabila asid karboksilik menyumbangkan proton, ia menjadi anion karboksilat, yang diwakili dalam imej atas. Dalam anion ini beban negatif dipindahkan antara kedua -dua atom karbon, menstabilkannya dan, oleh itu, memihak kepada reaksi yang berlaku.
Bagaimana bervariasi keasidan ini dari satu asid karboksilik ke yang lain? Semuanya bergantung pada keasidan proton dalam kumpulan OH: yang lebih miskin dalam elektron, lebih banyak asid.
Keasidan ini dapat ditingkatkan jika salah satu substituen rantai RA adalah spesies elektronegatif (yang menarik atau mengeluarkan ketumpatan elektronik dari persekitarannya).
Contohnya, jika di Cho3-COOH diganti H dari kumpulan metil dengan atom fluorin (CFH2-COOH) keasidan meningkat dengan ketara kerana F menarik balik ketumpatan elektronik dari karbonil, oksigen, dan kemudian hidrogen. Sekiranya semua H digantikan oleh F (CF3-COOH) Keasidan mencapai nilai maksimumnya.
Boleh melayani anda: hidrogen: sejarah, struktur, sifat dan kegunaanPembolehubah apa yang menentukan tahap keasidan? Pkke. Semakin rendah pkke Dan lebih dekat dengan 1, lebih besar adalah keupayaan asid untuk memisahkan air dan, seterusnya, lebih berbahaya dan berbahaya. Dari contoh sebelumnya, CF3-COOH mempunyai nilai PK terendahke.
Penggunaan/aplikasi asid karboksilik
Oleh kerana pelbagai asid karboksilik, masing -masing mempunyai aplikasi yang berpotensi dalam industri, sama ada polimer, farmaseutikal atau makanan.
Industri Makanan
- Aditif.
- Pengawet (asid sorbik dan asid benzoik).
- Pengawal selia alkaliniti banyak produk.
- Pengeluaran minuman ringan.
- Ejen antimikrob sebelum tindakan antioksidan. Dalam kes ini, trend adalah antimikrobial cecair.
- Bahan utama cuka biasa (asid asetik).
- Asidulant dalam minuman berkarbonat dan makanan (asid sitrik dan asid laktik).
- Pembantu dalam kematangan keju Swiss (asid propionik).
- Keju, Chucrut, Colm Fermentasi dan Minuman Lembut (Asid Laktik).
Industri farmaseutikal
- Antipyretik dan analgesik (asid acetylsalicylic).
- Aktif dalam proses sintesis aroma, dalam beberapa ubat (asid butyric atau butanoik).
- Antimikotik (asid benzoik digabungkan dengan asid salisilik).
- Aktif untuk pembuatan ubat vitamin C (asid askorbik).
- Fungisida (asid caprilic).
- Pembuatan beberapa julap (asid hydroxybothanodium).
Industri lain
- Pembuatan plastik dan pelincir (asid sorbik).
- Pembuatan varnis, resin elastik dan pelekat telus (asid akrilik).
- Pembuatan lukisan dan varnis (asid linoleik).
- Pembuatan sabun, detergen, syampu, kosmetik dan produk pembersihan logam (asid oleik).
- Pembuatan Pasta Pergigian (asid salisilik).
- Pengeluaran Acetate Rayon, Filem Fotografi dan Pelarut untuk Cat (Asid Acetic).
- Pengeluaran pewarna dan kecokelatan (asid metana).
- Penyediaan minyak pelincir, bahan kalis air dan lukisan secant (asid palmitik).
- Pembuatan getah (asid asetik).
- Penghuraian dan Galvanplasty.
- Pelarut.
- Pengeluaran minyak wangi (asid benzoik).
- Pembuatan Plastik dan Resin (Asid Photal).
- Penghuraian poliester (asid tereftallic).
- Penyediaan lilin parafin (asid stearic).
Rujukan
- Graham Solomons t.W., Craig b. Fryhle. Kimia organik. Asid karboksilik dan derivatif mereka (edisi ke -10., halaman 779-783). Wiley Plus.
- Asid Organik. Naturalwellbeing pulih.com
- Francis a. Tortoiseshell. Kimia organik. Asid karboksilik. (Edisi Keenam., Halaman 805-820). MC Graw Hill.
- William Reusch. Asid karboksilik. Pulih dari kimia.MSU.Edu

