Strontium Chloride (SRCL2)
- 2582
- 100
- Anthony Breitenberg
Apa itu strontium klorida?
Dia Strontium Chloride Ia adalah sebatian bukan organik yang dibentuk oleh strontium, alkalinoterreo logam (SR. Becamgbara) dan halogen klorin. Kerana kedua -dua elemen mempunyai elektronegativiti yang sangat berbeza, sebatiannya adalah pepejal ionik yang formula kimianya adalah srcl2.
Seperti pepejal ionik, ia terdiri daripada ion. Dalam kes SRCL2, Mereka adalah kation sr2+ Untuk setiap dua anion cl-. Sifat dan aplikasinya serupa dengan kalsium dan barium klorida.
Seperti kalsium klorida (CACL2), adalah hygroscopic dan kristalnya menyerap air untuk membentuk garam hexahydrate, di mana enam molekul air terdapat dalam kekisi kristal (SRCL2· 6h2Sama ada). Malah, ketersediaan hidrat lebih besar daripada SRCL2 anhydrous (tanpa air).
Salah satu aplikasi utamanya adalah sebagai pendahulu kepada sebatian strontium lain; iaitu, ia merupakan sumber strontium dalam sintesis kimia tertentu.
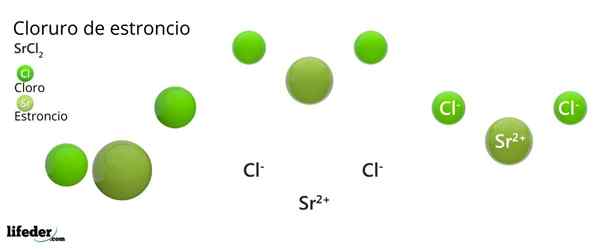
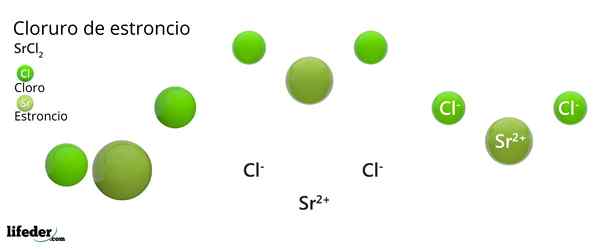
Struktur kimia strontium klorida
 Struktur kristal strontium klorida
Struktur kristal strontium klorida Imej unggul mewakili jenis struktur kristal yang cacat dari SRCL2 anhydrous. Dalam hal ini, sfera hijau kecil sesuai dengan ion SR2+, Walaupun sfera hijau besar mewakili ion -ion-.
Dalam struktur ini setiap ion sr2+ Ia "dipenjarakan" oleh lapan cl ion-, Akibatnya mempunyai nombor koordinasi yang sama dengan 8 dan, mungkin, geometri padu di sekelilingnya. Iaitu, empat sfera hijau membuat bumbung kiub, manakala empat lagi lantai, terletak SR2+ Di tengah -tengahnya.
Apa yang akan menjadi struktur fasa soda? Struktur Lewis untuk garam ini adalah CL-SR-CL, nampaknya linear dan mengandaikan seratus peratus pautannya. Walau bagaimanapun, dalam fasa gas -srcl2(g)- "garis" ini menunjukkan sudut kira-kira 130 °, sebenarnya menjadi sejenis v.
Boleh melayani anda: keadaan gas: ciri -ciri, undang -undang umum, contohAnomali ini tidak dapat dijelaskan dengan jayanya, memandangkan fakta bahawa strontium tidak mempunyai elektron berkongsi yang menduduki jumlah elektronik. Mungkin ia boleh disebabkan oleh penyertaan orbital D dalam pautan, atau ke gangguan elektron teras.
Penggunaan/Aplikasi Strontium Chloride
SRCL2· 6h2Atau ia telah digunakan sebagai bahan tambahan dalam polimer organik; Contohnya, dalam alkohol polyvinyl, untuk mengubah suai sifat mekanikal dan elektriknya.
Ia digunakan sebagai ferit strontium dalam pembuatan magnet seramik dan kaca yang ditakdirkan untuk menjadikan kristal depan televisyen.
Bertindak balas dengan natrium kromat (NA2CRO4) untuk menghasilkan kromat strontium (srcro4), yang digunakan sebagai cat tahan kakisan untuk aluminium.
Apabila mereka dipanaskan dengan api, sebatian strontium bersinar dengan api kemerahan, itulah sebabnya mereka ditakdirkan untuk menghuraikan suar dan bunga api.
Aplikasi ubat
Radioisotop strontium chloride 89 (isotop yang paling banyak adalah 85Encik.
Penggunaan penyelesaian yang dicairkan (3-5 %) selama lebih dari dua minggu dalam rawatan rhinitis alergi (keradangan kronik mukosa hidung), menunjukkan peningkatan penurunan bersin dan menggosok hidung.
Sebaik sahaja ia digunakan dalam formulasi pasta gigi untuk mengurangkan sensitiviti pergigian, membentuk penghalang pada microtubules dentinal.
Kajian kompaun ini menunjukkan keberkesanan terapeutik berbanding prednisolone (metabolit ubat prednisone) dalam rawatan kolitis ulseratif.
Ia boleh melayani anda: pecahan molar: bagaimana ia dikira, contoh, latihanHasilnya didasarkan pada model tikus; Walaupun begitu, ia mewakili harapan bagi pesakit yang juga mengalami osteoporosis, kerana mereka boleh pergi ke ubat yang sama untuk memerangi kedua -dua penyakit tersebut.
Ia digunakan untuk mensintesis strontium sulfat (SRSO4), lebih padat daripada srcl2. Walau bagaimanapun, kelarutan air minimumnya tidak menjadikannya cukup ringan untuk digunakan dalam radiologi, tidak seperti barium sulfat (BASO4).
Penyediaan strontium klorida
Strontium klorida boleh disediakan dengan tindakan langsung asid hidroklorik (HCl) pada logam tulen, sehingga mengalami tindak balas jenis redoks:
MR (s) + HCl (ac) => srcl2(Ac) + h2(g)
Di sini, logam strontium dioksidakan dengan mendermakan dua elektron untuk membolehkan pembentukan hidrogen gas.
Juga, hidroksida dan strontium karbonat (SR (OH)2 dan SRCO3) bertindak balas dengan asid ini dengan mensintesisnya:
Sr (oh)2(s) + 2hcl (ac) => srcl2(Ac) + 2h2Atau (l)
Srco3(s) + 2hcl (ac) => srcl2(ac) + co2(g) + h2Atau (l)
Memohon teknik penghabluran, SRCL diperolehi2· 6h2Sama ada. Setelah dehidrasi oleh tindakan haba sehingga SRCL akhirnya menghasilkan2 anhydrous.
Strontium Chloride Properties
Ciri -ciri fizikal dan kimia kompaun ini bergantung kepada sama ada dalam bentuk terhidrat atau anhydrous. Ini kerana interaksi elektrostatik berubah apabila molekul air ditambah kepada kekisi kristal SRCL2.
Anhydrous
Strontium klorida adalah pepejal kristal putih, dengan berat molekul 158.53 g/mol, dan ketumpatan 3.05 g/ml.
Titik leburnya (874 ºC) dan mendidih (1250 ºC) adalah tinggi, menunjukkan interaksi elektrostatik yang kuat antara ion SR2+ dan Cl-. Ia juga mencerminkan tenaga retikular kristal yang hebat yang strukturnya anhidrat.
Boleh melayani anda: selulosa asetatEntalpi pembentukan SRCL2 pepejal adalah 828.85 kJ/mol. Ini merujuk kepada tenaga haba yang dikeluarkan oleh setiap tahi lalat yang terbentuk dari komponennya dalam keadaan standardnya: Klorin dan Gas Pepejal untuk Strontium.
Hexahydrate
Dalam bentuk hexahydrate ia mempunyai berat molekul yang lebih tinggi daripada bentuk anhydrous (267 g/mol), dan ketumpatan yang lebih rendah (1.96 g/ml). Penurunan ketumpatannya adalah disebabkan oleh fakta bahawa molekul air "melebarkan" kristal, meningkatkan jumlah; Oleh itu, ketumpatan struktur berkurangan.
Hampir dua kali ganda daripada air pada suhu bilik. Kelarutan airnya sangat tinggi, tetapi dalam etanol sedikit larut. Ini disebabkan oleh watak organiknya walaupun polaritinya. Iaitu, hexahydrate adalah sebatian kutub bukan organik. Akhirnya, pada 150 ºC ia menjadi dehidrasi untuk menghasilkan garam anhydrous:
Srcl2· 6h2Atau (s) => srcl2(s) + 6H2O (g)
Rujukan
- Wikipedia. (2018). Strontium Chloride. Diambil dari.Wikipedia.org
- DrugBank. (2018). Strontium Chloride SR-89. Drugbank pulih.Ac
- Pubchem. (2018). Strontium Chloride. Pulih dari pubchem.NCBI.NLM.NIH.Gov
- Bull. Mater. (2010). Pengaruh stontium klorida granular sebagai bahan tambahan pada sifat elektrik dan mekanikal submary untuk alkohol polivinil tulen. Sci., Vol. 33, no. 2, ms. 149-155. Akademi Sains India.
- Ccoil. (4 September 2009). Stontium-chloride -xtal-3D-SF. [Rajah]. Diperoleh pada 13 April 2018, dari: Commons.Wikimedia.org
- Semua tindak balas. SRCL2 - Stontium Chloride. Pulih dari allreactions.com