Kompaun kimia
- 4809
- 470
- Julius Dibbert
Kami menerangkan apa sebatian kimia yang terdiri daripada, jenis yang wujud, perbezaan dengan unsur -unsur kimia dan memberi beberapa contoh.
 Sebatian kimia adalah semua bahan yang mempunyai atom dua elemen kimia yang berbeza
Sebatian kimia adalah semua bahan yang mempunyai atom dua elemen kimia yang berbeza Apa itu sebatian kimia?
A Kompaun kimia Ia adalah bahan yang dibentuk oleh kesatuan dua atau lebih atom unsur kimia yang berbeza. Sebatian kimia tetap bersatu terima kasih kepada ikatan kimia, yang berkaitan dengan elektron atom yang dipautkan; iaitu, dalam sebatian kimia elektron (paling luar) atom campur tangan dalam pembentukan pautan.
Komponen sebatian kimia (elemen kimia) tidak boleh dipisahkan antara satu sama lain dengan kaedah fizikal, seperti: penyulingan, sentrifugasi, penapisan, dll., Memerlukan kaedah kimia untuk mencapainya.
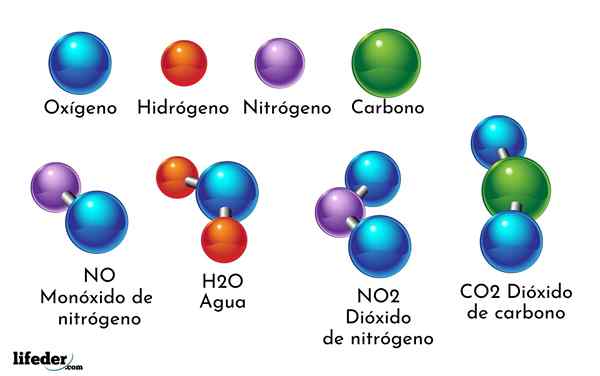
Contoh sebatian kimia adalah air. Ia dibentuk oleh hanya dua atom dua elemen kimia yang berbeza: oksigen dan hidrogen, mempunyai formula kimia h2Sama ada. Oleh itu, dua h mengikat dengan satu atau untuk membentuk h2Sama ada.
Elemen kimia, tidak seperti sebatian kimia, adalah cara paling mudah dan paling asas yang membentuk perkara. Ia dibentangkan sebagai jenis atom yang unik yang tidak dapat dipecahkan kepada bahan yang lebih mudah oleh tindak balas kimia.
Jenis sebatian kimia
Sebatian kimia boleh diklasifikasikan terutamanya mengikuti dua kriteria:
- Menurut jenis bon yang menyatukan unsur -unsur kimia yang terdapat di dalam sebatian kimia.
- Menurut komposisi dan struktur sebatian kimia.
Menurut jenis pautan
Bergantung pada jenis pautan, sebatian kimia boleh:
- Molekul. Mereka adalah sebatian kimia yang dibentuk oleh dua atau lebih jenis elemen kimia yang berbeza, yang disertai oleh ikatan kovalen. Pautan ini dicirikan oleh perkongsian satu atau lebih pasang elektron luaran, atau Valencia, antara dua atom.
- Ion. Sebatian kimia yang dimuatkan secara elektrik dipanggil sebatian kimia ion, dan ion mereka disatukan oleh pautan ionik. Ikatan ini berlaku apabila menyertai elemen kimia jenis logam dengan elemen kimia bukan logam.
- Sebatian intermetallic. Ia adalah sejenis aloi logam yang merupakan bahan pepejal yang antara dua atau lebih unsur kimia logam untuk menyatukannya.
- Penyelarasan. Mereka dibentuk oleh elemen logam pusat, yang dipanggil pusat koordinasi, dan yang mengelilingi satu set molekul bersatu atau ion yang dikenali sebagai ligan. Hemoglobin, sebagai contoh, adalah protein yang terdapat dalam sel darah merah dan mengangkut oksigen dalam darah. Hemoglobin mempunyai sebatian koordinasi yang dipanggil Grupo Hemo. Di tengah -tengah hemo terdapat atom besi yang campur tangan dalam pengangkutan oksigen melalui hemoglobin.
Menurut komposisi dan struktur
Menurut kriteria ini, sebatian kimia diklasifikasikan sebagai organik dan bukan organik.
- Sebatian organik. Mereka adalah sebatian yang elemen kimia utamanya adalah karbon, yang biasanya membentuk pautan dengan atom karbon dan hidrogen yang sama. Walau bagaimanapun, mereka juga hadir, walaupun pada tahap yang lebih rendah, oksigen, nitrogen, sulfur, boron, fosforus, dll. Sebatian organik boleh:
- Alifatik. Molekul sebatian alifatik boleh mempunyai bentuk linear atau kitaran, iaitu, dalam bentuk tertutup seperti segitiga, dataran, pentagon, dll. Mereka boleh mempunyai ikatan karbon tiga jenis: mudah (c-c), double (c = c) atau triple (c≡C).
- Aromatik. Mereka adalah sebatian kitaran yang secara bergantian membentangkan ikatan karbon-karbon mudah dan ikatan karbon karbon berganda.
- Heterocyclic. Mereka adalah sebatian yang mempunyai struktur kitaran, yang boleh membentangkan penggantian atom karbon dengan elemen kimia lain (o, s, n, dll.).
- Organometallic. Mereka adalah sebatian organik yang boleh hadir dalam unsur logam komposisi mereka.
- Polimer. Mereka adalah molekul besar (makromolekul) yang dibentuk oleh unit kecil dan identik yang diulangi di seluruh polimer, dan yang dipanggil monomeri.
- Sebatian bukan organik. Sebatian bukan organik, tidak seperti yang organik, tidak mempunyai karbon sebagai elemen kimia pusat, melainkan campur tangan dalam komposisi mereka kebanyakan unsur kimia yang diketahui. Sebatian bukan organik boleh:
- Oksida asas. Mereka dibentuk oleh reaksi elemen kimia logam, seperti natrium, kalsium, besi, tembaga, dan sebagainya., Dengan oksigen. Sebagai contoh, natrium oksida (Nao) adalah oksida asas. Mereka dipanggil oksida asas kerana mereka akan menimbulkan pangkalan atau hidroksida.
- Oksida asid. Mereka berasal dari reaksi unsur kimia bukan metal, seperti klorin, fluorin, sulfur, bromin, dll., Dengan oksigen. Contohnya, Bromic Oxide (BR2Sama ada5) Ia adalah oksida asid. Mereka dipanggil oksida asid kerana ia menimbulkan asid.
- Hidror. Mereka hadir dalam komposisi kimia mereka kehadiran hidrogen. Terdapat dua jenis: hidro logam dan hidror bukan logam.
- Logam. Mereka dibentuk oleh reaksi hidrogen, dengan keadaan pengoksidaan -1, dengan logam. Sebatian kimia ini adalah satu -satunya di mana hidrogen hadir dengan keadaan pengoksidaan -1. Contohnya, CAH2 Ia adalah kalsium hidrida.
- Tidak logam. Mereka dibentuk oleh reaksi hidrogen, dengan keadaan pengoksidaan + 1, dengan elemen bukan logam dengan keadaan pengoksidaan yang lebih rendah. Klorin hidrida (HCl) adalah gas yang apabila asid hidroklorik dibubarkan di dalam air.
- Asid. Mereka adalah sebatian kimia bukan organik, walaupun terdapat asid organik, yang mempunyai pH kurang dari 7 dan beralih kepada warna kertas merah ke merah ke merah. Mereka boleh dikelaskan kepada hidracycids dan oxacids.
- Hydracy. Mereka berasal dari tindak balas hidrogen dengan bukan metal untuk membentuk hidrida yang larut dalam air berasal dari asid; Contohnya, asid iarhydric (HI).
- Oxcacids. Ia berasal dari reaksi oksida unsur kimia bukan logam dengan air. Sebagai contoh, tindak balas oksida sulfurik (begitu3) Dengan air menghasilkan asid sulfurik (h2SW4).
- Awak keluar. Mereka adalah sebatian kimia yang berasal dari interaksi asid dan sebatian asas. Dalam komposisinya mungkin terdapat banyak elemen logam sebagai bukan logam. Garam diklasifikasikan sebagai:
- Garam neutral. Mereka berasal dari tindak balas peneutralan antara asid dan asas dengan pembentukan garam dan air. Contohnya, tindak balas natrium hidroksida (NaOH) dengan asid hidroklorik (HCl) menghasilkan natrium klorida (NaCl), garam dan air. Mereka dipanggil neutral kerana mereka tidak menghasilkan variasi pH.
- Garam asid. Mereka dibentuk oleh reaksi hidroksida logam dengan Valencia +1, dengan asid dengan beberapa hidrogen. Reaksi litium hidroksida (LIOH) dengan asid karbonik (h2Co3), menghasilkan penggantian hanya satu hidrogen dengan litium, yang menyebabkan bikarbonat litium (lihco3), Garam dan air asid.
- Garam asas. Mereka dihasilkan oleh tindak balas asas yang mempunyai lebih dari satu kumpulan OH dengan asid hidrasi, contohnya, asid hidroklorik. Apabila bertindak balas asid dengan kalsium hidroksida, CA (OH)2, Atom klorin menggantikan kumpulan hidroksil (OH). Ini menghasilkan kalsium hydroxychloride (cuckloh), garam asas dan air.
Perbezaan antara sebatian kimia dan elemen kimia
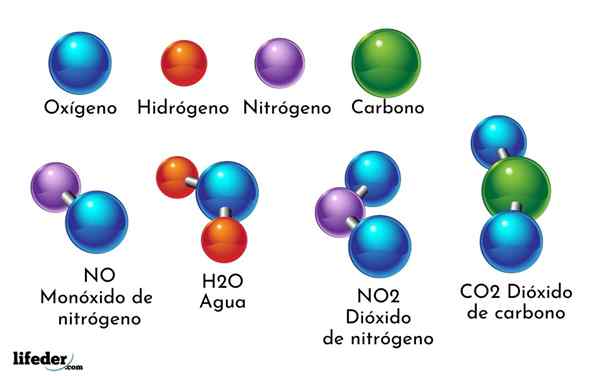 Naik elemen kimia dan sebatian kimia. Sebatian kimia dibentuk oleh unsur -unsur di atas
Naik elemen kimia dan sebatian kimia. Sebatian kimia dibentuk oleh unsur -unsur di atas Setiap elemen kimia sepadan dengan atom tertentu dan hanya dengan jenis atom; iaitu unsur kimia tidak mempunyai pelbagai jenis atom. Atom adalah zarah asas bahan yang tidak dibahagikan dengan kaedah fizikal atau kimia.
Atom elemen kimia boleh disatukan dengan atom unsur -unsur kimia lain untuk membentuk sebatian kimia, yang boleh dipisahkan ke dalam komponen mereka (elemen kimia) menggunakan kaedah kimia.
Unsur -unsur kimia dan sebatian kimia dengan teka -teki boleh dilengkapi: kepingan teka -teki mempunyai ciri -ciri yang berbeza, sehingga mereka dapat memadankan unsur -unsur kimia.
Potongan teka -teki dapat bergabung untuk membentuk angka yang berbeza. Angka yang terbentuk dapat disamakan dengan sebatian kimia. Setelah aktiviti selesai, angka teka -teki dapat dipisahkan ke dalam kepingan yang membentuknya.
Contoh sebatian kimia
Di bawah ini anda dapat melihat beberapa contoh sebatian kimia harian:
- HCL: Asid hidroklorik
- H2S: Asid sulfhydric
- HF: Asid Fluorhydric
- H2SW4: Asid sulfurik
- Hclo4: Asid perchloric
- H3PO4: Asid fosforik
- H2Co3: Asid karbonik
- Hno3: Asid nitrik
- NaOH: Natrium hidroksida
- CA (oh)2: Kalsium hidroksida
- Iman (oh)2: Ferrous hidroksida
- Iman (oh)3: Ferric Hydroxide
- NAH: Natrium hidrida
- Cu2O: Cuprous oksida
- Cuo: Cupric Oxide
- Iman2Sama ada3: Ferric Oxide
- Cl2Sama ada7: Perchloric Oxide
- Br2O: oksida hipobromus
- Yo2Sama ada3: Hypoyodose oxide
- NaCl: natrium klorida
- FECL3: Ferric Chloride
- HCO3: Natrium bikarbonat
- Ch3Laluan: Natrium asetat
- Na2SW4: Natrium sulfat
- Feso4: Sulfida ferus
- H2O: Air
- Co2: Karbon dioksida
- C6H12Sama ada6: Glukosa
- C12H22Sama adasebelas: Sukrosa
Topik lain yang menarik
Tindak balas kimia
Kimia dalam Kehidupan Seharian: Contohnya
Sebatian organik
Sebatian bukan organik
Ikatan kimia
Bahan tulen
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Wikipedia. (2021). Kompaun kimia. Diperoleh dari: dalam.Wikipedia.org
- Helmestine, Anne Marie, Ph.D. (27 Ogos 2020). Definisi Kompaun dalam Kimia. Pulih dari: Thoughtco.com
- Toppr. (s.F.). Apa itu Kompaun dalam Kimia? Jenis kompaun kimia. Pulih dari: TOPPR.com

