Kepekatan kimia

- 3854
- 1086
- Ms. Edgar Carroll
 Kepekatan kimia adalah apa yang menentukan perkadaran larut dan pelarut dalam larutan kimia
Kepekatan kimia adalah apa yang menentukan perkadaran larut dan pelarut dalam larutan kimia Apakah kepekatan kimia?
The Kepekatan kimia Ia adalah harta penyelesaian yang mewakili jumlah larutan bagi setiap unit penyelesaian. Dalam erti kata lain, ia adalah nombor yang menunjukkan perkadaran di mana larut dan pelarut berada.
Ingatlah bahawa penyelesaian adalah campuran homogen yang dibentuk oleh pelarut (umumnya cair) dan satu atau lebih bahan yang dibubarkan dalam pelarut yang kita panggil larutan. Penyelesaian dicirikan oleh pelarut, larutan dan kepekatan.
Kepekatan adalah harta benda yang sangat berguna, kerana ia membolehkan kita menggambarkannya. Sebagai contoh, jika kita tahu bahawa kepekatan garam di dalam air laut adalah 35 gram untuk setiap liter, maka kita tahu bahawa, di rumah kita kita membubarkan 35 gram garam dalam satu liter penyelesaian, kita akan memperoleh penyelesaian yang sama masin itu air laut.
Ciri -ciri kepekatan kimia
Ia adalah harta yang intensif
Ini adalah ciri utama kepekatan. Intensif bermakna bahawa ia tidak bergantung pada jumlah penyelesaian yang kita ada. Sebagai contoh, ini bermakna kepekatannya adalah sama dalam setitik air laut daripada 100 liter yang sama.
Boleh bervariasi dengan suhu
Secara umum, cecair berkembang atau meningkatkan jumlahnya semasa pemanasan. Ini juga berlaku untuk penyelesaian. Atas sebab ini, kepekatan yang dinyatakan bergantung kepada jumlah boleh berubah sedikit apabila pemanasan atau penyejukan penyelesaiannya.
Ia dapat merangkumi julat yang sangat luas
Tanpa mengira unit di mana kepekatan kimia dinyatakan, ia boleh mempunyai dari nilai yang agak besar, kepada nilai yang sangat kecil.
Sebagai contoh, kepekatan penyelesaian yang dinyatakan dalam peratusan boleh mempunyai nilai dari 0% hingga 100%, dengan itu meliputi banyak pesanan magnitud. Kami dapat menyediakan penyelesaian 90%, kerana kami juga dapat menyediakan satu demi 10-12%, yang hampir 14 pesanan magnitud kecil.
Apakah kepekatan kimia untuk?
Mengetahui kepekatan penyelesaian membolehkan kita menerangkannya. Terdapat banyak sifat penyelesaian yang bergantung kepada kepekatan mereka. Sebagai contoh, titik lebur dan mendidih bergantung kepada kepekatan, jadi mengetahui ia membolehkan kita mengira kedua -dua sifat ini.
Boleh melayani anda: keadaan vitreousSebaliknya, kepekatan membolehkan kita dengan mudah membandingkan penyelesaian dengan yang lain. Sekiranya kita mempunyai dua penyelesaian air dengan gula, mengetahui kepekatan mereka akan membolehkan kita mengetahui yang mana kedua -duanya lebih manis.
Di samping.
Sebagai contoh, kepekatan oksigen di udara menentukan sama ada seseorang akan mati lemas atau tidak; PH penyelesaian (yang merupakan cara untuk mengukur kepekatan ion h+) Menentukan sama ada bakteria akan hidup dan menghasilkan semula atau jika, sebaliknya, ia akan mati; dan kepekatan racun akan menentukan sama ada ia akan mematikan atau tidak.
Jenis unit tumpuan
Kepekatan penyelesaian adalah satu, jadi tidak betul untuk bercakap mengenai jenis kepekatan. Walau bagaimanapun, kepekatan yang sama boleh dinyatakan dalam pelbagai jenis unit tumpuan. Ini adalah:
- Unit kepekatan fizikal
- Unit kepekatan kimia
Unit kepekatan fizikal
Ini dicirikan dengan menyatakan jumlah larutan dan pelarut sama ada dalam unit jisim atau kelantangan. Mereka dipanggil unit fizikal, kerana ia dikaitkan dengan massa dan jumlah dan bukannya tahi lalat dan setara.
Apabila kita membandingkan dua penyelesaian yang mempunyai kepekatan fizikal yang sama, kita tidak dapat memastikan bahawa mereka mempunyai jumlah atom dan molekul yang sama. Inilah yang membezakannya dari unit tumpuan kimia.
Unit fizikal yang paling biasa adalah:
- Tajuk Mudah (TS)
- berat/berat (%P/P) atau jisim/jisim (%m/m)
- %Berat/Volum (%P/V) atau jisim/kelantangan (%m/v)
- % volum/kelantangan (% v/v)
- Bahagian per juta berat/berat (ppmp/p) atau jisim/massa (ppmm/m)
- Bahagian per juta berat/isipadu (ppmp/v) atau jisim/kelantangan (ppmm/v)
- Bahagian per juta jumlah/kelantangan (ppmV/v)
Unit kepekatan kimia
Dalam kes unit kimia, jumlah larut dan, dalam beberapa kes, pelarut atau penyelesaiannya, dinyatakan dari segi bilangan zarah atau tahi lalat atau kesamaan yang ada dalam penyelesaiannya.
Mereka dipanggil unit kimia, kerana dua penyelesaian yang mempunyai kepekatan kimia yang sama mempunyai jumlah yang setara atom, molekul atau ion larut per unit penyelesaian, mengikut mana -mana yang berkenaan.
Boleh melayani anda: Peraturan Kelarutan: Aspek dan Peraturan UmumUnit kimia yang paling biasa adalah:
- Molariti (M)
- Molality (m)
- Pecahan molar (x)
- Normalisasi (n)
Formula unit kepekatan fizikal
Tajuk Mudah (TS)
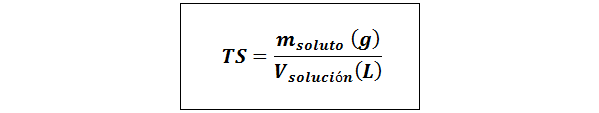
Di mana mlarut mewakili jisim larut dalam gram dan vpenyelesaian Ia adalah jumlah penyelesaian dalam liter.
berat/berat (%P/P) atau jisim/jisim (%m/m)
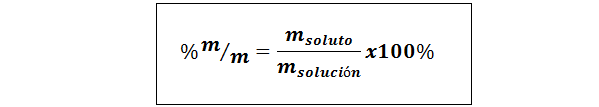
Di mana mlarut dan mpenyelesaian masing -masing mewakili jisim larut dan penyelesaiannya. Mana -mana unit jisim boleh digunakan (g, mg, kg, dll.), selagi kedua -dua massa dinyatakan dalam unit yang sama.
%Berat/Volum (%P/V) atau jisim/kelantangan (%m/v)
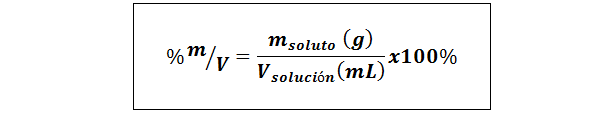
Di mana mlarut Ia adalah jisim penyelesaian dalam gram dan vpenyelesaian Ia adalah jumlah penyelesaian, dalam kes ini dalam mililiter.
% volum/kelantangan (% v/v)

Di mana vlarut dan vpenyelesaian masing -masing mewakili kelantangan larut dan penyelesaiannya. Dalam kes ini, mana -mana unit boleh digunakan untuk menyatakan jumlah ini, selagi ia sama untuk kedua -duanya.
Bahagian per juta berat/berat (ppmp/p) atau jisim/massa (ppmm/m)
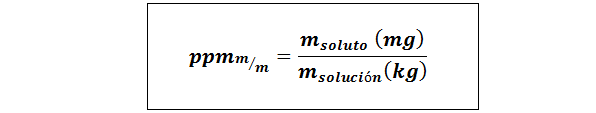
Di mana mlarut dan mpenyelesaian Mereka mewakili jisim larut dan penyelesaian dalam miligram dan kilogram masing -masing.
Bahagian per juta berat/isipadu (ppmp/v) atau jisim/kelantangan (ppmm/v)
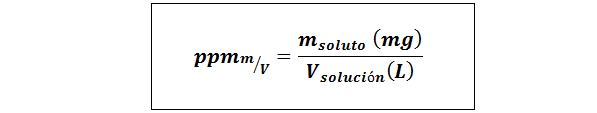
Di mana mlarut Ia adalah jisim penyelesaian dalam miligram dan vpenyelesaian Ia adalah jumlah penyelesaian, dalam kes ini dalam liter.
Bahagian per juta jumlah/kelantangan (ppmV/v)
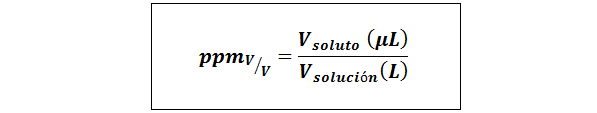
Di mana vlarut dan vpenyelesaian Mereka adalah jumlah larutan dan penyelesaian dalam microliters dan liter, masing -masing.
Formula unit kepekatan kimia
Dalam kes unit kepekatan kimia, jumlah komponen penyelesaian, khususnya larut, dinyatakan sama ada dalam bilangan tahi lalat atau bilangan setara. Jumlah ini mempunyai bilangan zarah sebenar (atom, molekul atau ion, mengikut mana -mana yang berkenaan).
Jumlah ini tidak dapat diketahui hanya dengan menimbang atau mengukur jumlah bahan, tetapi perlu mengetahui komposisi atau formula kimia sebatian untuk menentukan kepekatan. Inilah sebab utama mengapa mereka dipanggil kepekatan kimia.
Seterusnya, formula yang berbeza dibentangkan untuk mengira empat kepekatan kimia yang paling biasa digunakan:
Molariti (M)
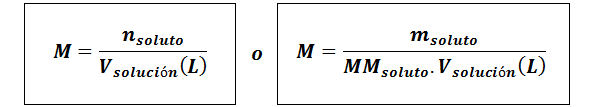
Di manalarut Mereka adalah tahi lalat larut, mlarut mewakili jisim larut dalam gram, mmlarut adalah jisim molar dan vpenyelesaian Ia adalah jumlah penyelesaian dalam liter.
Molality (m)
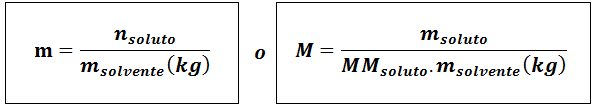
Di manalarut Mereka adalah tahi lalat larut, mlarut mewakili jisim larut dalam gram, mmlarut Ia adalah jisim molar dan mpelarut Ia adalah jisim pelarut dalam kilogram.
Boleh melayani anda: solvationPecahan molar (x)
Pecahan molar boleh dikira untuk kedua -dua larutan dan pelarut. Pecahan molar larut adalah:
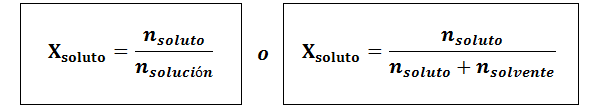
Pelarut adalah:
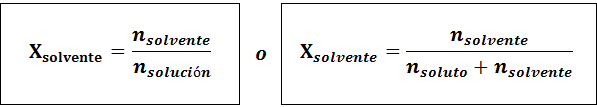
Hubungan antara kedua -dua pecahan molar adalah:
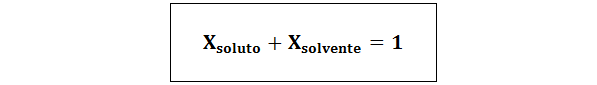
Dalam semua kes nlarut, npenyelesaian dan npelarut adalah tahi lalat larut, penyelesaian dan pelarut.
Normalisasi (n)
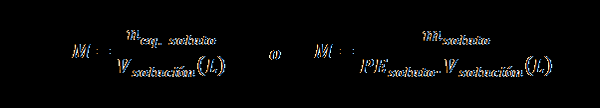
Di sini nPers. larut mewakili bilangan setara dengan larut, mlarut mewakili jisim larut, PElarut Ia adalah berat setara larut dan vpenyelesaian Ia adalah jumlah penyelesaian dalam liter.
Contoh kepekatan kimia
- Kepekatan garam dalam air laut adalah 35 g/l, yang sepadan dengan molaritas 0.60 mol/l.
- Purata kepekatan gula darah antara 82 mg/dL dan 110 mg/dL. Kepekatan ini bersamaan dengan tajuk mudah pada 0.82 g/l dan 1.10 g/l, dan dalam molariti pada 4.4.10-3 mol/l dan 6.1.10-3 mol/l, masing -masing.
- Udara boleh dianggap sebagai penyelesaian gas yang dibentuk terutamanya oleh nitrogen dan oksigen, pelarut menjadi nitrogen, kerana ia adalah lebih besar. Penyelesaian gas ini mengandungi pecahan oksigen dan nitrogen 0.22 kira -kira 0.78.
- Keluli adalah aloi antara besi dan karbon. Walaupun mereka bukan penyelesaian yang ketat, ini adalah campuran pepejal homogen yang biasanya mengandungi kepekatan karbon dalam urutan 0.03% dan 1,075% secara besar -besaran.
- Walaupun kesannya yang dahsyat untuk alam sekitar dan kesihatan manusia, kepekatan banyak bahan pencemar biasanya sangat rendah. Contohnya ialah kepekatan maksimum logam beracun arsenik di dalam air. Pertubuhan Kesihatan Sedunia (WHO) menegaskan bahawa air minuman tidak boleh mengandungi kepekatan arsenik yang lebih besar daripada 10ppb m/v (bahagian per bilion atau nanogram per liter). Kepekatan ini bersamaan dengan 0.010 ppm m/v.
Rujukan
- BBC (s. F.). Konsentrasi Penyelesaian - Pengiraan dalam Kimia - Kajian AQA - GCSE Kimia (Sains Single) - AQA. BBC diambil.co.UK.
- Inilah maksud kepekatan dalam kimia (2020). Taked dari Thoughtco.com.
- Libretexts (2022). 4.5: Kepekatan penyelesaian. Diambil dari chem.Libretxts.org.
- Mandal, a., Md. (2021). Nilai gula darah biasa. Diambil dari berita-perubatan.jaring.
- Bahan kimia.Bersih (s. F.). Kepekatan kimia. Diambil dari chemics.jaring.

