Apakah elemen elektronegatif yang paling banyak dan mengapa?
- 1817
- 535
- Dallas Bernhard
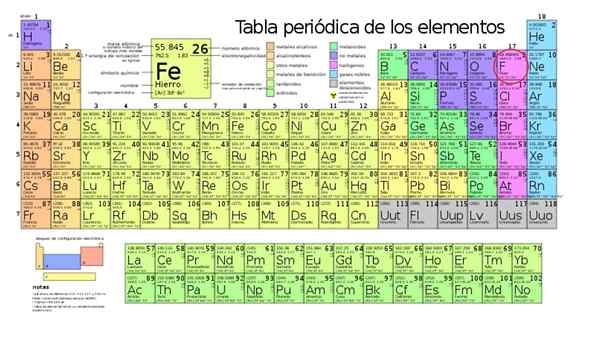
 Unsur yang paling elektronegatif ialah fluorida (F), terkunci dalam bulatan merah
Unsur yang paling elektronegatif ialah fluorida (F), terkunci dalam bulatan merah Dia lebih banyak elemen elektronegatif Dalam jadual berkala ia adalah Fluorin, yang bahan kimianya adalah f dan milik kumpulan halogen. Di antara semua elemen jadual berkala, fluorida adalah yang paling ingin menangkap elektron dari atom lain.
Unsur ini, gas pada suhu bilik, sangat reaktif dan oleh itu tidak mudah untuk mencarinya dalam keadaan murni. Fluorin mudah dihubungkan dengan elemen lain seperti sulfur, kalsium dan logam, serta sebatian, terutama yang mengandungi hidrogen.
Elektronegativiti yang tinggi membolehkan anda menggabungkan dengan gas mulia seperti Xenon, Kripton dan Radon.
Selepas fluorin, oksigen adalah elemen kedua dengan elektronegativiti tertinggi. Sebaliknya, unsur -unsur dengan elektronegativiti terendah ialah Francio (FR) dan Cesium (CS).
 Kerana ia adalah elemen yang paling elektronegatif, fluorin membentuk banyak sebatian, seperti fluorit, atau fluorida kalsium. Sumber: Wikimedia Commons
Kerana ia adalah elemen yang paling elektronegatif, fluorin membentuk banyak sebatian, seperti fluorit, atau fluorida kalsium. Sumber: Wikimedia Commons Oleh itu, ini adalah yang paling banyak Electropositive yang wujud, walaupun Francio adalah radioaktif dan sangat sedikit.
Elektronegativiti dan jadual berkala
Skala elektronegativiti telah dibangunkan oleh ahli kimia dan hadiah Nobel Linus Pauling (1901-1994), walaupun konsep itu disebabkan oleh ahli kimia Sweden Jöns Jakob Berzelius (1779-1848).
Skala Pauling, yang memberikan nilai berangka dimensi kepada elektronegativiti, digunakan untuk mengukur intensiti yang mana atom menarik elektron atom lain yang berbeza, dan dengan itu membentuk pautan.
Setiap elemen mempunyai elektronegativiti sendiri, yang bergantung kepada sifat atomnya. Ia ditentukan secara eksperimen dan tidak langsung, sebagai contoh, mengukur tenaga pautan, seperti yang dilakukan Pauling sekitar tahun 1932.
Pada Skala Elektronegativiti Pauling, Fluoride adalah yang pertama, dengan nilai anggaran 3.98 ≈ 4.0.
Boleh melayani anda: hidrokarbon alifatik: sifat, tatanama, reaksi, jenisElektronegativiti adalah harta berkala unsur -unsur. Dalam kebanyakan kes (terdapat beberapa pengecualian), diperhatikan bahawa elektronegativiti meningkat apabila bergerak dari kiri ke kanan melalui barisan jadual berkala.
Dan juga, peningkatan dari bawah ke atas, dengan bergerak di lajur.
 Jadual berkala elektronegativiti mengikut skala Pauling. Fluorin adalah elemen yang paling elektronegatif, yang terletak di atas dan di sebelah kanan, sementara Francio adalah elektronegatif paling kurang semua, atau yang paling elektropositif, jika disukai, dan berada di lajur kiri dan ke bawah. Sumber: f. Zapata.
Jadual berkala elektronegativiti mengikut skala Pauling. Fluorin adalah elemen yang paling elektronegatif, yang terletak di atas dan di sebelah kanan, sementara Francio adalah elektronegatif paling kurang semua, atau yang paling elektropositif, jika disukai, dan berada di lajur kiri dan ke bawah. Sumber: f. Zapata. Elektronegativiti fluorin
Sebab fluorin adalah unsur yang paling elektronegatif dalam jadual berkala, adalah disebabkan oleh konfigurasi elektroniknya (cara elektronnya diatur dalam orbital di sekitar nukleus).
Konfigurasi ini adalah 1s22s22 p5, Jadi fluorida mempunyai 5 elektron di lapisan paling luarnya.
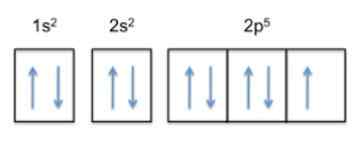
Sekarang, kerana trend atom adalah untuk melengkapkan lapisan luarnya, itu bermakna bahawa fluorin akan menerima elektron atom lain dengan mudah, untuk mendapatkan kestabilan dan menyerupai gas mulia baris yang sama, iaitu neon , yang konfigurasi elektroniknya adalah 1s22s22 p6.
Atom fluorin mempunyai jejari yang sangat kecil, kerana proton dalam nukleus mereka menarik elektron dengan sangat kuat, menjaga mereka lebih dekat daripada atom -atom yang kurang elemen elektronegatif, seperti Cessium dan Francio.
Oleh itu, yang terakhir sanggup menyerahkan elektron dengan mudah untuk membentuk pautan.
Rujukan
- Aguilar, c. Panduan untuk unit pembelajaran kimia i. Diperolehi dari: IPN.mx.
- Atkins, ms. (2005). Prinsip Kimia, Laluan Penemuan. Ke -3. Edisi. Pan -American Editorial.
- Clark, j. Electronegives. Pulih dari: chem.Libretxts.org.
- Hein, m. (2014). Asas Kimia Kolej. Edisi ke -14. Wiley.
- Lentech. Unsur -unsur kimia yang diperintahkan oleh elektronegativiti. Pulih dari: lentech.adalah.

