Ikatan kimia
- 3700
- 457
- Delbert Dare
Kami menerangkan apa pautan kimia, jenis yang ada, dan kami memberikan banyak contoh
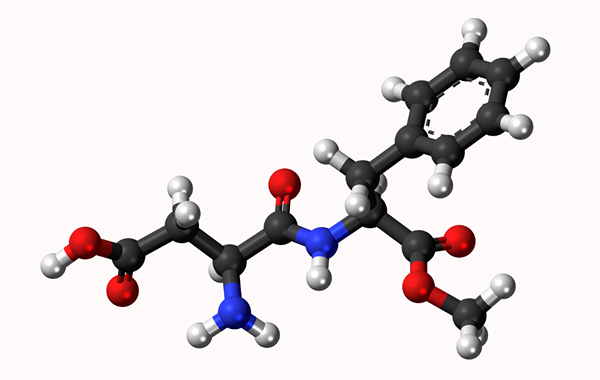
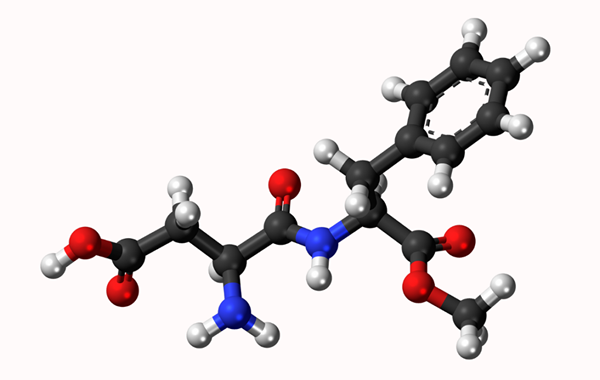 Model Molekul Aspartamo: Pautan mudah diwakili oleh garis dan ikatan berganda dengan dua baris. Bola adalah atom
Model Molekul Aspartamo: Pautan mudah diwakili oleh garis dan ikatan berganda dengan dua baris. Bola adalah atom Apa itu ikatan kimia?
A Ikatan kimia Ia adalah kekuatan yang bersatu dengan atom -atom sebatian. Daya yang menyatukan atom adalah elektromagnet, dan apabila atom -atom terikat mereka mengekalkan sifat mereka sendiri.
Sebagai contoh, air biasa dibentuk kerana kesatuan dua atom hidrogen (h2) dan salah satu oksigen (O); Itulah sebabnya formula kimianya adalah h2Sama ada. Walaupun mereka bersatu untuk membentuk air, atom hidrogen kekal hidrogen dan oksigen masih oksigen.
Ingatlah bahawa atom dibentuk oleh nukleus yang dikelilingi oleh awan elektron, yang mempunyai beban negatif. Nukleus atom mempunyai caj positif, yang berjaya menarik elektron.
Walau bagaimanapun, elektron juga tertarik dengan nukleus atom lain. Ini adalah bagaimana pautan kimia terbentuk. Fakta bahawa atom menghasilkan atau berkongsi elektron menghasilkan pelbagai jenis pautan kimia.
Dalam ikatan kimia, atom menghasilkan, memenangi atau berkongsi elektron dari apa yang disebut lapisan Valencia, yang merupakan lapisan paling luar atom di mana kereaktifan berlaku atau kecenderungan untuk membentuk ikatan kimia.
Pautan ini menjadikan bahan baru (bukan campuran) yang tidak dapat dipisahkan melalui teknik seperti ayak atau penapisan.
Jenis ikatan kimia
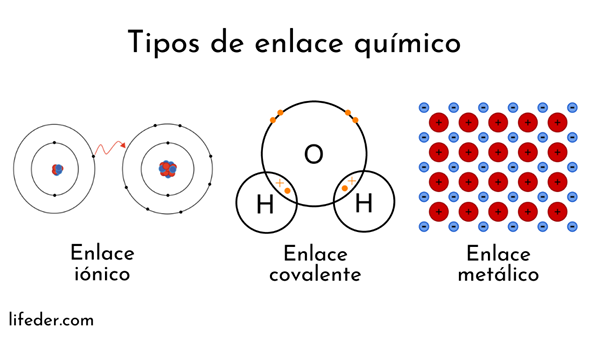
Atom dibentuk oleh nukleus (dengan caj elektrik positif) dan elektron (zarah dengan cas elektrik negatif) yang berputar di sekitar. Kedua -dua pihak campur tangan dalam ikatan kimia.
Ikatan kimia yang melibatkan nukleus atom dipanggil logam. Sebaliknya, mereka yang melibatkan pertukaran elektron dibahagikan kepada ion dan kovalen.
Boleh melayani anda: chlorobenzene (c6h5cl)Pautan ionik
Pautan jenis ini sangat tahan; menghasilkan sebatian kimia pepejal (kristal) di dalam air dan dengan titik lebur yang tinggi (antara 300 dan 1.000 darjah Celsius). Dibubarkan di dalam air, mereka adalah konduktor elektrik.
Bagaimana pautan ionik?

Ikatan ionik berlaku di antara logam dan bukan logam yang mempunyai elektronegativiti yang berbeza (keupayaan untuk menarik elektron). Elektron lapisan Valencia satu atom melewati ke atom Valencia yang lain. Yang sama; Atom logam memberikan elektron kepada atom bukan logam, mencapai kestabilan elektronik.
Sepanjang ion proses pembentukan pautan (kation dan anion) dibentuk, oleh itu nama bon ionik.
Contoh ikatan jenis ini adalah natrium klorida: sebatian kimia ini terbentuk apabila klorin (CL) menarik elektron lapisan valensi yang mempunyai atom natrium (NA).
Contoh lain ialah mangan klorida (MGC), yang digunakan dalam pembuatan lukisan dan kuman. Akibat ikatan kimia, elektron atom mangan diserap oleh atom klorin.
Pautan kovalen
Ikatan kovalen sangat sukar dan menjana sebatian kimia yang tidak larut dengan suhu gabungan yang tinggi (lebih dari 1.000 darjah Celsius). Mereka tidak menjalankan elektrik.
Mengikut cara atom berkongsi elektron mereka, ikatan kovalen boleh:
- Mudah: Mereka berkongsi beberapa elektron (a-a).
- Ganda: Kongsi dua pasangan elektron (a =).
- Triple: Kongsi tiga pasangan elektron (A≡A).
Bagaimana ikatan kovalen terbentuk?

Ikatan kovalen dibentuk apabila dua elemen bukan logam berkongsi elektron lapisan valensi mereka.
Ia boleh melayani anda: Rubidio: Sejarah, Hartanah, Struktur, Mendapatkan, MenggunakanPertukaran elektron selalu berlaku sedemikian rupa sehingga ia mematuhi undang -undang oktet. Ini adalah prinsip kimia yang menyatakan bahawa konfigurasi yang paling stabil untuk atom adalah satu di mana ia mempunyai lapan elektron di lapisan paling luarnya.
Contoh ikatan kovalen adalah air (h2Sama ada). Untuk mencipta molekul air, dua ikatan kovalen mudah diperlukan. Dalam ikatan mudah, elektron hidrogen dikongsi dengan oksigen, dan oksigen berkongsi elektron dengan hidrogen.
Contoh ikatan kovalen lain ialah karbon dioksida (CO2), salah satu yang bertanggungjawab utama untuk kesan rumah hijau dan perubahan iklim. Untuk membentuk kompaun ini, karbon dan oksigen membuat dua ikatan berganda, iaitu, untuk setiap pautan dua pasang elektron berkongsi.
Pautan logam
Jenis pautan ini hanya berlaku dalam elemen logam. Ia terdiri daripada kesatuan nukleus dua atom elemen logam yang sama bersama dengan elektron mereka.
Pautan logam dicirikan dengan menjadi konduktor elektrik yang berkesan, mempunyai titik gabungan dan mendidih yang sangat tinggi, dan mudah dioksidakan. Mereka juga mudah dibentuk dan tahan terhadap awal, sangat kukuh dan kuat.
Bagaimana pautan logam?
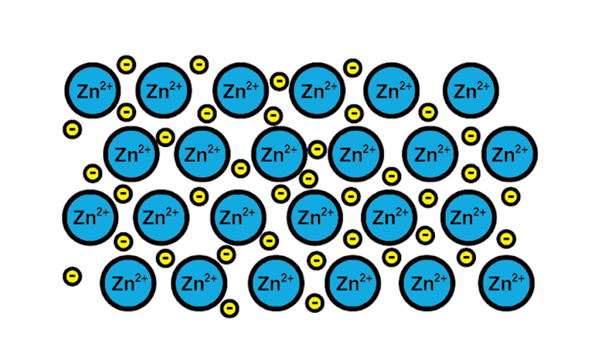 Pautan logam zink
Pautan logam zink Contoh pautan logam ialah zink, elemen logam. Proses latihan jenis pautan ini adalah:
1-nukleus atom unsur logam memenuhi nukleus lain dari elemen yang sama.
2-elektron lapisan Valencia dari kedua-dua nukleus menjadi laut elektron di sekitar. Iaitu, mereka tidak mengorbit nukleus atom tunggal.
3-beban positif nukleus atom dan negatif elektron tertarik. Hasilnya ialah elektron valensi yang membentuk laut elektron di sekitar nukleus atom (kation).
Ia boleh melayani anda: tembaga sulfat (cuso4): struktur, sifat, mendapatkan, menggunakanContoh ikatan kimia
Pautan ionik
- Barium Oxide (BAO).
- Magnesium Chloride (MGCL2).
- Kalsium oksida (CAO)
- Nitrat Perak (AGNO3)
- Zink hidroksida (ZnOH2)
- Potassium Bromide (KBR)
- Kalsium karbonat (Caco3)
- Sulfat tembaga (CUO4)
- Lithium fluoride (LIF)
- Mangan klorida (MNCL2)
- Kalium sulfat (k2SW4)
- Oksida besi (hodoh)
- Disodium fosfat (NA2HPO4)
- Potassium Ioduro (ki)
Pautan kovalen
- Karbon dioksida (CO2)
- Ammonia (NH3)
- Paraffin (Cnh2N+2)
- Diesel (c12H26)
- Dibromo (Br2)
- Karbon monoksida (CO)
- Butano (c4H10)
- Benzene (c6H6)
- Nitrogen molekul (n2)
- Metana (ch4)
- Asid hidroklorik (HCL)
- Asid Cyanhydric (HCN)
Pautan logam
Mana -mana logam dalam keadaan tulennya adalah contoh pautan logam, iaitu:
- Nikel (ni)
- Besi (Iman)
- Aluminium (AL)
- Titanium (Ti)
- Lead (PB)
- Cobalt (CO)
- Tembaga (Cu)
- Zink (Zn)
- Mercury (HG)
- Emas (au)
- Perak (AG)
- Barium (BA)
Kepentingan ikatan kimia
Kepentingan ikatan kimia adalah bahawa mereka membentuk molekul organik dan bukan organik, dan dengan cara ini mereka adalah sebahagian daripada asas semua organisma hidup. Sekiranya mereka tertakluk kepada syarat -syarat tertentu, pautan ini boleh dipecahkan. Tenaga ini dipanggil Pautan tenaga.
Beberapa teknik untuk memecahkan pautan digunakan oleh elektrik, suhu tinggi atau menimbulkan tindak balas kimia dengan sebatian yang berbeza.
Sebagai contoh, untuk memisahkan molekul oksigen dan hidrogen dari H2Atau, kita boleh menggunakan elektrik ke air, yang merupakan proses yang dikenali sebagai elektrolisis.
Sebatian kimia yang dibentuk oleh pautan banyak dan hadir dalam kehidupan seharian. Garam yang kami gunakan untuk makanan musim adalah produk kompaun kimia hubungan antara natrium (NA) dan satu atom klorin (CL) (CL). Formula kimianya adalah NaCl, yang membaca natrium klorida.

