Deuterium
- 3214
- 137
- Donnie Ryan
Apa itu deuterium?
Dia deuterium Ia adalah salah satu spesies hidrogen isotop, yang diwakili sebagai d atau 2H. Di samping itu, nama hidrogen berat telah diberikan, kerana jisimnya adalah dua kali ganda dari proton. Isotop adalah spesies yang berasal dari elemen kimia yang sama, tetapi bilangan jisimnya berbeza dari ini.
Perbezaan ini disebabkan oleh perbezaan bilangan neutron yang ada. Deuterium dianggap sebagai isotop yang stabil dan boleh didapati dalam sebatian yang dibentuk oleh hidrogen asal semula jadi, walaupun dalam perkadaran yang agak kecil (kurang daripada 0.02 %).
Memandangkan sifatnya, sangat mirip dengan hidrogen biasa, ia boleh menggantikan hidrogen dalam semua reaksi di mana ia mengambil bahagian, menjadi bahan yang setara.
Atas sebab ini dan lain -lain, isotop ini mempunyai banyak aplikasi dalam bidang sains yang berbeza, menjadi salah satu yang paling penting.
Struktur deuterium
Struktur deuterium kebanyakannya dibentuk oleh nukleus yang mempunyai proton dan neutron, dengan berat atom atau jisim kira -kira 2,014 g.
Begitu juga, isotop ini berhutang penemuannya kepada Harold C. Urey, ahli kimia dari Amerika Syarikat, dan kolaboratornya Ferdinand Brickwedde dan George Murphy, pada tahun 1931.

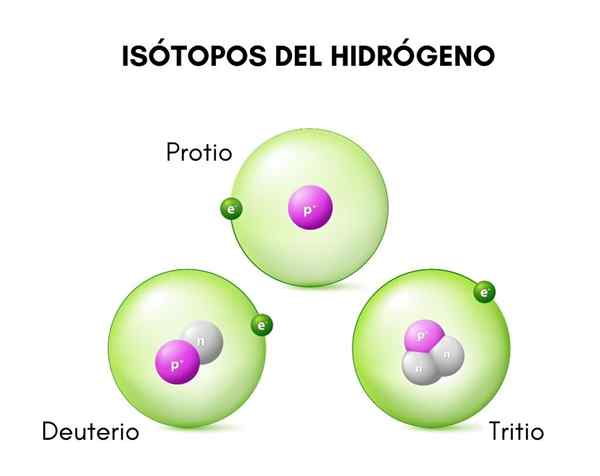
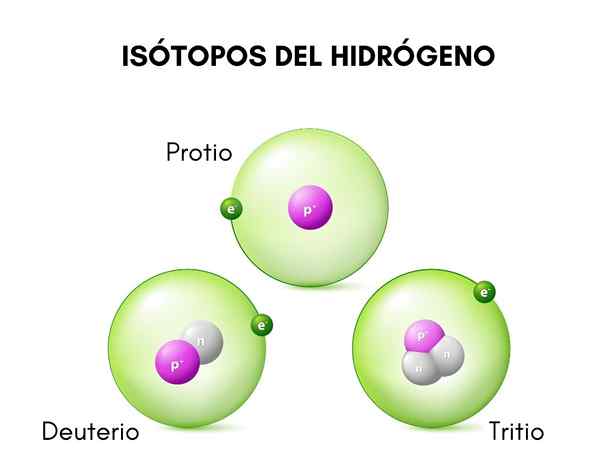
Di bahagian atas, anda dapat melihat perbandingan antara struktur isotop hidrogen, yang wujud dalam bentuk protio (isotop yang paling banyak), deuterium dan tritium, yang diperintahkan dari kiri ke kanan.
Penyediaan deuterium dalam keadaan murni telah dijalankan dengan jayanya untuk kali pertama pada tahun 1933, tetapi sejak tahun 1950 -an bahan fasa pepejal telah digunakan dan telah menunjukkan kestabilan, yang dipanggil litium deuteride (LID), untuk menggantikan deuterium dan tritium di dalam sebilangan besar tindak balas kimia.
Boleh melayani anda: klorin oksida (iii): sifat, struktur, kegunaanDalam pengertian ini, kelimpahan isotop ini telah dikaji dan telah diperhatikan bahawa perkadarannya di dalam air boleh berubah sedikit, bergantung kepada sumber dari mana sampel diambil.
Di samping itu, melalui kajian spektroskopi kewujudan isotop ini di planet lain galaksi ini telah ditentukan.
Beberapa data mengenai deuterium
Perbezaan asas antara isotop hidrogen (yang merupakan satu -satunya yang telah dinamakan dengan cara yang berbeza) terletak pada struktur mereka, kerana jumlah proton dan neutron spesies memberikan sifat kimianya.
Sebaliknya, deuterium yang ada di dalam badan bintang dihapuskan dengan kelajuan lebih cepat daripada yang berasal.
Di samping itu, dianggap bahawa fenomena alam semula jadi yang lain hanya membentuk jumlah yang sangat kecil, jadi pengeluarannya terus menghasilkan minat hari ini.
Begitu juga, satu siri penyiasatan telah mendedahkan bahawa sebahagian besar atom yang telah terbentuk dari spesies ini berasal dari Big Bang; Inilah sebab mengapa kehadirannya di planet besar seperti Musytari diberi amaran.
Sebagai cara yang paling biasa untuk mencapai spesies ini adalah apabila ia digabungkan dengan hidrogen dalam bentuk protio, kepentingan masyarakat saintifik masih dibangkitkan oleh hubungan yang ditubuhkan antara perkadaran kedua -dua spesies dalam bidang sains yang berlainan, seperti itu, seperti itu sebagai astronomi atau cuaca.
Boleh melayani anda: Renio: penemuan, sifat, struktur, kegunaanSifat deuterium
- Ia adalah isotop yang tidak mempunyai ciri -ciri radioaktif; iaitu, ia agak stabil.
- Ia boleh digunakan untuk menggantikan atom hidrogen dalam tindak balas kimia.
- Spesies ini menunjukkan tingkah laku selain daripada hidrogen biasa dalam tindak balas biokimia.
- Apabila kedua -dua atom hidrogen diganti di dalam air, D diperoleh2Atau, memperoleh nama air berat.
- Hidrogen yang terdapat di lautan yang dalam bentuk deuterium wujud dalam perkadaran 0.016 % berhubung dengan protio.
- Di bintang -bintang, isotop ini mempunyai kecenderungan untuk bersatu dengan cepat untuk menimbulkan helium.
- D2Atau membentuk spesies toksik, walaupun sifat kimianya sangat mirip dengan H2
- Apabila atom deuterium tertakluk kepada proses gabungan nuklear pada suhu tinggi, detasmen tenaga besar diperolehi.
- Ciri -ciri fizikal seperti titik mendidih, ketumpatan, haba pengewapan, titik tiga, antara lain, mempunyai magnitud utama dalam molekul deuterium (D2) bahawa dalam hidrogen (h2).
- Cara yang paling biasa di mana ia dijumpai dikaitkan dengan atom hidrogen, menyebabkan hidrogen deuteride (HD).
Penggunaan/aplikasi
Oleh kerana sifatnya, deuterium digunakan dalam pelbagai aplikasi di mana hidrogen terlibat. Beberapa kegunaan ini diterangkan di bawah:
- Dalam bidang biokimia ia digunakan dalam penanda isotop, yang terdiri daripada "menandakan" sampel dengan isotop yang dipilih untuk mengesannya melalui laluannya melalui sistem tertentu.
Boleh melayani anda: asid kuat- Dalam reaktor nuklear yang menjalankan tindak balas gabungan, ia digunakan untuk mengurangkan kelajuan yang neutron bergerak tanpa penyerapan tinggi ini yang dibentangkan oleh hidrogen biasa.
- Di kawasan resonans magnetik nuklear (NMR), pelarut berdasarkan deuterium digunakan untuk mendapatkan sampel spektroskopi jenis ini tanpa kehadiran gangguan yang dihasilkan dengan menggunakan pelarut terhidrogenasi.
- Dalam bidang biologi, makromolekul dikaji melalui teknik penyebaran neutron, di mana sampel yang disediakan dengan deuterium digunakan untuk mengurangkan bunyi bising dengan ketara dalam sifat kontras ini.
- Di kawasan farmakologi, penggantian hidrogen digunakan oleh deuterium dengan kesan isotopik kinetik yang dihasilkan dan membolehkan ubat -ubatan ini mempunyai separuh masa yang lebih lama.