Elektroforesis asas, teknik, apa itu, contohnya

- 3674
- 577
- Ms. Micheal Rippin
The Elektroforesis Ini adalah teknik yang digunakan untuk memisahkan molekul dalam medan elektrik. Ia harus dilakukan, khususnya, dengan penghijrahan zarah yang dimuatkan di bawah pengaruh arus elektrik yang digunakan di antara dua tiang, satu positif dan lain -lain negatif.
Elektroforesis kini merupakan salah satu prosedur paling rutin yang berlaku semasa pembangunan percubaan, terutamanya dalam bidang yang berkaitan dengan kimia analisis, biokimia dan sains biologi dan perubatan secara umum.
 Baldi elektroforesis. Sumber: Melodygar/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/4.0)
Baldi elektroforesis. Sumber: Melodygar/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/4.0) Ia digunakan untuk memisahkan protein, peptida, DNA, RNA dan lain -lain mengikut beban, saiz, ketumpatan dan kesucian mereka.
Rumah komersial yang berbeza telah merancang format yang berbeza, dengan aplikasi yang berbeza dan keuntungan yang sesuai untuk tujuan tertentu, bagaimanapun, semua prosedur memerlukan unsur -unsur asas yang sama:
- Sumber tenaga untuk menjana cas elektrik
- Sederhana sokongan untuk pemisahan
- Penyelesaian penampan (penampan) Untuk menjaga pH tetap
[TOC]
Asas
Elektroforesis tidak lebih daripada penghijrahan (pemisahan) zarah atau molekul yang dimuatkan (secara semulajadi atau buatan) dalam medium atau sokongan di bawah pengaruh medan elektrik.
Teknik ini didasarkan pada salah satu persamaan fizikal utama elektromagnetisme, mengikut mana daya itu sama dengan cas elektrik yang didarabkan oleh medan elektrik yang digunakan pada titik itu (f (force) = q (caj elektrik) x e (medan elektrik ).
Mengikut persamaan ini, dua zarah dengan jisim yang sama, tetapi beban yang berbeza, akan bergerak ke kadar yang berbeza dalam medan elektrik yang sama. Di samping itu, kelajuan pergerakan zarah -zarah ini bergantung kepada hubungan antara beban dan jisim mereka.
Para saintis telah memanfaatkan sifat -sifat ini dan hubungan kargo/massa untuk memisahkan komponen dari biomolekul di bahagian terkecil mereka, serta memisahkan molekul yang berbeza dalam campuran, antara aplikasi lain.
Adalah penting untuk diingat bahawa molekul biologi seperti asid amino, peptida, protein, beberapa karbohidrat, nukleotida dan asid nukleik semuanya mempunyai sesuatu yang kita sebut sebagai "kumpulan yang dapat diubahsuai", sehingga mereka boleh wujud sebagai spesies positif atau negatif di bawah keadaan tertentu pH.
Teknik
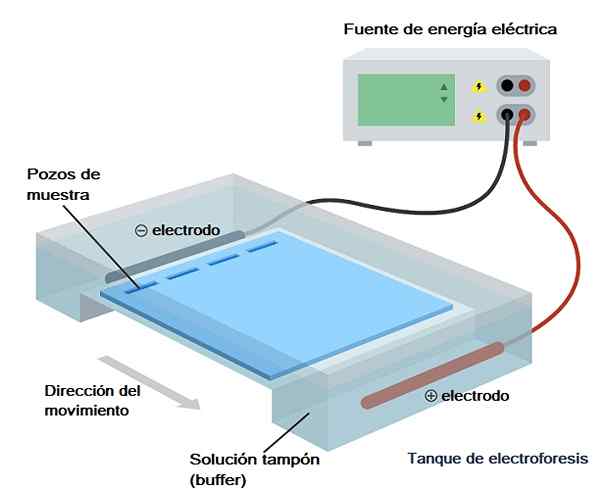
Walaupun terdapat pelbagai jenis elektroforesis, elektroforesis gel adalah yang paling banyak digunakan dalam analisis biokimia, biologi molekul dan bioteknologi, jadi ia akan menjadi apa yang akan kita bincangkan secara ringkas dari segi teknikal.
Seperti namanya, elektroforesis gel membayangkan penggunaan medium sokongan pepejal berbentuk pepejal, sama ada untuk analisis/pemisahan campuran protein atau asid nukleik (DNA dan/atau RNA) di bawah pengaruh medan elektrik.
Sistem atau radas yang digunakan untuk melakukan "larian" elektroforetik boleh mendatar (biasanya digunakan untuk asid nukleik) atau menegak (biasanya digunakan untuk protein).
- Contoh teknik elektroforesis asid nukleat
Asid nukleik biasanya dipisahkan menggunakan gel agarose (galaktosa polysaccharide) yang disediakan dengan larutan penampan yang mencukupi (Tris/acetate/EDTA atau Tris/borato/EDTA) dan kepekatannya akan menentukan "resolusi" serpihan saiz yang berbeza.
Boleh melayani anda: rantaian makanan bumi: pautan dan contohPenyediaan sampel
Langkah pertama sebelum melakukan larian elektroforetik dalam gel agarose adalah untuk mendapatkan sampel. Ini bergantung kepada hujung eksperimen dan sampel boleh menjadi hasil pencernaan enzimatik, pada tindak balas rantai polimerase (PCR), pemurnian asid nukleik, dll.
 Campurkan sampel dengan buff beban.Org/lesen/by/4.0) melalui Wikimedia Commons)
Campurkan sampel dengan buff beban.Org/lesen/by/4.0) melalui Wikimedia Commons) Selepas mendapat, ini dicampur dengan penyelesaian berwarna (penyelesaian beban) yang membolehkan pemendapan cepat sampel di dalam telaga, kerana ia mempunyai gliserol dan pewarna yang membolehkan larian secara visual.
Penyediaan gel
Langkah ini terdiri daripada mencampurkan jumlah yang diperlukan dari substrat gelling (agarose) dengan penyelesaian penampan, mencairkannya menggunakan haba dan mengukuhkannya dengan sokongan yang berfungsi sebagai "acuan".
Semasa gelicification beberapa "sikat" diperkenalkan ke dalam gel yang diposisikan dalam "acuan" untuk membatasi "telaga" di mana sampel akan diperkenalkan sebelum larian.
Sebaik sahaja gel telah disejukkan dan dikuatkan, "sikat" dikeluarkan dan ia diperkenalkan ke dalam bekas yang dikenali sebagai "baldi", yang penuh dengan penyelesaian penampan yang berjalan, (Tris/acetate/EDTA atau Tris/Borato/Borato/EDTA).
Baldi ini, pada gilirannya, termasuk dalam apa yang disebut "ruang elektroforetik", yang tidak lebih daripada bekas di mana medan elektrik diluluskan dan mempunyai ruang di mana gel diperkenalkan dan dua bahagian yang dipenuhi Penyelesaian Buffer (penampan lari).
Kamera ini mempunyai dua elektrod, satu positif dan satu negatif, di antaranya pergerakan ion dihasilkan selepas penggunaan medan elektrik (ia disambungkan ke sumber kuasa).
Memuatkan sampel
Sebaik sahaja sampel bercampur dengan penyelesaian beban masing -masing, ini diperkenalkan ke dalam "telaga" yang sebelum ini dibuat ke dalam gel.
Oleh kerana asid nukleik mempunyai beban bersih negatif, mereka berhijrah dari tiang negatif kepada yang positif, jadi ini mesti diambil kira apabila kamera disambungkan ke sumber kuasa, memastikan tiang negatif sepadan dengan tapak paling di sebelah tempat itu di mana sampel dimuatkan.
Masa Corrida ditubuhkan dalam ketergantungan yang ketat terhadap penyelidik yang bertanggungjawab terhadap eksperimen. Voltan biasanya dikira dalam nisbah 5 volt peratus dalam gel yang memisahkan dua elektrod.
Paparan
Apabila gel berjalan (apabila sampel telah mengembara gel dari satu hujung ke yang lain), ia tenggelam dalam larutan etid bromida (ETBR), pewarna yang diselaraskan antara pangkalan nitrogen dan "jenama" Mereka boleh digambarkan dalam transilumenan menggunakan cahaya ultraviolet.
Apa itu elektroforesis untuk?
Elektroforesis secara historis digunakan dengan pelbagai tujuan. Walau bagaimanapun, hari ini kegunaannya bergantung pada "soalan" yang ditanya oleh penyelidik berhubung dengan fenomena atau sistem tertentu, serta jenis elektroforesis yang dia ingin gunakan.
Boleh melayani anda: topoisomerase: apa, ciri, fungsi, jenisWalau bagaimanapun, kita boleh mendapatkan beberapa fungsi utama yang teknik ini, bermula dengan yang paling "jarang" dan berakhir dengan yang paling popular dan kebanyakannya dieksploitasi dalam dunia sains biologi. Elektroforesis berguna:
- Untuk analisis kuantitatif campuran kompleks makromolekul dan untuk pengiraan potensi "zeta" (sifat koloid zarah dalam medium cecair di bawah pengaruh medan elektrik statik).
- Untuk analisis sera darah untuk tujuan diagnostik.
- Untuk pemisahan glukoprotein, lipoprotein dan hemoglobin darah.
- Untuk analisis makanan, produk farmaseutikal dan bahan pencemar alam sekitar.
Elektroforesis dalam gel agarose
- Untuk pemisahan serpihan DNA selepas pencernaan dengan enzim sekatan.
- Untuk pemisahan molekul asid nukleik sebelum dipindahkan ke membran untuk analisis berikutnya.
- Untuk analisis produk PCR (tindak balas rantai polimerase) mengesahkan sama ada ia berlaku atau tidak.
- Untuk anggaran saiz molekul dalam campuran DNA atau RNA.
- Untuk anggaran kuantiti dan/atau kualiti asid nukleik yang disucikan.
Elektroforesis dalam gel polyacrylamide di bawah keadaan denaturalisasi atau asli
- Untuk menentukan saiz protein.
- Untuk mengenal pasti protein.
- Untuk menentukan kesucian sampel selepas beberapa langkah pembersihan.
- Untuk mengenal pasti kehadiran pautan disulfida intramolekul.
- Untuk menentukan interaksi antara protein.
- Untuk menentukan titik isoelektrik protein.
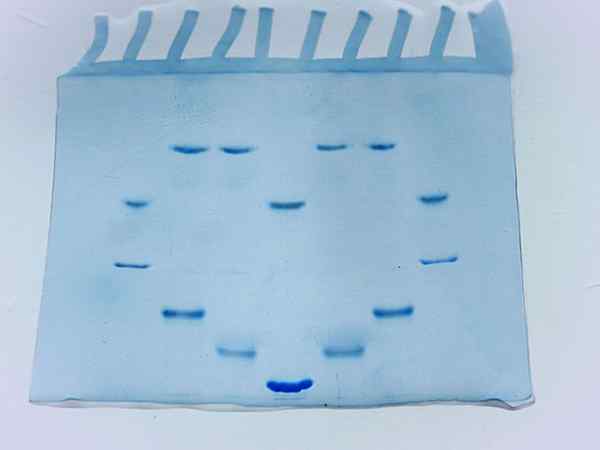 Fotografi gel acrylamide selepas menjalankan beberapa sampel protein (Sumber: Larionova.Marina/cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0) melalui Wikimedia Commons)
Fotografi gel acrylamide selepas menjalankan beberapa sampel protein (Sumber: Larionova.Marina/cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0) melalui Wikimedia Commons) Faktor yang mempengaruhi elektroforesis
Penghijrahan zarah dalam medan elektrik bergantung kepada pelbagai faktor, antaranya:
- Caj elektrik anda
- Saiz molekulnya
- Hidrofobisinya dan bentuknya
- Besarnya medan elektrik yang digunakan
- Suhu sistem dan daya ionik penyelesaian penampan yang digunakan
- Sifat persekitaran di mana ia berada
Berhubung dengan sampel
Antara parameter yang berkaitan dengan zarah (sampel) yang tertakluk kepada medan elektrik, faktor utama yang mempengaruhi proses ini berkaitan dengan beban mereka, saiz dan bentuknya.
Semakin besar beban bersih zarah, semakin besar kadar penghijrahannya dan magnitud ini bergantung pada pH. Walau bagaimanapun, hubungan dengan saiz berkadar songsang, yang bermaksud bahawa lebih "besar" molekul, semakin perlahan -lahan berhijrah.
Ia boleh melayani anda: Lia Agar (Iron Lysine): Apa, Yayasan, Penyediaan, KegunaanBerhubung dengan medan elektrik
Setakat ini kita telah membincangkan kepentingan medan elektrik untuk mencapai pergerakan zarah oleh elektroforesis, tetapi kita tidak menentukan apa itu: daya elektrik per unit beban atau, dalam istilah yang lebih mudah, kawasan ruang di mana terdapat daya elektrik.
Parameter mengenai medan elektrik yang boleh menjejaskan penghijrahan adalah voltan, semasa dan rintangan.
Voltan mempengaruhi "masa penerbangan" molekul yang dipisahkan selepas menggunakan medan elektrik. Semakin tinggi, semakin cepat langkah ini.
Elektron semasa (berterusan dan seragam yang "ditolak" oleh sumber voltan) dijalankan di antara elektrod sistem elektroforetik terima kasih kepada ion -ion yang terdapat dalam penyelesaian penampan. Berkaitan secara langsung dengan voltan.
Berhubung dengan penyelesaian penampan
Komposisi, daya ionik dan pH penyelesaian penampan adalah parameter utama yang mempengaruhi "larian" elektroforetik, kerana mereka secara langsung mempengaruhi beberapa sifat sampel, terutama caj elektrik.
Kerana? Penyelesaian penampan menstabilkan pH medium sokongan di mana elektroforesis berlaku. Komposisinya boleh menjejaskan anjakan zarah -zarah yang bermigrasi dan kepekatan ionik juga, kerana ia secara langsung berkaitan dengan semasa.
Berhubung dengan medium sokongan
Jenis dan format elektroforesis yang berlainan juga menunjukkan media yang berbeza di mana penghijrahan berlaku dan di mana ia boleh kemudian "didaftarkan".
Kadar penghijrahan molekul yang tertakluk kepada elektroforesis bergantung kepada jenis medium sokongan, yang biasanya tidak sesuai.
Ciri-ciri penyerapannya, elektroendo-osmosis adalah penting (kapasiti pergerakan cecair melalui membran di bawah pengaruh medan elektrik) dan kapasiti penapis molekulnya.
Contoh penggunaan elektroforesis
Contoh klasik teknik elektroforetik yang digunakan dalam biologi dan bioteknologi termasuk:
- Elektroforesis dalam gel agarose (Bahasa Inggeris Gel Elektroforesis)
- Elektroforesis dalam gel acrylamide dalam keadaan denaturalisasi (SDS-PAGE, Bahasa Inggeris Elektroforesis gel polyacrylamide natrium dodecyl sulphat)
- Elektroforesis dalam gel acrylamide dalam keadaan asli (BN-PAGE, Bahasa Inggeris Elektroforesis gel polyacrylamide asli biru)
- Elektroforesis dalam dua dimensi (2D-halaman, dari Bahasa Inggeris Elektroforesis gel polyacrylamide dua dimensi)
- Elektroforesis kapilari (dari bahasa Inggeris Elektroforesis kapilari)
- Isolectroenfoque (Bahasa Inggeris Isolectrophocusing)
- Elektroforesis medan berdenyut (Bahasa Inggeris Elektroforesis medan berdenyut)
Rujukan
- Beck, Kevin. (2020, 25 Mei). Jenis elektroforesis. Saintifik.com. Diperolehi daripada sains.com
- Esei, UK. (November 2018). Jenis dan aplikasi elektroforesis. Diperolehi daripada Ukessays.com
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Prinsip Biokimia Lehninger. Macmillan.
- Parmar, ms. (Ogos 2018). Elektroforesis: makna, definisi dan klasifikasi (dengan rajah). Teknologi Bio. Diperolehi daripada bioteknologi.com
- Perrett, d. (2010). 200 tahun elektroforesis. Kromatog. Hari ini, 4-7.
- Righetti, ms. G. (2005). Elektroforesis: perarakan wang, perarakan dimes. Jurnal Kromatografi A, 1079 (1-2), 24-40.
- Rilbe, h. (Sembilan-belas sembilan puluh lima). Som reminisciones sejarah elektroforesis. Elektroforesis, 16 (1), 1354-1359.
- Vesterberg, atau. (1993). Sejarah pendek kaedah elektroforetik. Elektroforesis, 14 (1), 1243-1249.
- Vinayagam, m. (Tiada tarikh). Faktor yang mempengaruhi elektroforesis. Akademi.Edu. Diperolehi daripada akademik.Edu

