Elemen kimia
- 3006
- 849
- Horace Gulgowski
Kami menerangkan apa unsur kimia, sifatnya, jenis yang ada, dan kami memberikan beberapa contoh
 Unsur kimia adalah komponen yang tidak dapat dibahagikan dan mempunyai sifat unik selain bahan yang ada
Unsur kimia adalah komponen yang tidak dapat dibahagikan dan mempunyai sifat unik selain bahan yang ada Apa itu elemen kimia?
A elemen kimia Ia boleh ditakrifkan sebagai perkara atau komponen yang tidak dapat dibahagikan dan mempunyai sifat unik selain daripada bahan yang ada. Mengikut ciri -ciri setiap elemen, mereka boleh menjadi lebih kurang dan kurang berharga.
Agar elemen kimia ditakrifkan seperti itu, ia mesti memenuhi ciri -ciri yang tidak dapat dipisahkan. Iaitu, ia tidak boleh dipecah menjadi bahagian yang lebih kecil. Bahagian -bahagian yang tidak dapat dibahagikan lagi adalah apa yang dikenali sebagai atom.
Beberapa elemen kimia dapat berkongsi sebatian yang sama, yang menjadikannya rapat dan hubungan antara ini. Walau bagaimanapun, mereka mempunyai banyak bahagian lain yang tidak berkongsi dengan unsur -unsur lain yang menentukan diri mereka dan juga unik.
Bahan kimia ini boleh berada dalam keadaan pepejal atau gas dan terdapat di tempat dan persekitaran yang berbeza di seluruh planet. Malah kajian saintifik telah menemui jenis bahan dalam unsur -unsur yang luaran ke bumi, seperti asteroid atau planet jauh lain.
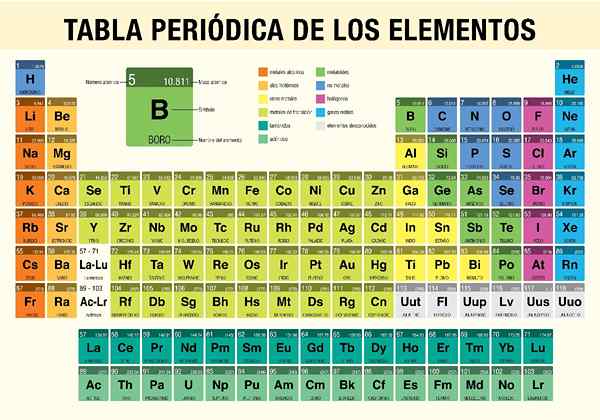
118 elemen kimia kini dikenali dan dianjurkan mengikut bilangan atom dan ciri -ciri mereka dalam apa yang dikenali sebagai jadual berkala.
Jenis elemen kimia
Secara semula jadi, unsur -unsur kimia yang ditakrifkan di atas dapat dijumpai; Walau bagaimanapun, kebanyakannya mungkin murni atau harus menyertai orang lain untuk membentuk bahan kimia baru, dengan itu menimbulkan klasifikasi sebatian ini.
Antara jenis elemen kimia terdapat empat kumpulan besar, yang akan dijelaskan di bawah. Walau bagaimanapun, terdapat subkumpulan lain yang lebih spesifik dari unsur -unsur seperti ini yang juga akan terdedah.
Logam
Mereka adalah komponen yang kebanyakannya berada dalam keadaan pepejal dan kerana sifat mereka adalah konduktor panas dan elektrik yang sangat baik. Di samping itu, mereka adalah unsur -unsur yang mempunyai kecerahan ciri, yang bervariasi keamatannya mengikut setiap subjek.
Boleh melayani anda: Apakah setara mekanikal panas?Bahan yang diklasifikasikan sebagai logam juga dicirikan dengan menjadi sangat mudah diurus dan mulur, dengan itu membolehkan mereka dengan mudah mengubah atau menyertai elemen kimia lain.
Di dalam unsur -unsur logam, terdapat enam subkumpulan yang:
- Actinids
- Lantanids
- Logam peralihan
- Alkali
- Alkaline-Terrreos
- Logam lain.
Tiada logam
Komponen ini kebanyakannya dalam keadaan pepejal; Walaupun demikian mereka berbeza dari logam, kerana mereka tidak panas atau konduktor elektrik yang baik dan tidak mempunyai kecerahan ciri yang terakhir.
Di samping itu, mereka adalah komponen yang tidak mempunyai kemuluran dan pengendalian logam yang mudah, jadi mengubahnya adalah proses yang lebih kompleks.
Metalloid
Dikatakan bahawa komponen ini adalah gabungan antara unsur logam dan bukan logam, berkongsi ciri -ciri kedua -dua kumpulan. Sebahagian daripada ini membenarkan pengaliran elektrik dan haba dan kemuluran mereka mungkin lebih besar atau lebih rendah, bergantung kepada elemen kimia.
Gas mulia
Mereka adalah bahan kimia yang terdapat di alam semula jadi dalam keadaan gas dan komponen dengan ciri -ciri yang sangat istimewa dan berbeza dari elemen gas yang sedia ada.
Unsur -unsur ini dianggap agak stabil dan tidak membuat pengubahsuaian kimia atau reaksi dengan unsur -unsur lain untuk membuat bahan baru.
Sifat berkala
Seperti yang disebutkan di atas, semua elemen kimia yang ada diklasifikasikan sebagai apa yang dikenali sebagai jadual berkala. Jadual ini tidak lebih daripada skim teratur yang ditempatkan oleh kumpulan (menegak) dan tempoh (mendatar) masing -masing subjek kimia mengikut ciri -ciri mereka.
Menjadi jelas mengenai jadual berkala, sifat berkala kemudiannya boleh ditakrifkan. Yang terakhir adalah ciri -ciri atau kekhususan yang menentukan setiap elemen kimia dan seterusnya menubuhkan lokasi mereka dalam jadual berkala.
Boleh melayani anda: karbon amorf: apakah, jenis, sifat, kegunaanTerdapat empat sifat berkala utama:
Elektronegativiti
Harta ini boleh ditakrifkan sebagai kapasiti komponen kimia tertentu untuk menarik atau menghubungkan dengan elemen kimia lain. Dalam erti kata lain, elektronegativiti adalah daya yang atom komponen tertentu mempunyai, untuk menarik atom elemen lain.
Dalam jadual berkala, unsur -unsur yang meningkatkan elektronegativiti terletak dari kiri ke kanan dalam tempoh dan kumpulan menaik.
Radio atom
Harta radio atom tidak lebih daripada rujukan kepada saiz atom yang membentuk setiap elemen kimia. Iaitu, setiap subjek mempunyai bilangan atom tertentu dengan saiz yang berbeza.
Dalam jadual berkala, mereka terletak dari atas ke bawah kerana saiz radius atom meningkat dalam kumpulan dan dalam tempoh berkurangan.
Pertalian atau struktur elektronik
Harta ini boleh ditakrifkan sebagai perubahan tenaga yang diperoleh unsur dalam struktur atomnya dengan mempunyai beberapa perubahan dalam hal yang sama.
Dalam jadual berkala mereka terletak dalam kumpulan yang sama, kerana mereka mempunyai persamaan struktur atom ini.
Potensi pengionan
Ini merujuk kepada tenaga yang diperlukan oleh struktur atom unsur tertentu untuk mengubah statusnya.
Dalam jadual berkala, klasifikasinya diberikan dalam kumpulan dengan menurun dari atas ke bawah dan dalam tempoh yang semakin meningkat dari kiri ke kanan.
Terdapat sifat berkala sekunder lain seperti elektropositiviti, ketumpatan atom, isipadu atom, suhu gabungan dan suhu mendidih.
Boleh melayani anda: kepekatan kimiaContoh elemen kimia
Seperti yang disebutkan, kini terdapat 118 elemen kimia yang dikenal pasti. Unsur -unsur ini mempunyai nama dan simbol yang unik yang mengenal pasti mereka bukan sahaja dalam jadual berkala tetapi juga dalam bidang saintifik kimia.
Seterusnya, 50 elemen ini akan dibentangkan dengan nama dan simbol pengenalan mereka, yang merupakan sebahagian daripada empat jenis elemen yang disebutkan di atas.
- Oksigen (o)
- Fluorida (F)
- Neon (NE)
- Natrium (NA)
- Magnesium (mg)
- Aluminium (AL)
- Silikon (ya)
- Fosforus (P)
- Sulfur (s)
- Klorin (CL)
- Xenón (xe)
- Cesio (CS)
- Barium (BA)
- Lantano (LA)
- Cerio (CE)
- Prasodimio (PR)
- Neodimium (ND)
- Prometio (PM)
- Samario (SM)
- Europio (EU)
- Renio (semula)
- Osmio (OS)
- Ididio (IR)
- Platinum (PT)
- Emas (au)
- Mercury (HG)
- Talio (TL)
- Lead (PB)
- Bismut (bi)
- Polonio (PO)
- Astato (at)
- Radon (RN)
- Francio (FR)
- Radio (RA)
- Actinio (AC)
- Torio (th)
- Protacinium (PA)
- Uranium (u)
- Neptunio (NP)
- Plutonium (PU)
- Dubnium (db)
- Seaborgio (SG)
- Bohrio (BH)
- Hassio (HS)
- Meitnerio (MT)
- Darmstatio (DS)
- RoentGenio (RG)
- Copernicio (CN)
- Flerovio (FL)
- Livermoorio (LV)
Rujukan
- Bola, ms. (2019). Apa itu elemen? Diperolehi dari Kimia Dunia.com
- Jadual Berkala (2018). Diperoleh dari RSC.org
- Jadual Elemen Berkala (2019). Diperolehi dari Pubchem.NCBI.NLM.NIH.Gov
- Jadual berkala unsur -unsur (2018). Diperoleh dari Sigmaaldrich.com
- Apa aremen? (2020). Diperoleh dari BBC.co.UK

