Unit Tenaga Percuma Helmholtz, Bagaimana Ia Dikira, Latihan Diselesaikan

- 3926
- 1272
- Clarence Greenholt DDS
The Helmholtz Tenaga Percuma Ia adalah potensi termodinamik yang mengukur kerja berguna sistem tertutup dalam keadaan suhu dan kelantangan yang tetap. Tenaga bebas Helmholtz dilambangkan sebagai F Dan ia ditakrifkan sebagai perbezaan dari tenaga dalaman Atau kurang produk suhu T Untuk entropi S:
F = u - t ⋅ s
Oleh kerana ia adalah tenaga, ia diukur dalam joules dalam sistem antarabangsa (SI), walaupun unit lain yang sesuai juga boleh menjadi Ergios (CGS), kalori atau voltan elektron (EV).
 Rajah 1. Definisi Tenaga Helmholtz. Sumber: Pixabay.
Rajah 1. Definisi Tenaga Helmholtz. Sumber: Pixabay. Variasi negatif tenaga Helmholtz semasa proses disamakan dengan kerja maksimum yang dapat dilakukan oleh sistem dalam proses isokorik, iaitu, kepada jumlah tetap. Apabila kelantangan tidak malar, sebahagian daripada kerja ini dapat dilakukan di alam sekitar.
Dalam kes ini kita merujuk kepada kerja di mana jumlahnya tidak berbeza, seperti kerja elektrik: dw = φdq, dengan φ sebagai potensi elektrik dan q sebagai caj elektrik.
Sekiranya suhu juga tetap, tenaga Helmholtz diminimumkan apabila baki dicapai. Untuk semua ini, tenaga Helmholtz amat berguna dalam proses volume tetap. Dalam kes ini anda ada:
- Untuk proses spontan: ΔF < 0
- Apabila sistem berada dalam keseimbangan: ΔF = 0
- Dalam proses bukan spontan: ΔF> 0.
[TOC]
Bagaimana tenaga bebas Helmholtz dikira?
Seperti yang dinyatakan pada mulanya, tenaga Helmholtz ditakrifkan sebagai "tenaga dalaman atau sistem, kecuali produk suhu mutlak t, oleh entropi s sistem":
F = u - t ⋅ s
Ia adalah fungsi suhu t dan isipadu v. Langkah -langkah untuk memvisualisasikan ini adalah seperti berikut:
Boleh melayani anda: elektron dalaman- Bermula dari undang -undang termodinamik pertama, tenaga dalaman atau berkaitan dengan entropi sistem dan volumnya V untuk proses yang boleh diterbalikkan melalui hubungan pembezaan berikut:
Du = DQ - DW = TDS - PDV
Ini berikutan tenaga dalaman atau fungsi pembolehubah S dan V, Oleh itu:
U = u (s, v)
- Sekarang definisi F Dan ia diperoleh:
df = du - d (ts) = du - tds - sdt
- Menggantikan di sana ungkapan pembezaan yang diperolehi untuk DU dalam langkah pertama, kekal:
Df = tds - pdv - tds - sdt = -sdt - pdv
- Akhirnya, disimpulkan bahawa F adalah fungsi suhu T dan volum V dan boleh dinyatakan sebagai:
F = f (t, v)
 Rajah 2. Hermann von Helmholtz (1821-1894), ahli fizik dan doktor Jerman, diiktiraf atas sumbangannya kepada elektromagnetisme dan termodinamik, antara bidang sains lain. Sumber: Wikimedia Commons.
Rajah 2. Hermann von Helmholtz (1821-1894), ahli fizik dan doktor Jerman, diiktiraf atas sumbangannya kepada elektromagnetisme dan termodinamik, antara bidang sains lain. Sumber: Wikimedia Commons. Proses spontan
Tenaga Helmholtz boleh digunakan sebagai kriteria umum spontan dalam sistem terpencil, tetapi sebelum beberapa konsep harus ditentukan:
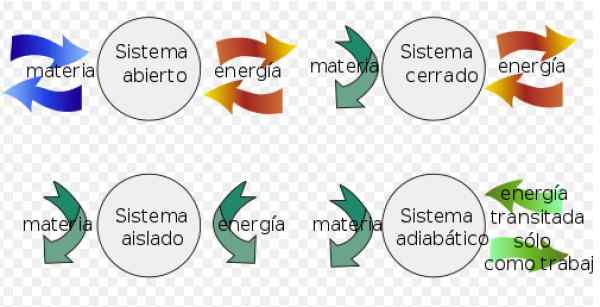
- A Sistem ditutup Ia boleh bertukar tenaga dengan alam sekitar, tetapi tidak dapat menukar perkara.
- Sebaliknya a sistem terpencil tidak menukar bahan atau tenaga dengan persekitaran.
- Akhirnya a sistem terbuka pertukaran bahan dan tenaga dengan persekitaran.
 Rajah 3. Sistem termodinamik. Sumber: Wikimedia Commons. Fjgar (bis) [cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0)].
Rajah 3. Sistem termodinamik. Sumber: Wikimedia Commons. Fjgar (bis) [cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Dalam proses yang boleh diterbalikkan, variasi tenaga dalaman dikira seperti berikut:
Du = TDS - PDV
Sekarang anggap proses volum (isokorik) yang tetap, di mana istilah kedua ungkapan sebelumnya mempunyai sumbangan null. Ia juga harus diingat bahawa mengikut Ketidaksamaan Clausius:
ds ≥ dq/t
Ketidaksamaan seperti itu berlaku untuk sistem termodinamik terpencil.
Supaya untuk proses (boleh diterbalikkan atau tidak) di mana jumlahnya dikekalkan tetap dipenuhi:
Boleh melayani anda: asid fosforik (H3PO4)T ds ≥ du (Pada jumlah tetap)
Dengan mengambil kira bahawa:
df = du - t ds
Kita perlu dalam proses isokorik pada suhu malar dipenuhi bahawa: Df ≤ 0, Seperti yang ditunjukkan pada awal.
Jadi tenaga Helmholtz F adalah jumlah yang menurun dalam proses spontan semasa ia adalah sistem terpencil. F mencapai nilai minimum dan stabil apabila baki boleh diterbalikkan telah dicapai.
Latihan yang diselesaikan
Latihan 1
Kirakan variasi tenaga bebas Helmholtz f untuk 2 tahi lalat gas ideal pada suhu 300k semasa pengembangan isoterma yang membawa kepada sistem jumlah awal 20 liter ke jumlah akhir 40 liter.
Penyelesaian
Bermula dari definisi F:
F = u - t s
Kemudian variasi terhingga F, yang dipanggil ΔF, akan menjadi:
ΔF = ΔU - T ΔS
Seperti kata pernyataan bahawa suhu adalah malar: Δt = 0. Walau bagaimanapun, dalam gas ideal tenaga dalaman hanya bergantung pada suhu mutlaknya, tetapi kerana ia adalah proses isoterma, maka ΔU = 0 dan ΔF = - t ΔS. Untuk gas yang ideal, variasi entropi proses isoterma ditulis seperti ini:
ΔS = n.R.ln (v2/V1)
Memohon ungkapan ini:
ΔS = 2 moles x 8,314 j/(k mol) x ln (40L/20L) = 11.53 J/k
Akhirnya, perubahan tenaga Helmholtz adalah:
ΔF = - t ΔS = - 300k x 11.53 j/k = -3457.70 j.
Latihan 2
Di dalam silinder terdapat omboh yang membahagikannya kepada dua bahagian dan di setiap sisi omboh ada n tahi lalat gas monoatomik yang ideal, seperti yang ditunjukkan dalam gambar di bawah.
Dinding silinder adalah konduktor haba yang baik (diathermic) dan bersentuhan dengan takungan suhu TSama ada.
Jumlah awal setiap bahagian silinder adalah v1i dan v2i, Walaupun jumlah terakhirnya adalah v1f dan v2f Selepas anjakan kuasi. Omboh bergerak dengan cara pelocok yang hermetically melintasi dua silinder.
Ia boleh melayani anda: Tecnecio (TC): Struktur, sifat, kegunaan, memperolehDiminta untuk mencari:
a) perubahan tenaga dalaman gas dan kerja yang dilakukan oleh sistem dan
b) variasi tenaga Helmholtz.
Penyelesaian kepada
Apabila omboh bergerak secara kuasi, daya luaran yang digunakan untuk pelocok mesti mengimbangi daya kerana perbezaan tekanan dalam dua bahagian silinder.
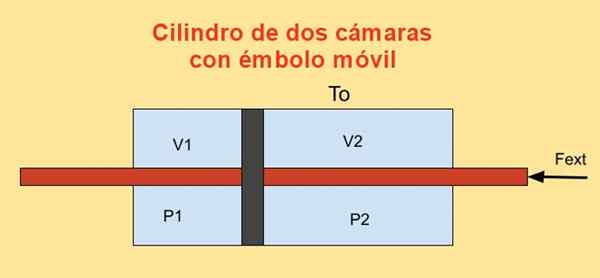 Rajah 4. Variasi tenaga bebas f dalam silinder dengan dua kamera. Sumber: f. Zapata.
Rajah 4. Variasi tenaga bebas f dalam silinder dengan dua kamera. Sumber: f. Zapata. Kerja DW Dibuat oleh daya luaran Fext Semasa anjakan yang sangat kecil Dx adalah:
Dw = - fext Dx = (p1 - P2) Dx = p1 Dv1 + P2 Dv2
Di mana hubungan telah digunakan Dv1 = - dv2 = A dx, menjadi ke Kawasan omboh. Sebaliknya, variasi tenaga Helmholtz adalah:
Df = -sdt - pdv
Oleh kerana semasa proses suhu tidak berubah, maka dt = 0 dan Df = - pdv. Memohon ungkapan ini untuk setiap bahagian silinder yang anda ada:
dw = p1 Dv1 + P2 Dv2 = - df1 - Df2
Menjadi F1 dan F2 Tenaga Helmholtz di setiap kamera.
Kerja terhingga boleh dikira dari variasi terhingga tenaga Helmholtz setiap kamera:
W = -ΔF1 - ΔF2
Penyelesaian b
Untuk mencari perubahan tenaga dari Helmholtz, definisi digunakan: F = u - t s. Seperti dalam setiap kamera, anda mempunyai gas monoatomik yang ideal pada suhu malar TSama ada, Tenaga dalaman tidak berubah (Δu = 0), supaya: ΔF = - tSama ada ΔS. Selain:
ΔS = nr ln (vF/Gergaji)
Itu dengan menggantikannya akhirnya membolehkan kerja yang dilakukan adalah:
W = -tSama ada Nr ln (v1f /V1i) -To nr ln (v2f /V2i) = -ΔF1 -ΔF2
W = - hingga nr ln [(v1f ⋅ v1i)/(V2f .V2i)] = - ΔFJumlah
Menjadi ΔFJumlah Jumlah variasi tenaga Helmholtz.
Rujukan
- Castaños e. Latihan Tenaga Percuma. Pulih dari: lidiaconlachimica.WordPress.com
- Libretxts. Helmholtz Energy. Pulih dari: chem.Libretxts.org
- Libretxts. Apa itu Tenaga Percuma. Pulih dari: chem.Libretxts.org
- Wikipedia. Helmholtz Energy. Pulih dari: Adakah.Wikipedia.com
- Wikipedia. Helmholtz Tenaga Percuma. Diperoleh dari: dalam.Wikipedia.com

