Inersia kimia

- 4213
- 857
- Horace Gulgowski
Apakah inersia kimia?
Inersia kimia adalah harta yang mempunyai bahan atau bahan untuk menahan kemerosotan yang disebabkan oleh agen luaran. Dalam pengertian ini sifat fizikalnya dan, terutama bahan kimia, tetap tidak berubah. Tidak ada rehat pautan atau pembentukan yang baru.
Sekarang, inersia kimia adalah relatif. Sesetengah bahan atau bahan lebih lengai daripada yang lain, yang disebabkan oleh sifat dan kekuatan interaksi mereka. Seperti yang boleh, pada dasarnya, kontras fenomena perubahan, sangat diperlukan untuk berubah dalam pelbagai produk.
 Mengintip emas. Emas adalah kakisan lebih banyak logam tahan
Mengintip emas. Emas adalah kakisan lebih banyak logam tahan Itulah sebabnya, namun tidak teratur bahawa ia adalah bahan atau bahan, akan selalu ada keadaan di mana ia menjadi reaktif. Sebagai contoh, emas adalah logam paling mulia, dan dianggap tidak aktif. Walau bagaimanapun, ia diserang dan dibubarkan oleh air diraja, penyelesaian yang sangat reaktif.
Mungkin, dan setakat ini, satu -satunya elemen kimia yang telah menunjukkan inersia kimia mutlak adalah neon. Tidak ada sebatian yang diketahui, bahkan tidak berada di bawah keadaan ultrapressure, seperti yang ada di dalam nukleus planet atau bulan.
Ciri -ciri inersia kimia
Kekurangan pengoksidaan
Untuk bahan atau bahan yang tidak aktif, pada dasarnya, ia tidak boleh bertindak balas dengan udara sekitarnya. Ini bermakna ia tidak cenderung membentuk hubungan dengan molekul oksigen atau nitrogen yang mengelilingi permukaannya. Dengan kata lain: jangan mengoksidakan pendedahan udara.
Makanan dan semua bahan organik yang berkenaan cenderung mengoksida. Oleh itu, dikatakan bahawa mereka tidak lengai.
Kekurangan pengoksidaan dalam inersia kimia perlu dikekalkan pada suhu yang lebih tinggi daripada 100 ºC. Semakin tinggi suhu, bahan atau bahan akan mula mengoksida lebih cepat, bertindak balas dengan oksigen atau nitrogen udara untuk membentuk oksida atau nituros, masing -masing.
Rintangan asid atau alkali
Ciri lain yang terdapat dalam inersia kimia adalah rintangan kepada asid atau pangkalan. Ini bermakna bahawa bahan atau bahan lengai harus menahan serangan asid, tanpa kecenderungan untuk merendahkan oleh penerimaan ion H+ atau elektrofil yang sangat kuat; atau serangan pangkalan, tanpa merendahkan kerana ion oh-.
Ia boleh melayani anda: asid percomic (HBRO4): sifat, risiko dan kegunaanSekali lagi, ini adalah relatif, kerana terdapat pelbagai jenis asid dan pangkalan. Sesetengah bahan lengai boleh sangat tahan, katakan, asid sulfurik, tetapi mereka terdegrad. Begitulah kes botol kaca ketika mereka bertindak balas dengan HF.
Kestabilan elektronik
Ciri -ciri di atas mempunyai kaitan dengan kestabilan termodinamik yang diperolehi daripada sifat interaksi intermolecular, sebagai tambahan kepada faktor lain. Sebaliknya, inersia kimia juga dilihat dalam ciri -ciri elektronik atom yang sama.
Semakin stabil konfigurasi elektronik atom, semakin rendah kecenderungannya untuk menang atau kehilangan elektron. Oleh itu, ia akan menunjukkan inersia kimia yang lebih besar. Ini adalah kes gas mulia, yang akan dilihat di bahagian seterusnya.
Bioinactivity
Dalam bidang perubatan, bahan atau bahan tidak aktif jika tidak mempunyai bioaktiviti. Iaitu, ia boleh ditempatkan di dalam organisma tanpa diasimilasikan semasa metabolismenya. Ciri ini sangat diinginkan dalam prostesis tulang, atau dalam pembinaan semula tisu.
Rintangan radiasi
Akhirnya, bahan atau bahan lengai juga harus tahan terhadap radiasi, menjadi ultraviolet atau nuklear.
Contoh inersia kimia
Kaca
 Kaca adalah bahan yang agak tidak aktif
Kaca adalah bahan yang agak tidak aktif Antara contoh bahan yang mempamerkan inersia kimia kita mempunyai kaca. Sekiranya mereka tidak lengai, mereka tidak akan berkhidmat untuk penjelasan bekas atau bekas, kerana mereka akan bertindak balas dengan kandungan mereka. Bergantung pada komposisi mereka, seperti borosilicates, mereka boleh menjadi sangat tahan terhadap kakisan dan suhu.
Walau bagaimanapun, seperti yang disebutkan pada mulanya, kaca tidak kebal terhadap semua bahan: ia bertindak balas dengan HF, bahkan dicairkan, alkali panas, seperti NaOH, dan H3PO4 Sangat pekat dan panas.
Boleh melayani anda: pirolisisPlastik
 Sekiranya kuali Teflon tidak lengai, ia akan merosakkan semua makanan yang kami masak di dalamnya. Sumber: Mdevicente, CC0, melalui Wikimedia Commons
Sekiranya kuali Teflon tidak lengai, ia akan merosakkan semua makanan yang kami masak di dalamnya. Sumber: Mdevicente, CC0, melalui Wikimedia Commons Plastik juga memenuhi fungsi yang serupa dengan kaca, tetapi terdapat lebih banyak serba boleh (mereka tidak mudah pecah). Beberapa plastik, seperti Teflon (polytetrafluoroethylene), kynar (polyvinylidene fluoride), dan telene (polydiccyclopentadiene), sangat tahan terhadap serangan asid dan kakisan.
Seramik
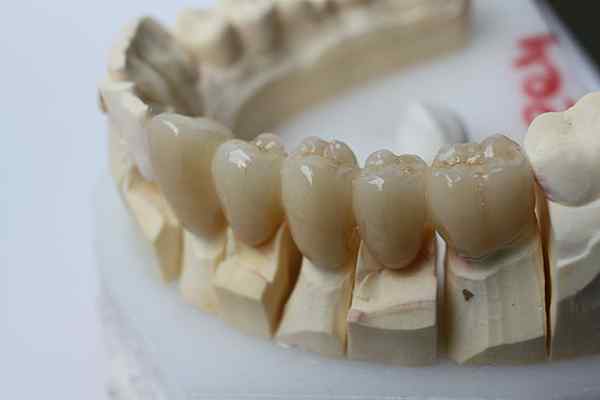 Inersia kimia zirkonia membolehkannya digunakan untuk prostesis gigi. Sumber: Bin Im Garten melalui Wikipedia.
Inersia kimia zirkonia membolehkannya digunakan untuk prostesis gigi. Sumber: Bin Im Garten melalui Wikipedia. Seramik lengai melangkah lebih jauh daripada plastik. Mereka bertujuan untuk aplikasi di mana suhu tinggi mendominasi, agak biasa dalam industri automotif dan aeroangkasa; atau dalam sistem biokimia, seperti dalam industri farmaseutikal dan dalam pelaksanaan prostesis tulang.
Antara beberapa seramik ini dengan inersia kimia yang hebat kita ada: alumina (ke2Sama ada3, Hadir di corindon dan nilam), silikat (kaca khusus), silikon karbida (sic, keras dan tenacious), dan zirkonia (zio2).
Gas inert
Meninggalkan bahan lengai, kini kami mempunyai bahan lengai. Gas inert tidak begitu reaktif, jadi kehadiran mereka di udara tidak menyiratkan risiko tindak balas dalam keadaan normal.
Antara gas ini kita mempunyai CO2, Co dan n2. Nitrogen adalah yang paling tidak aktif dari semua gas ini; Namun, dia dapat bertindak balas panas dengan beberapa logam untuk membentuk nituros, m3Nn, menjadi n Keadaan pengoksidaan valencia atau logam.
Co2 Ia agak tidak aktif; Kecuali apabila ia memenuhi penyelesaian alkali, di mana ia diubah menjadi karbonat, atau di hadapan enzim arang batu.
Bagi pihaknya, CO tetap tidak aktif pada suhu bilik; Tetapi pada suhu tinggi ia bertindak balas dengan arang batu, wap air, oksida logam, olefin, antara sebatian lain.
Boleh melayani anda: keseimbangan kimia: penjelasan, faktor, jenis, contohReaksi tersebut dapat diteruskan dengan kehadiran pemangkin logam. Begitu juga, Co, walaupun tanpa melanggar ikatan kovalennya, dapat menyelaraskan atom logam neutral.
Logam mulia
Logam mulia adalah yang paling tahan terhadap kakisan dan serangan asid dan alkali. Masing -masing, pada suhu tinggi, atau dalam format habuk, akan bertindak balas dengan oksigen atau fluorida. Oleh itu, inersia kimia unsur -unsur ini agak relatif.
Antara logam mulia yang kita ada: Emas (AU), Ruthenio (RU), Platinum (PT), Paladio (PD), Osmio (OS) dan Iridido (IR). Daripada mereka semua, emas adalah yang paling mulia, walaupun dalam keadaan logam di kerak bumi.
Gas mulia
Dan akhirnya, di kerusi tertinggi inersia kimia, kita mempunyai gas mulia: helium (dia), neon (ne), argon (ar), crypton (kr), xenon (xe) dan radon (rn). Semuanya sangat tidak aktif. Walau bagaimanapun, banyak sebatian xenon telah disintesis, termasuk garam yang dikenali sebagai perxenatos, dengan anion xeo64-.
 Lampu neon sesuai dengan unsur -unsur kimia yang paling tidak aktif
Lampu neon sesuai dengan unsur -unsur kimia yang paling tidak aktif Inersia kimianya adalah kerana atom mereka mengandungi tenaga dan lapisan orbit mereka yang penuh dengan elektron. Dari argon, ada kemungkinan bahawa di bawah ultrapressions mereka akan mengakses elektron menggunakan lapisan orbital kosong atau lebih banyak (3D dan 4s, sebagai contoh); perkara yang mustahil untuk helium atau neon.
Gas mulia tepat helium dan neon adalah yang paling tidak aktif. Helium dapat membentuk sebatian dengan natrium hingga tekanan yang sangat tinggi (Hena).
Sementara itu, tidak ada sebatian yang diketahui sama sekali, lebih lengai daripada Helium sendiri kerana beban nuklearnya yang lebih berkesan, yang sangat menangkis mana -mana atom yang cuba mendekati atom neon.
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Shiver & Atkins. (2008). Kimia InorgánICA. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2020). Kimia tidak aktif. Diperoleh dari: dalam.Wikipedia.org
- Dr. Doug Stewart. (2020). Definisi lengai. Pulih dari: chemicool.com
- Elsevier b.V. (2020). Kekurangan kimia. Scientedirect. Diperoleh dari: Scientedirect.com
- Clara Moskowitz. (20 Mac, 2018). Kejutan Gas Mulia: Helium boleh membentuk sebatian pelik. Pulih dari: Scientific American.com
- Coorstek. (2020). Sifat Kimia Seramik Teknikal. Pulih dari: Coorstek.com
- Osborne Industries. (2020). 3 plastik tahan asid yang paling banyak. Pulih dari: Osborneindustries.com

