Meniskus (Kimia)
- 4366
- 1332
- Miss Elmer Hagenes
 Meniskus Convex dan Cembung. Sumber: Wikimedia Commons
Meniskus Convex dan Cembung. Sumber: Wikimedia Commons Apakah Meniskus (Kimia)?
Dia Meniskus Ia adalah kelengkungan permukaan cecair. Ia juga merupakan permukaan bebas cecair di antara muka udara cecair. Cecair dicirikan dengan mempunyai jumlah tetap, yang tidak kompresi.
Walau bagaimanapun, bentuk cecair berbeza -beza mengamalkan bentuk bekas yang mengandunginya. Ciri ini disebabkan oleh pergerakan rawak molekul yang membentuknya.
Cecair mempunyai keupayaan untuk mengalir, ketumpatan tinggi dan tersebar dengan cepat dalam cecair lain yang mana.
Mereka menduduki kawasan terendah dalam bekas, meninggalkan permukaan bebas yang tidak rata di bahagian atas. Dalam beberapa keadaan mereka boleh mengamalkan bentuk khas seperti titisan, gelembung dan gelembung.
Sifat -sifat cecair seperti titik lebur, tekanan wap, kelikatan dan haba pengewapan bergantung kepada intensiti daya intermolecular yang memberikan perpaduan kepada cecair.
Walau bagaimanapun, cecair juga berinteraksi dengan bekas melalui daya lekatan.
Meniskus kemudian timbul dari fenomena fizikal ini: perbezaan antara daya perpaduan antara zarah cecair, dan lekatan, yang membolehkan mereka membasahi dinding.
Apa itu meniskus?
Seperti yang dijelaskan, meniskus adalah hasil daripada beberapa fenomena fizikal, di antaranya ketegangan permukaan cecair juga boleh disebutkan.
Pasukan perpaduan
Daya perpaduan adalah istilah fizikal yang menerangkan interaksi intermolecular dalam cecair. Dalam kes air, daya perpaduan adalah disebabkan oleh interaksi dipole-dipolo dan jambatan hidrogen.
Boleh melayani anda: klorin oksida (iii): sifat, struktur, kegunaanMolekul air adalah sifat bipolar. Ini kerana oksigen molekul adalah elektronegatif kerana ia mempunyai kekerasan yang lebih besar disebabkan oleh elektron daripada hidrogen, yang menentukan bahawa oksigen kekal dengan beban negatif dan hidrogen dicas secara positif.
Terdapat tarikan elektrostatik antara beban negatif molekul air, yang terletak di oksigen, dan beban positif molekul air lain, yang terletak di hidrogen.
Interaksi ini adalah apa yang dia tahu sebagai interaksi atau daya dipole-dipole, yang menyumbang kepada perpaduan bendalir.
Kuasa melekat
Sebaliknya, molekul air dapat berinteraksi dengan dinding kaca, dengan beban separa atom hidrogen molekul air yang mengikat atom oksigen permukaan kaca kaca dalam atom oksigen.
Ini merupakan daya lekatan antara cecair dan dinding tegar, yang secara colloqually bermaksud bahawa cecair itu memancarkan dinding.
Apabila larutan silikon diletakkan di permukaan kaca, air tidak sepenuhnya membuang kaca, tetapi terbentuk pada beberapa titisan yang mudah dihapuskan.
Oleh itu, ditunjukkan bahawa dengan rawatan ini daya lekatan antara air dan kaca dikurangkan.
Kes yang sangat serupa berlaku apabila tangan berminyak, dan ketika mencuci mereka dengan air, titisan yang sangat jelas dapat dilihat pada kulit dan bukannya kulit yang dibasahi.
Jenis meniscs
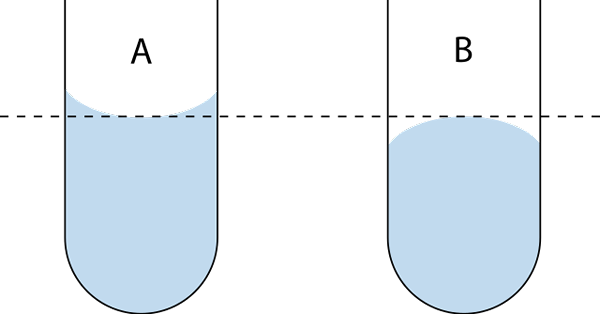
Terdapat dua jenis meniskus: cekung dan cembung. Dalam imej yang unggul, cekung adalah A dan cembung b. Garis putus -putus menunjukkan siram yang betul ketika membaca ukuran kelantangan.
Boleh melayani anda: atom neutralMeniscus Concave
 Langkah Meniskus Concave. Sumber: Wikimedia Commons
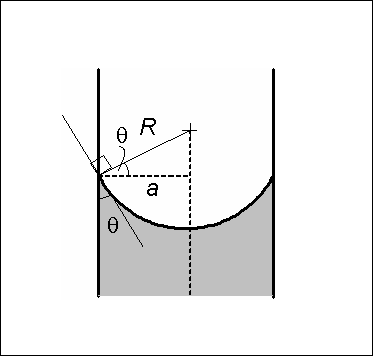
Langkah Meniskus Concave. Sumber: Wikimedia Commons Meniscus cekung dicirikan di mana sudut sentuhan θ yang membentuk dinding kaca dengan garis tangen ke meniskus, yang diperkenalkan ke dalam pangkuan cecair, mempunyai nilai kurang dari 90º.
Sekiranya jumlah cecair diletakkan di atas kaca, ia cenderung menyebar di permukaan kaca.
Kehadiran menisc cekung.
Oleh itu, mandi cecair atau memasak dinding kaca, mengekalkan jumlah cecair dan memberikan tiscus concave. Air adalah contoh cecair yang membentuk meniskus cekung.
Convex Meniscus
Dalam kes meniskus cembung, sudut sentuhan θ mempunyai nilai lebih besar daripada 90º. Mercury adalah contoh cecair yang membentuk meniskus cembung. Apabila setitik merkuri diletakkan di permukaan kaca, sudut sentuh θ mempunyai nilai 140º.
Pemerhatian menisc cembung. Dikatakan bahawa cecair tidak membasuh kaca.
Kekuatan perpaduan (cecair-cecair) dan lekatan (cecair-padat) bertanggungjawab untuk banyak fenomena kepentingan biologi, seperti kes ketegangan permukaan dan kapilariti.
Ketegangan permukaan
Ketegangan permukaan adalah daya tarikan bersih yang dikenakan ke atas molekul bendalir yang terdapat di permukaan dan yang cenderung memperkenalkannya ke dalam cecair.
Boleh melayani anda: elemen diatomikOleh itu, ketegangan permukaan cenderung cohes cecair dan memberi lebih banyak meniskus cekung. Dengan kata lain, daya ini cenderung untuk menghilangkan permukaan cecair dinding kaca.
Ketegangan permukaan cenderung menurun apabila suhu meningkat, contohnya: ketegangan air permukaan adalah sama dengan 0.076 N/m A 0 ° C dan 0.059 N/m A 100 ° C.
Walaupun ketegangan permukaan merkuri pada 20 ° C ialah 0.465 n/m. Ini akan menjelaskan mengapa merkuri membentuk meniscus cembung.
Capillarity
Sekiranya sudut kenalan θ kurang daripada 90º, dan cecair itu mengalir dinding kaca, cecair di dalam kapilari kaca dapat naik sehingga mencapai keadaan keseimbangan.
Berat lajur cecair dikompensasi oleh komponen menegak daya perpaduan akibat ketegangan permukaan. Daya lekatan tidak campur tangan kerana ia berserenjang dengan permukaan tiub.
Undang -undang ini tidak menjelaskan bagaimana air dapat naik dari akar ke daun melalui kapal xylem.
Sebenarnya, terdapat faktor -faktor lain yang terlibat dalam hal ini, contohnya: Apabila air menguap di daun, ia membolehkan molekul air disedut di bahagian atas kapilari.
Ini membolehkan molekul lain di bahagian bawah kapilari untuk naik untuk menduduki tapak molekul air yang disejat.
Rujukan
- Whitten, Davis, Peck & Stanley. Kimia. Pembelajaran Cengage.
- Helmestine, Anne Marie, Ph.D. Cara Membaca Meniscus dalam Kimia. Pulih dari pemikiran.com

