Logam alkalineter
- 4205
- 993
- Miss Elmer Hagenes
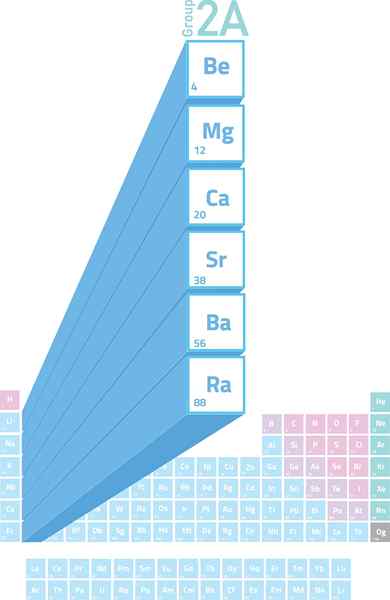
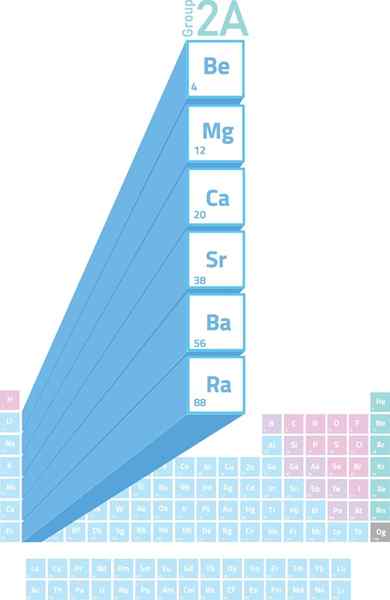 Lokasi logam alkali dalam jadual berkala
Lokasi logam alkali dalam jadual berkala Apakah logam alkali?
The Logam alkalineter Mereka adalah unsur -unsur kumpulan 2 (dahulunya dipanggil kumpulan 2a) dari jadual berkala. Maksudnya, mereka dibentuk oleh 6 elemen lajur kedua jadual berkala dari berilium (BE) ke radio (RA).
Mereka adalah sekumpulan unsur logam yang agak reaktif dan agak biasa. Mereka hanya mempunyai dua elektron valensi yang terletak di orbital s. Atas sebab ini, mereka tergolong dalam blok s dari jadual berkala.
Nama "alkalinoterreo" berasal dari kesatuan kata -kata "alkali", yang merupakan cara lain untuk mengatakan asas, dan bumi, iaitu bagaimana mereka diberitahu sebelum oksida. Oleh itu logam alkalinoterrous secara harfiah bermaksud logam yang membentuk oksida asas.
Logam ini mempunyai banyak aplikasi yang menjadikannya penting dalam masyarakat kita sekarang, terutama magnesium. Aplikasi ini disebabkan oleh sifat tertentu mereka, yang diterangkan di bawah.
Sifat logam alkalinoterapi
Mereka mempunyai penampilan logam
Semua logam alkali mempunyai warna perak dengan kecerahan logam. Radon juga radioaktif sehingga bersinar dalam gelap memancarkan cahaya hijau ciri.
Mereka adalah logam padat sedikit
Semua logam alkalinoterrous lebih padat daripada air, tetapi kurang padat daripada kebanyakan elemen logam lain dalam jadual berkala.
Ketumpatan dalam kumpulan ini berkisar dari 1.54 g/cm3 Untuk kalsium sehingga 5.5 g/cm3 Untuk radio, yang jauh lebih rendah daripada kepadatan logam lain seperti besi (7.9 g/cm3), tembaga (9.0 g/cm3), plumbum (11.3 g/cm3) dan El Mercurio (13.5 g/cm3), untuk menamakan beberapa.
Mereka mempunyai titik lebur dan mendidih yang agak rendah
Menjadi logam, titik lebur dan mendidihnya lebih besar daripada yang paling bukan logam. Walau bagaimanapun, mereka lebih rendah daripada titik gabungan dan mendidih kebanyakan logam lain, dengan beberapa pengecualian.
Boleh melayani anda: persamaan ArrheniusMereka mempunyai valencia +2
Oleh kerana konfigurasi elektronik mereka, logam ini cenderung kehilangan dua elektron apabila mereka bertindak balas dengan unsur -unsur lain seperti bukan logam. Atas sebab ini, satu -satunya Valencia adalah +2.
Mereka agak reaktif
Logam alkalinoterrous jauh lebih reaktif daripada logam seperti besi atau tembaga, tetapi kurang reaktif daripada logam alkali (unsur -unsur kumpulan 1). Semakin rendah kumpulan, semakin reaktif logam.
Sebagai contoh, berilium (kumpulan pertama) tidak bertindak balas dengan air manakala dua berikut boleh bertindak balas dengan air panas dan yang terakhir juga boleh bertindak balas dengan air sejuk.
Bertindak balas dengan udara untuk membentuk oksida asas
Logam ini cenderung membentuk oksida asas apabila mereka bertindak balas dengan oksigen udara. Malah, inilah sebabnya mereka dipanggil alkaliners. Oksida ini, apabila larut dalam air, menjadi hidroksida yang menghasilkan penyelesaian alkali atau asas.
Aplikasi logam alkalinotherrous
Dalam industri teknologi
Sebilangan logam alkalinoterrous digunakan dalam pembuatan semikonduktor. Ini penting dalam pembinaan litar elektronik seperti yang mengandungi hampir semua peralatan elektrik moden, dari komputer dan telefon bimbit, mesin basuh, kereta dan lain -lain.
Dalam industri makanan
Kalsium adalah nutrien penting untuk hidup. Ia adalah sebahagian daripada struktur tulang dan mempunyai fungsi penting lain dalam badan. Atas sebab ini, elemen ini ditambah sebagai pemula kepada banyak makanan dari bijirin ke produk tenusu. Di samping itu, ia juga digunakan dalam pembuatan keju.
Ia boleh melayani anda: Circonium: Sejarah, Hartanah, Struktur, Risiko, KegunaanDalam industri kereta
Sebilangan logam alkali mempunyai sifat mekanikal yang sangat baik, yang bermaksud bahawa mereka sukar dan tahan. Di samping itu, mereka tahan kakisan, jadi mereka sering digunakan dalam pembuatan roda mewah untuk kereta serta bahagian lain dari mereka.
Dalam industri ketenteraan
Oleh kerana sifat mekanikal mereka dan ketumpatan rendah, logam seperti magnesium dan berilium digunakan dalam pembinaan pesawat tempur, satelit dan helikopter.
Di samping itu, disebabkan sifat elektrik mereka, mereka juga digunakan dalam pembuatan pelbagai jenis sensor dan sistem optik dan elektronik yang digunakan oleh industri ketenteraan untuk mewujudkan sistem senjata dan komunikasi.
Enam logam alkali
Hanya ada enam logam alkali. Seterusnya, terdapat penerangan ringkas mengenai masing -masing:
Beryllium (BE)
Ia adalah nombor elemen 4 dari jadual berkala dan yang pertama dari kumpulan logam alkalinother. Ia adalah logam yang sangat ringan dan kuat dengan sifat unik yang menjadikannya berguna dalam pembuatan semikonduktor.
Magnesium (mg)
Magnesium adalah logam perak yang agak ringan, dengan titik lebur dan mendidih yang rendah (berbanding logam lain). Ia sangat keras dan tahan dan sering digunakan dalam pembuatan bahagian kereta dan sebagai bahan tambahan dalam penyediaan aloi seperti jenis keluli tertentu.
Ia adalah logam alkali dan nombor unsur kedua 12 dari jadual berkala. Seperti elemen lain dalam kumpulan ini, ia adalah nutrien penting untuk hidup.
Kalsium (CA)
Kalsium adalah elemen paling banyak ke -5 dalam korteks bumi. Ia didapati sebagai kalsium karbonat di banyak mineral dan batu dan juga merupakan elemen penting untuk kehidupan kerana penyertaannya dalam pembentukan tulang dan kepentingannya dalam sistem saraf.
Boleh melayani anda: Strontium Chloride (SRCL2)Logam ini adalah nombor unsur 20 dari jadual berkala, berada dalam tempoh keempat dan merupakan logam alkali ketiga.
Strontium (SR)
Elemen nombor 38 dan logam alkali keempat adalah strontium. Ia lebih berat daripada kalsium, tetapi nampaknya banyak dari segi sifat kimia dan fizikalnya. Malah, strontium dapat menggantikan kalsium dalam tulang.
Ini amat bermasalah apabila kita mendedahkan diri kita kepada strontium radioaktif yang berlaku selepas tindak balas nuklear, kerana, ketika mematuhi tulang, sangat sukar untuk menghapuskan dari badan dan meracuni kita dengan radiasi sedikit demi sedikit oleh sedikit.
Barium (BA)
Unsur ini mempunyai nombor atom 56 dan juga mempunyai sifat yang hampir sama dengan kalsium dan strontium. Ia adalah logam yang agak lembut dan sangat reaktif yang tidak bersifat unsur. Ia adalah salah satu logam alkali dengan watak logam yang lebih besar.
Radio (RA)
Unsur terakhir kumpulan Alcalinoterreos adalah radio, logam radioaktif (oleh itu namanya) yang memancarkan cahaya hijau yang lemah yang mudah diperhatikan dalam kegelapan.
Dulu banyak digunakan dalam penyediaan lukisan yang bersinar dalam kegelapan, tetapi setelah bahaya kesihatan ditemui, penggunaannya dilarang.

