Rutherford Sejarah Model Atom, Eksperimen, Postulates
- 2760
- 741
- Delbert Dare
Dia Model Atom Rutherford Ini adalah perihalan atom yang dicipta oleh ahli fizik British Ernest Rutherford (1871-1937) ketika pada tahun 1911 ia menemui nukleus atom, terima kasih kepada eksperimen penyebaran terkenal yang dinamakan.
Idea atom ("tidak dapat dipisahkan"Dalam bahasa Yunani) sebagai komponen perkara terkecil, ia adalah ciptaan intelektual yang dilahirkan di Yunani kuno, sekitar 300 hingga.C. Seperti banyak konsep Yunani yang lain, konsep atom dibangunkan berdasarkan logik dan argumentasi, tetapi tidak untuk percubaan.
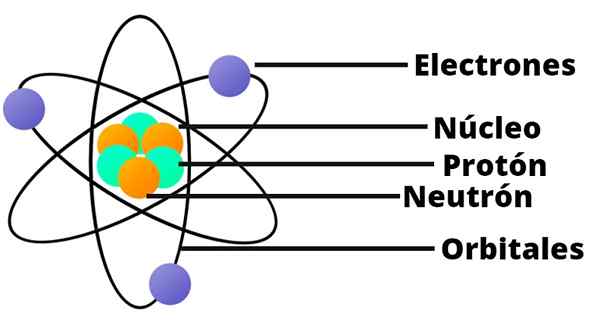 Model Atom Rutherford
Model Atom Rutherford Ahli falsafah atomis yang paling terkenal ialah Demokrit Abdera (460 - 360 SM), Epicurus Samos (341 - 270 ac) dan Tito Lucrecio (98 - 54 ac). Orang -orang Yunani mengandung empat jenis atom yang sesuai dengan empat elemen yang menurut mereka membentuk perkara itu: udara, air, bumi dan api.
Selanjutnya Aristotle akan menambah elemen kelima: eter yang membentuk bintang -bintang, kerana empat elemen yang lain adalah murni daratan.
Penaklukan Alexander the Great, yang mana Aristotle adalah seorang guru, mengembangkan kepercayaannya untuk dunia kuno, dari Sepanyol ke India dan dengan itu, selama berabad -abad, idea atom Dia mencipta tempatnya sendiri di dunia sains.
[TOC]
Atom tidak dapat dipisahkan
Idea ahli falsafah Yunani mengenai struktur subjek dikekalkan selama beratus-ratus tahun, sehingga seorang ahli kimia dan guru Inggeris bernama John Dalton (1776-1844) menerbitkan hasil eksperimennya pada tahun 1808.
Dalton bersetuju bahawa unsur -unsur terdiri daripada zarah yang sangat kecil, yang dipanggil atom. Tetapi ia lebih jauh dengan menyatakan bahawa semua atom elemen yang sama adalah sama, mereka adalah saiz yang sama, jisim yang sama dan sifat kimia yang sama, yang menjadikan mereka tetap tidak berubah semasa reaksi kimia.
Ini adalah model atom pertama dengan asas saintifik. Seperti orang Yunani, Dalton terus mempertimbangkan atom sebagai tidak dapat dipisahkan, oleh itu, kekurangan struktur. Walau bagaimanapun, jenius Dalton memimpinnya untuk memerhatikan salah satu prinsip pemeliharaan fizik:
- Dalam tindak balas kimia, atom tidak dicipta atau dimusnahkan, Mereka hanya menukar pengedaran mereka.
Dan menubuhkan cara di mana sebatian kimia dibentuk oleh "atom kompaun" (molekul):
- Apabila dua atau lebih atom unsur yang berbeza digabungkan untuk membentuk sebatian yang sama, mereka selalu melakukannya dalam perkadaran besar -besaran ditakrifkan dan malar.
Abad kesembilan belas adalah abad yang besar dari elektrik dan magnet. Beberapa tahun selepas penerbitan Dalton, hasil beberapa eksperimen menanam keraguan di kalangan saintis mengenai ketidakpatuhan atom.
Boleh melayani anda: Apakah reaksi kapasitif dan bagaimana mengiranya?Tiub Crookes
The Crookes Tube adalah peranti yang direka oleh ahli kimia British dan ahli meteorologi William Crookes (1832-1919). Eksperimen yang dicabut pada tahun 1875, terdiri daripada meletakkan, di dalam tiub yang penuh dengan gas pada tekanan rendah, dua elektrod, yang dipanggil Katod dan yang lain dipanggil anod.
Dengan mewujudkan perbezaan yang berpotensi antara kedua -dua elektrod, gas bersinar dengan warna yang ciri gas yang digunakan. Fakta ini mencadangkan bahawa terdapat organisasi tertentu di dalam atom dan oleh itu, ia tidak dapat dipisahkan.
Di samping itu, radiasi ini menghasilkan pendarfluor yang lemah di dinding tiub kaca di hadapan katod, memotong bayang -bayang tanda silang yang terletak di dalam tiub.
Ia adalah radiasi misteri yang dikenali sebagai "Cathode Rays", yang bergerak dalam garis lurus ke anod dan yang sangat bertenaga, mampu menghasilkan kesan mekanikal, dan yang menyimpang ke arah plat yang dimuatkan secara positif atau juga dengan magnet.
Penemuan elektron
Sinaran di dalam tiub Crookes tidak dapat dirawat, kerana ia mempunyai beban negatif. Joseph John Thomson (1856 - 1940) mendapati jawapannya pada tahun 1887 apabila dia mendapati hubungan antara beban dan jisim radiasi ini, dan mendapati bahawa ia selalu sama: 1.76 x 10sebelas C/kg., Tidak kira gas terkunci di dalam tiub atau bahan yang digunakan untuk mengeluarkan katod.
Thomson memanggil zarah -zarah ini Corpuscles. Dengan mengukur jisimnya berhubung dengan caj elektriknya, menyimpulkan bahawa setiap corpuscle jauh lebih kecil daripada atom. Oleh itu, beliau mencadangkan agar mereka menjadi sebahagian daripada mereka, dengan itu menemui elektron.
Saintis British adalah yang pertama menggariskan model grafik atom, melalui lukisan sfera dengan titik yang dimasukkan, yang dengan bentuknya diberikan sebutan "Buddin of Ciruela". Tetapi penemuan ini membawa soalan lain:
- Sekiranya perkara itu neutral, dan elektron mempunyai beban negatif: di mana bahagian atom adalah beban positif yang meneutralkan elektron?
- Sekiranya jisim elektron lebih rendah daripada atom, maka apakah atom yang lain terdiri daripada?
- Mengapa zarah -zarah yang diperoleh selalu elektron dan tidak pernah dari jenis lain?
Eksperimen Penyebaran Rutherford: Nukleus dan Proton Atom
Menjelang 1898 Rutherford telah mengenal pasti dua jenis radiasi dari uranium, yang dipanggilnya Alpha dan beta.
Radioaktiviti semulajadi telah ditemui oleh Marie Curie pada tahun 1896. Zarah alfa mempunyai beban positif dan hanya nukleus helium, tetapi pada masa itu konsep teras belum diketahui. Rutherford akan menemuinya.
Boleh melayani anda: Sistem termodinamik: sifat, jenis, contohSalah satu eksperimen yang dibuat oleh Rutherford pada tahun 1911 di Manchester University, dengan bantuan Hans Geiger, terdiri daripada membombardir lembaran emas halus dengan zarah Alpha, beban yang positif. Sekitar lembaran emas meletakkan skrin pendarfluor yang membolehkan mereka memvisualisasikan kesan pengeboman.
Pemerhatian
Mempelajari kesan pada skrin pendarfluor, Rutherford dan pembantunya mengamati bahawa:
- Peratusan zarah alfa yang tinggi menyeberangi lembaran tanpa sisihan yang ketara.
- Ada yang menyimpang pada sudut yang agak jelas
- Dan sangat sedikit melantun ke belakang
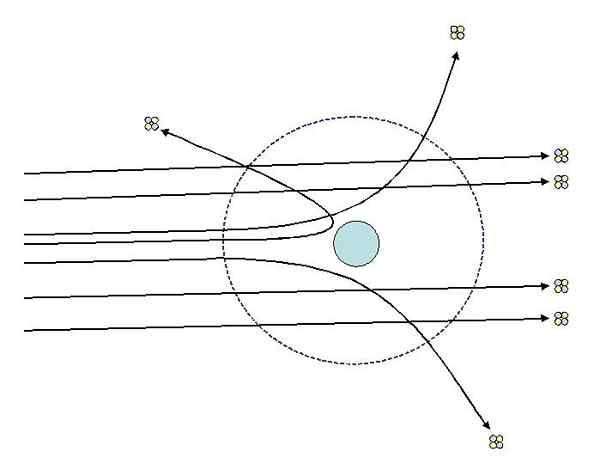 Eksperimen Penyebaran Rutherford. Sumber: [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]].
Eksperimen Penyebaran Rutherford. Sumber: [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]]. Pemerhatian 2 dan 3 mengejutkan penyiasat dan membawa mereka untuk mengandaikan bahawa orang yang bertanggungjawab terhadap sinar yang tersebar harus mempunyai caj positif dan berdasarkan pemerhatian nombor 1, orang yang bertanggungjawab mempunyai saiz yang jauh lebih kecil daripada zarah alfa.
Rutherford sendiri berkata dalam hal ini bahawa ia adalah "... seolah -olah anda mencuba projektil tentera laut 15 inci terhadap sekeping kertas dan peluru itu melantun kembali dan memukul anda". Ini pasti dapat dijelaskan oleh model Thompson.
Menganalisis hasilnya dari sudut pandang klasik, Rutherford telah menemui kewujudan nukleus atom, di mana beban positif atom yang memberikan berkecuali ini tertumpu.
Rutherford meneruskan eksperimen penyebarannya. Menjelang tahun 1918 sasaran baru zarah alfa adalah atom nitrogen gas.
Dengan cara ini ia mengesan nukleus hidrogen dan segera tahu bahawa satu -satunya tapak dari mana nukleus ini boleh datang dari nitrogen itu sendiri. Bagaimana mungkin nukleus hidrogen adalah sebahagian daripada nitrogen?
Rutherford kemudian mencadangkan bahawa teras hidrogen, elemen yang telah diberikan nombor atom 1, harus menjadi zarah asas. Saya memanggilnya proton, Perkataan Yunani untuk ditetapkan Pertama. Oleh itu, penemuan nukleus atom dan proton adalah disebabkan oleh neozyre yang cemerlang ini.
Model atom Rutherford
Model baru sangat berbeza dari Thompson. Ini adalah postulatnya:
- Atom mengandungi teras yang dimuatkan secara positif, yang walaupun sangat kecil, mengandungi hampir seluruh jisim atom.
- Elektron mengorbit nukleus atom pada jarak yang jauh dan dalam orbit bulat atau elips.
- Beban bersih atom tidak sah, kerana caj elektron mengimbangi beban positif yang ada di dalam nukleus.
Pengiraan Rutherford menunjuk nukleus sfera dan radio sekecil 10-lima belas m, sebagai nilai jejari atom kira -kira 100.000 kali lebih tinggi, kerana nukleus agak jauh dari satu sama lain: dari urutan 10-10 m.
 Ernest Rutherford muda. Sumber: Tidak Diketahui, Diterbitkan pada tahun 1939 di Rutherford: Menjadi Kehidupan dan Surat RT. Hon. Lord Rutherford, atau. M [cc oleh 4.0 (https: // creativeCommons.Org/lesen/by/4.0)]
Ernest Rutherford muda. Sumber: Tidak Diketahui, Diterbitkan pada tahun 1939 di Rutherford: Menjadi Kehidupan dan Surat RT. Hon. Lord Rutherford, atau. M [cc oleh 4.0 (https: // creativeCommons.Org/lesen/by/4.0)] Ini menjelaskan mengapa kebanyakan zarah alfa menyeberangi lembaran tanpa kesulitan atau tidak mengalami pesongan yang sangat kecil.
Dilihat pada objek sehari -hari, atom Rutherford akan terdiri daripada teras saiz besbol, manakala jejari atom akan kira -kira 8 km. Oleh itu atom boleh dianggap hampir semuanya sebagai ruang kosong.
Terima kasih kepada persamaannya dengan sistem solar kecil, ia dikenali sebagai "model planet atom". Daya tarikan elektrostatik antara nukleus dan elektron akan sama dengan tarikan graviti antara matahari dan planet.
Batasan
Walau bagaimanapun, terdapat perselisihan tertentu mengenai beberapa fakta yang diperhatikan:
- Jika idea bahawa elektron mengorbit di sekitar nukleus diterima, ia berlaku bahawa elektron harus terus memancarkan radiasi sehingga ia bertembung dengan nukleus, dengan pemusnahan atom yang akibatnya kurang dari satu saat. Ini, mujurlah ia bukan apa yang sebenarnya berlaku.
- Di samping itu, pada masa -masa tertentu atom memancarkan frekuensi tertentu radiasi elektromagnet apabila terdapat peralihan antara keadaan tenaga yang lebih besar kepada satu dengan kurang tenaga, dan hanya frekuensi itu, bukan yang lain. Bagaimana menjelaskan hakikat bahawa tenaga dikira?
Walaupun terdapat batasan -batasan ini dan hari ini terdapat model yang lebih canggih dan menurut fakta yang diperhatikan, model atom Rutherford masih berguna untuk pelajar mempunyai pendekatan pertama yang berjaya atom dan zarah konstituennya.
Dalam model atom ini, neutron tidak muncul, satu lagi penyusun nukleus, yang tidak ditemui sehingga tahun 1932.
Tidak lama selepas Rutherford mencadangkan model planetnya, pada tahun 1913 ahli fizik Denmark Niels Bohr akan mengubahnya untuk menjelaskan mengapa atom tidak dimusnahkan dan kami masih di sini untuk menceritakan kisah ini.
Artikel yang menarik
Model atom Schrödinger.
Model Broglie Atom.
Model Atom Chadwick.
Model Atom Heisenberg.
Model atom Perrin.
Model Thomson Atom.
Model Atom Dirac Jordan.
Model Atom Democritus.
Model Atom Bohr.
Model Atom Dalton.
Rujukan
- Rex, a. 2011. Asas Fizik. Pearson. 618-621.
- Zapata, f. 2007. Nota Kelas untuk Kerusi Perlindungan Radiobiologi dan Radiologi. Sekolah Kesihatan Awam Universiti Pusat Venezuela.

