Model atom
- 2669
- 819
- Clarence Greenholt DDS
 Model atom adalah representasi grafik yang berbeza yang telah diberikan kepada atom sepanjang sejarah. Shuttersock
Model atom adalah representasi grafik yang berbeza yang telah diberikan kepada atom sepanjang sejarah. Shuttersock Apa itu model atom?
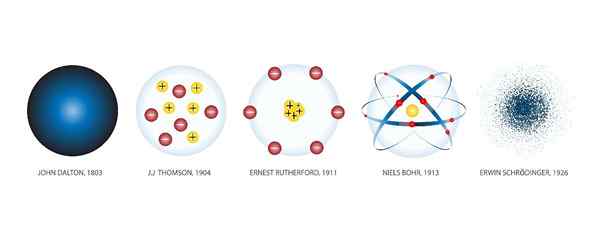
The Model atom Mereka adalah representasi grafik struktur dan operasi atom. Terdapat banyak model sepanjang sejarah.
Ini kerana idea atom sebagai blok asas yang dibuat, dilahirkan ribuan tahun yang lalu, di Yunani kuno. Pada masa itu atom hanyalah produk spekulasi falsafah.
Apabila penemuan saintifik baru dibuat, model baru dicipta untuk menggabungkan pengetahuan yang diperoleh. Oleh itu, ia telah berlaku abad selepas abad sehingga hari ini, ketika teknologi telah membolehkan kita memerhatikan atom melalui mikroskop dan menentukan model yang betul.
Apa itu atom?
Atom adalah struktur submikroskopik yang mana semua subjek yang kita anggap terbentuk dan dengan mana kita berinteraksi setiap hari, dari tubuh kita sendiri, makanan yang kita makan, pakaian yang kita pakai, ke bangunan pencakar langit dan pesawat besar.
Juga, matahari, bulan, planet, bintang dan galaksi dibentuk dengan atom.
Ini sangat kecil sehingga mereka tidak dapat dilihat dengan mikroskop biasa. Yang lain diperlukan dengan kuasa yang lebih besar, yang dipanggil ultramicroscopes. Walau bagaimanapun, atom bukan unit alam yang paling kecil.
Atom dibentuk sebaliknya oleh zarah yang lebih kecil: proton, neutron dan elektron.
Proton mempunyai caj elektrik positif, sementara neutron tidak mempunyai caj elektrik. Kedua -dua jenis zarah ini membentuk nukleus atom.
Berputar di sekitar nukleus seperti planet di sekeliling matahari adalah elektron, yang mempunyai cas elektrik negatif.
Model atom Demokritus

Demokritus Abdera adalah seorang ahli falsafah Yunani yang tinggal di antara 460 dan 370 sebelum era semasa. Dia mengesahkan bahawa semua perkara dibentuk oleh zarah -zarah kecil yang dipanggil atom, yang dalam bahasa Yunani bermaksud tidak dapat dipisahkan.
Menurut Democritus, atom adalah bahagian terkecil di mana perkara itu dapat dibahagikan. Terdapat bilangan yang tidak terhingga, yang tidak dapat dihancurkan, luar biasa, kekal dan benar -benar padat, tanpa liang. Terdapat beberapa jenis, yang berbeza mengikut bentuk, magnitud, kedudukan dan cara mereka bersedia.
Ia boleh melayani anda: bencana yang disebabkan oleh manusia semasa menggunakan sains dan teknologiTeori Demokritus ditolak oleh Aristotle dan kemudian dilupakan sehingga kemunculan sains moden.
Model Atom Dalton

John Dalton (1766-1844) adalah ahli meteorologi Inggeris yang berminat untuk menyiasat undang-undang yang mengawal tingkah laku gas. Buah karyanya di bidang itu adalah model atom pertama sains moden, yang dibuatnya pada tahun 1803.
Oleh kerana kewujudan proton dan elektron belum ditemui, kata Dalton, seperti Democritus, bahawa atom adalah bahagian terkecil di mana perkara dapat dibahagikan dan, oleh itu, dengan sendirinya, ia tidak dapat dipisahkan.
Menurut Dalton, atom adalah pepejal dan mempunyai bentuk sfera, seperti bola besbol. Dalton menggambarkan ukiran teorinya di kayu, bersama dengan pembantunya, berpuluh -puluh sfera yang mewakili atom -atom unsur kimia yang berbeza.
Model ini berkuatkuasa sehingga penemuan elektron.
Model Thomson Atom
Ahli fizik Inggeris Joseph John Thomson (1865-1940) terpaksa membuat salah satu penemuan yang paling penting dalam sains moden: iaitu elektron.
Ia pada tahun 1897, di makmal Cavendish di University of Cambridge, di England, di mana plak masih memperingati penemuan hebat.
Thompson dan pembantunya memproyeksikan sinar katod di medan elektrik. Apabila bersentuhan dengan lapangan, sinar menyimpang membentuk sudut lebar. Ini mengesahkan bahawa sinar katod mempunyai caj elektrik negatif. Zarah -zarah yang dikenakan secara negatif memanggil mereka elektron.
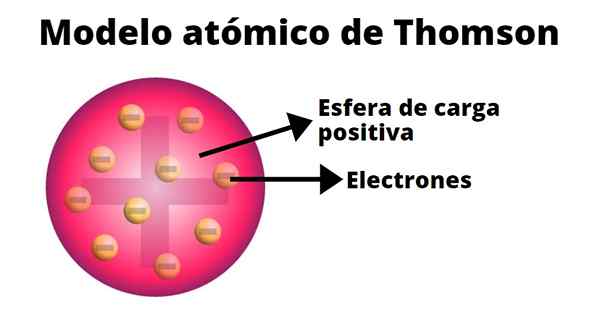
Thomson mengandaikan bahawa elektron tertanam dalam atom. Model atomnya bermula dari tahun 1904.
Puding kismis
Dalam model atom Thompson atom adalah sfera pepejal dengan beban positif (proton) di mana neutron (beban negatif) diedarkan secara rawak, seperti kismis yang dilemparkan pada pudin. Itulah sebabnya model ini dikenali sebagai "Pudin de Pasas".
Menurut Thompson, atom mempunyai jejari 0.00000001 sentimeter dan bebannya adalah neutral, kerana proton dan elektron mempunyai beban yang sama, tetapi tanda bertentangan.
Model Thompson tidak membentangkan neutron.
Model Atom Rutherford
Ernest Rutherford (1871-1937), seorang ahli fizik Neozylean, adalah salah seorang pelajar Thomson yang paling menonjol.
Boleh melayani anda: Penyelidikan korelasiPada tahun 1911, dan berdasarkan penemuan radioaktiviti baru -baru ini, Rutherford menjalankan eksperimen berikut: mereka menembak zarah radioaktif alfa dengan kelajuan tinggi dan tenaga terhadap sekeping emas.
Sekiranya model atom Thompson betul, zarah alfa akan melalui lembaran tanpa menyimpang atau dengan sisihan yang tidak penting. Walau bagaimanapun, apabila mereka mengira sudut sisihan dari zarah -zarah yang mereka dapati bahawa ia adalah luas, dan beberapa bahkan melantun ke atas lembaran keemasan.
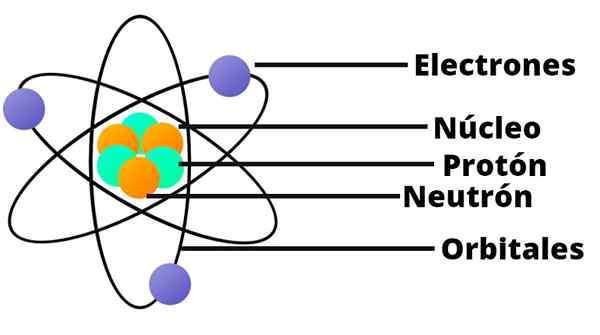
Dengan hasil ini Rutherford memahami bahawa atom harus mempunyai teras yang sangat kecil dan sangat pekat. Nukleus ini dicas secara positif.
Sistem suria kecil
Model Atom Rutherford seperti sistem suria kecil. Di tengah -tengah, di tempat yang sesuai dengan matahari, terdapat teras dengan proton yang dimuatkan secara positif. Sekitar ini, mengorbit sebagai planet, terdapat elektron yang diedarkan secara rawak.
Rutherford juga menegaskan bahawa jisim atom bersamaan dengan jumlah jisim elektron dan proton.
Model Atom Bohr
Walaupun model Rutherford adalah pendahuluan yang tidak dapat dinafikan berkenaan dengan model terdahulu, ia mempunyai kecacatan penting. Sebagai contoh, jika elektron berkesan orbital di sekitar nukleus mereka akan kehilangan tenaga dan runtuh pada nukleus. Tetapi ini jelas tidak berlaku.
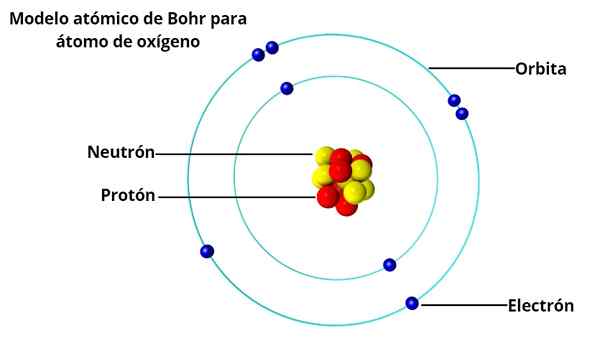
Ia adalah ahli fizik Denmark Niels Bohr (1885-1962), seorang pelajar Rutherford di University of Manchester (England), yang akan mencadangkan pada tahun 1913 sebagai model atom yang menyelesaikan masalah yang ditimbulkan oleh profesor lamanya.
Orbit bulat
Dalam model atom Bohr, elektron tidak mengorbit secara bebas di sekitar nukleus, tetapi berbuat demikian dalam orbit bulat yang stabil, dipisahkan antara satu sama lain dengan jarak tertentu, sama seperti bagaimana planet sistem solar disusun. Setiap orbit dipanggil tahap tenaga atau tenaga.
Berdasarkan penyiasatan Max Planck dan Albert Einstein, beliau memutuskan bahawa setiap elektron di orbit mereka mempunyai jumlah tenaga tertentu.
Semasa mengorbit stabil di sekitar nukleus, dikatakan bahawa elektron berada dalam keadaan pegun. Sebaliknya, apabila elektron "melompat" ke orbit tenaga yang lebih rendah, ada foton.
Boleh melayani anda: metodologiWalau bagaimanapun, model Bohr tidak berjaya menjelaskan operasi atom dengan lebih daripada satu elektron.
Model atom Sommerfeld
Arnold Sommerfeld (1868-1951) adalah seorang ahli fizik Jerman yang mendedikasikan karyanya untuk memperluaskan model atom Bohr. Model lanjutan ini dibentangkan pada tahun 1916.
Berdasarkan teori relativiti Einstein, Sommerfeld mendapati bahawa beberapa elektron mengorbit di sekitar nukleus pada kelajuan berhampiran cahaya (300.000 kilometer sesaat).
Beliau juga membuat pengubahsuaian berikut kepada model Bohr:
- Elektron bergerak di sekitar nukleus dalam orbit bulat dan elips. Bohr hanya mengiktiraf orbit bulat.
- Dalam tahap tenaga yang sama terdapat sub -level dengan tenaga yang sedikit berbeza.
Model mekanikal kuantum (Broglie, Heisenberg dan Schrödinger)
Ini adalah model atom yang paling tepat yang diketahui dan kini diterima, dengan beberapa penambahan berikutnya. Ia dibangunkan oleh tiga saintis: Jerman Werner Heisenberg (1901-1976), Austria Erwin Schrödinger (1887-1961) dan orang Perancis Louis de Broglie (1892-1987).
Model ini membuang idea elektron yang mengorbit nukleus. Sebaliknya, kita mempunyai awan elektronik, yang merupakan ruang di sekitar nukleus di mana ia mungkin untuk mencari elektron. Ini berkelakuan seperti gelombang pegun.
Kebarangkalian mencari ia dikira dengan persamaan yang ditubuhkan oleh Schrödinger.
Ini adalah model mekanikal kuantum atom yang bermula dari persamaan Schrödinger. Dengan persamaan ini, anda dapat mengetahui kebarangkalian mencari elektron pada titik tertentu atom.
Dalam model ini setiap elektron bergerak ke arah tertentu, yang ditentukan oleh empat nombor kuantum, iaitu: nombor kuantum utama, nombor kuantum sekunder, nombor kuantum magnet dan putaran nombor kuantum.
Tidak ada dua elektron yang mempunyai nombor kuantum yang sama, seperti yang dinyatakan oleh prinsip pengecualian yang ditemui oleh ahli fizik Wolfgang Pauli.
Rujukan
- (2010). Atom. Ensiklopedia moden British.
- (s. F.). Model Atom Demokritus, Atomisme Falsafah. Diambil dari tenaga nuklear.jaring.
- (s. F.). Model atom Sommerfeld, pengembangan kepada model Bohr. Diambil dari tenaga nuklear.jaring.
- Bertsch, g. F.; Trefil, James dan McGrayne, Sharon Bertsch (2021). Atom. Britannica Encyclopedia. Diambil dari Britannica.com.
- Duignan, b. (2021). Democritus. Britannica Encyclopedia. Diambil dari Britannica.com.
- Penyumbang Ensiklopedia Dunia Baru. (2021). Atom. Diambil dari Newworldyclopedia.org.
- Zita, Ana. (s. F.). Model atom. Diambil dari Todamateria.com.

