Struktur, C6H5NO2) Struktur, Kegunaan, Risiko, Risiko,
- 4282
- 775
- Erick Krajcik
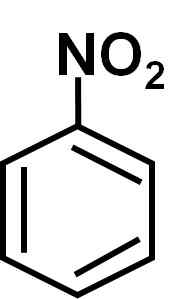
Dia Nitrobenzene Ia adalah sebatian organik aromatik yang dibentuk oleh cincin benzenik c6H5- Dan kumpulan nitro -no2. Formula kimianya adalah c6H5Tidak2. Ia adalah cecair berminyak berwarna kuning atau pucat, dengan bau badam pahit atau kasut untuk kasut.
Nitobenzene adalah sebatian yang sangat berguna dalam industri kimia kerana ia membolehkan untuk mendapatkan satu siri bahan kimia yang mempunyai pelbagai kegunaan. Ini kerana ia boleh tertakluk kepada pelbagai jenis tindak balas.
 Nitrobencene, c6H5-Tidak2. Pengarang: Marilú Stea.
Nitrobencene, c6H5-Tidak2. Pengarang: Marilú Stea. Antara tindak balas kimia yang penting adalah nitrasi (yang membolehkan anda menambah lebih banyak kumpulan -not2 kepada molekul) dan pengurangan (bertentangan dengan pengoksidaan kerana kedua -dua atom oksigen kumpulan nitro -no dihapuskan2 dan digantikan oleh hidrogen).
Dengan Nitrobencene, anda boleh mempersiapkan contoh Aniline dan Para-Acetaminophenol. Yang terakhir adalah acetaminophen yang terkenal yang merupakan antipyretik (ubat demam) dan analgesik lembut (ubat sakit kecil).
Nitobenzene mesti dimanipulasi dengan berhati -hati kerana ia menjengkelkan dan toksik, ia boleh menyebabkan jenis anemia, antara beberapa gejala, dan dipercayai bahawa ia boleh menyebabkan kanser. Ia juga membahayakan alam sekitar.
[TOC]
Struktur
Nitrobenzene c6H5-Tidak2 Ia adalah molekul rata yang dibentuk oleh cincin benzenik c6H5- yang mana kumpulan nitro dikaitkan -bukan2. Molekulnya rata kerana terdapat interaksi elektronik antara kumpulan nitro -no2 Dan cincin benzena.
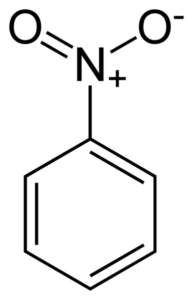 Struktur rata molekul nitrobenzene. Elektron pautan cincin Bondyan berganda cenderung berinteraksi dengan kumpulan nitro -no2. Pengarang: Benjah-bmm27. Sumber: Wikimedia Commons.
Struktur rata molekul nitrobenzene. Elektron pautan cincin Bondyan berganda cenderung berinteraksi dengan kumpulan nitro -no2. Pengarang: Benjah-bmm27. Sumber: Wikimedia Commons. Kumpulan nitro -no2 cenderung menarik elektron cincin benzenik c6H5-.
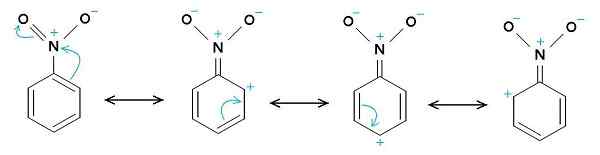 Struktur resonans nitrobenzene. Cincin benzena cenderung mempunyai beban positif, sementara kumpulan nitro -no2 cenderung mempunyai beban negatif. Pemuat semula asal adalah Samuele Madini di Wikipedia Itali. [Domain awam]. Sumber: Wikimedia Commons.
Struktur resonans nitrobenzene. Cincin benzena cenderung mempunyai beban positif, sementara kumpulan nitro -no2 cenderung mempunyai beban negatif. Pemuat semula asal adalah Samuele Madini di Wikipedia Itali. [Domain awam]. Sumber: Wikimedia Commons. Itulah sebabnya molekul mempunyai sisi yang sedikit lebih negatif (di mana oksigen -no adalah2) dan sisi yang sedikit lebih positif (cincin benzena).
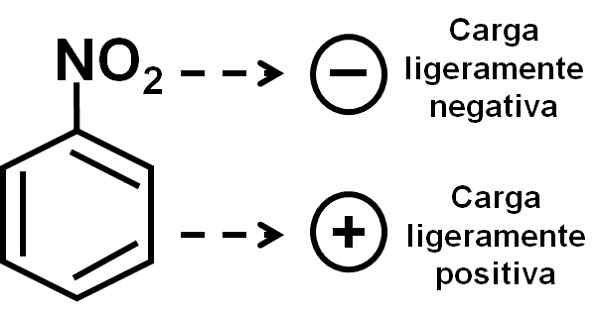 Oksigen kumpulan nitro mempunyai sedikit beban negatif berbanding dengan cincin benzenik. Pengarang: Marilú Stea.
Oksigen kumpulan nitro mempunyai sedikit beban negatif berbanding dengan cincin benzenik. Pengarang: Marilú Stea. Nomenclature
- Nitrobenzene.
- Nitrobenze.
- Nitrobenzole.
- Minyak atau intipati mirbano atau mirbana (istilah yang tidak digunakan).
Sifat
Keadaan fizikal
Cecair berminyak berwarna -warni menjadi kuning pucat.
Berat molekul
123.11 g/mol.
Takat lebur
5.7 ºC.
Takat didih
211 ºC.
Ia boleh melayani anda: kobalt klorida (cocl2 (: struktur, nomenclature, sifatTitik kilat
88 ºC (kaedah cawan tertutup).
Suhu sendiri
480 ° C.
Ketumpatan
1,2037 g/cm3 pada 20 ºC.
Kelarutan
Air larut kecil: 0.19 g/100 g air pada 20 ° C. Sama sekali dengan alkohol, benzena dan eter.
Sifat kimia
Nitrobencene stabil sehingga suhu kira -kira 450 ° C di mana ia mula menguraikan pembentukan (jika tiada oksigen) tidak, tidak2, benzena, biphenyl, aniline, dibenzofurano dan naphthalene.
Antara tindak balas penting nitrobencene ialah pengurangan, nitrasi, halogenasi dan sulfonasi.
Nitrobenzene Nitration pada mulanya menghasilkan meta-nitrobenzene dan dengan masa yang lama reaksi, 1,3,5-nitobenzene diperolehi.
Reacting bromin atau klorin dengan nitrobenzene dengan kehadiran pemangkin yang sesuai diperolehi 3-bromo-nitrobenzene (meta-bromonitrobencene) atau 3-cllor-nitrobenzene (meta-chloronitrobenzene).
Contoh pengurangan ialah apabila berurusan dengan timah (SN) dalam asid hidroklorik (HCl) meta-halogenonitobenzenes diperolehi oleh meta-halogenoanylins.
Sulfonasi nitrobenzene dilakukan dengan asid sulfurik merokok pada 70-80 ° C dan produknya adalah meta-nitrobenzeulfonic meta-nitrobenze. Ini dapat dikurangkan dengan besi dan HCl untuk memberikan asid metanil.
Pembentukan Dimmer
Dalam penyelesaian benzena c6H6 Molekul Nitrobencene dikaitkan dengan antara satu sama lain yang membentuk diameter atau molekul pasangan. Dalam pasangan ini salah satu molekul berada dalam kedudukan terbalik berkenaan dengan yang lain.
Pembentukan diameter nitrobenzene dengan molekul satu dalam kedudukan terbalik berkenaan dengan yang lain mungkin disebabkan oleh fakta bahawa masing -masing mempunyai sisi yang sedikit lebih positif dan sebaliknya dengan beban yang lebih negatif.
Di dimer bahagian dengan beban sedikit lebih positif salah satu molekul mungkin terletak berdekatan dengan beban sedikit negatif molekul lain, kerana beban bertentangan tertarik, dan oleh itu ia berlaku dengan dua sisi lain.
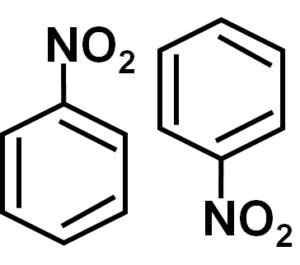 Nombor nitrobencene, iaitu, dua molekul yang cenderung bersama dalam beberapa pelarut. Pengarang: Marilú Stea.
Nombor nitrobencene, iaitu, dua molekul yang cenderung bersama dalam beberapa pelarut. Pengarang: Marilú Stea. Sifat lain
Ia memberikan bau yang serupa dengan badam atau menggilap kasut. Dengan menurunkan suhu mengukuhkannya dalam bentuk kristal kuning kehijauan.
Memperoleh
Anda merawat benzena c6H6 Dengan campuran asid nitrik hno3 dan asid sulfurik h2SW4. Proses ini dipanggil nitrasi dan melibatkan pembentukan ion nitronium tidak2+ Terima kasih kepada kehadiran asid sulfurik h2SW4.
- Nitronio ion no2+:
Hno3 + 2 jam2SW4 ⇔ h3Sama ada+ + 2 HSO4- + Tidak2+ (Ion nitronio)
- Ion Nitronio menyerang benzena:
Boleh melayani anda: Kesalahan sistematik: Cara mengira, dalam kimia, dalam fizik, contohC6H6 + Tidak2+ → c6H6Tidak2+
- Nitrobencene dibentuk:
C6H6Tidak2+ + Hso4- → c6H5Tidak2 + H2SW4
Ringkasnya:
C6H6 + Hno3 → c6H5Tidak2 + H2Sama ada
Reaksi nitrasi benzena sangat eksotermik, iaitu, sangat panas dihasilkan, jadi sangat berbahaya.
Aplikasi
Dalam mendapatkan aniline dan acetaminophen
Nitrobencene terutamanya digunakan untuk mensintesis aniline c6H5NH2, yang merupakan sebatian yang digunakan secara meluas untuk penyediaan racun perosak, gusi, pewarna, bahan letupan dan ubat -ubatan.
Mendapatkan aniline berlaku dengan mengurangkan nitrobenzene dalam medium berasid dengan kehadiran besi atau timah, yang dilakukan mengikut langkah -langkah berikut:
Nitrobenzene → nitrosobenzene → phenylhydroxylamine → aniline
C6H5Tidak2 → c6H5Tidak → c6H5NHOH → C6H5NH2
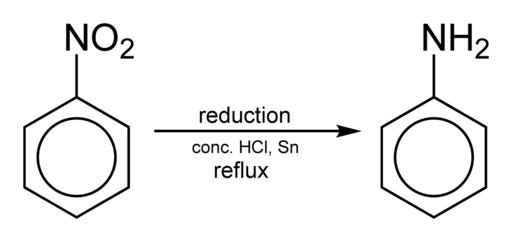 Pengurangan nitrobencene untuk mendapatkan aniline. Benjah-bmm27 [domain awam]. Sumber: Wikimedia Commons.
Pengurangan nitrobencene untuk mendapatkan aniline. Benjah-bmm27 [domain awam]. Sumber: Wikimedia Commons. Bergantung pada keadaan, proses boleh dihentikan di salah satu langkah pertengahan misalnya dalam phenylhydroxylamine. Bermula dari phenylhydroxylamine dalam persekitaran yang kuat, para-aminophenol dapat disediakan:
Phenylhdroxylamine → p-Aminophenol
C6H5NHOH → HOC6H4NH2
Yang terakhir dirawat dengan anhidrida asetik untuk mendapatkan paracetamol (acetaminophen) analgesik antipyretik dan lembut yang lembut, iaitu, ubat untuk merawat demam dan kesakitan dan kesakitan.
 Kadang -kadang ada kemungkinan untuk mengubati acetaminophen kepada kanak -kanak dengan demam. Acetaminophen adalah derivatif nitrobenzene. Pengarang: Augusto Ordonez. Sumber: Pixabay.
Kadang -kadang ada kemungkinan untuk mengubati acetaminophen kepada kanak -kanak dengan demam. Acetaminophen adalah derivatif nitrobenzene. Pengarang: Augusto Ordonez. Sumber: Pixabay.  Pil acetaminophen, derivatif nitrobenzene. PARACETAMOL_ACETAMINOPHEN_500_MG_PILS.JPG: Suku Michelle dari Ottawa, Kerja Canaderivatif: Anrie [CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)]. Sumber: Wikimedia Commons.
Pil acetaminophen, derivatif nitrobenzene. PARACETAMOL_ACETAMINOPHEN_500_MG_PILS.JPG: Suku Michelle dari Ottawa, Kerja Canaderivatif: Anrie [CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)]. Sumber: Wikimedia Commons. Satu lagi cara untuk mendapatkan aniline adalah dengan mengurangkan nitrobenzene dengan karbon monoksida (CO) dalam medium berair dengan kehadiran zarah yang sangat kecil (nanopartikel) paladium (PD) sebagai pemangkin.
C6H5-Tidak2 + 3 co + h2O → c6H5-NH2 + 3 co2
Dalam mendapatkan sebatian kimia lain
Nitobenzene adalah titik permulaan untuk mendapatkan pelbagai sebatian yang digunakan seperti pewarna, racun perosak, ubat -ubatan dan kosmetik.
 Beberapa pewarna diperoleh terima kasih kepada nitrobenzene. Pengarang: Edith Lüthi. Sumber: Pixabay.
Beberapa pewarna diperoleh terima kasih kepada nitrobenzene. Pengarang: Edith Lüthi. Sumber: Pixabay. Sebagai contoh, ia membolehkan untuk mendapatkan 1.3-dinitrobencene yang oleh pengklorinan (penambahan klorin) dan pengurangan (penghapusan atom oksigen) menghasilkan 3-chloroanylin. Ini digunakan sebagai perantara untuk racun perosak, pewarna dan ubat -ubatan.
Nitobenzene digunakan untuk menyediakan benchidine yang merupakan pewarna. Di samping itu, nitrobenzene berfungsi untuk menyediakan quinoline, azobenzene, asid metanil, dyitobenzene, isocianate atau pyroxilin di kalangan banyak sebatian lain.
Dalam beberapa aplikasi
Nitobenzene digunakan atau digunakan sebagai:
Boleh melayani anda: hidrokarbon tak tepu- Pelarut pengekstrakan untuk penyucian minyak pelincir yang digunakan dalam jentera
- Pelarut untuk ether selulosa
- Bahan campuran untuk logam menggilap
- Dalam sabun
- Dalam campuran untuk kasut Poland
- Semburan cat konservator
- Komponen campuran penggilap lantai
- Pengganti Essence Almond
- Dalam industri minyak wangi
- Dalam pengeluaran getah sintetik
- Pelarut dalam pelbagai proses
 Nitobenzene adalah sebahagian daripada beberapa campuran untuk kasut Poland. D-kuru [CC BY-SA 3.0 di (https: // creativeCommons.Org/lesen/by-sa/3.0/at/perbuatan.dalam)]. Sumber: Wikimedia Commons.
Nitobenzene adalah sebahagian daripada beberapa campuran untuk kasut Poland. D-kuru [CC BY-SA 3.0 di (https: // creativeCommons.Org/lesen/by-sa/3.0/at/perbuatan.dalam)]. Sumber: Wikimedia Commons. Risiko
Nitobenzene adalah toksik dengan penyedutan, pengambilan dan penyerapan melalui kulit.
Menjengkelkan kulit, mata dan saluran pernafasan. Ia boleh menyebabkan jenis anemia yang dipanggil methemoglobinemia yang terdiri daripada mengurangkan keupayaan sel darah merah untuk melepaskan oksigen dalam tisu dan menghasilkan keletihan.
Di samping itu, nitrobencene menyebabkan dyspnea, pening, penglihatan kecewa, kekurangan nafas, keruntuhan dan kematian. Ia juga merosakkan hati, limpa, buah pinggang dan sistem saraf pusat.
Dianggarkan bahawa ia boleh menjadi mutagen dan mungkin menyebabkan kanser manusia, kerana ia telah menyebabkannya pada haiwan.
Selain itu, Nitrobencene tidak boleh dibuang di alam sekitar. Ketoksikannya terhadap haiwan, tumbuh -tumbuhan dan mikroorganisma menjadikannya sangat berbahaya kepada ekosistem.
Ketoksikan ke arah mikroorganisma mengurangkan biodegradabilitynya.
Rawatan untuk penghapusan persekitarannya
Pencemaran alam sekitar dengan nitrobencene boleh berlaku melalui pembaziran pelbagai industri yang menggunakannya, seperti industri pewarna atau bahan peledak.
Nitobenzene adalah sangat toksik dan sukar untuk dipecahkan di bawah keadaan semula jadi, kerana sebab ini ia boleh menyebabkan pencemaran yang teruk dan menyemai sistem pengairan.
Oleh kerana kestabilan dan ketoksikannya yang tinggi terhadap mikroorganisma, ia sering dipilih sebagai model dalam kajian rawatan kumbahan.
Pelbagai cara sedang disiasat untuk menghapuskan nitrobenzene air yang tercemar. Salah satu daripada mereka adalah melalui degradasi photocatalytic, iaitu, menggunakan cahaya matahari sebagai pemecut tindak balas degradasi dengan kehadiran titanium dioksida titanium2.
 Dengan reaktor cahaya matahari, mungkin untuk menghapuskan pencemaran air dengan nitrobencene. Mihai-cosmin pascariu [cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons.
Dengan reaktor cahaya matahari, mungkin untuk menghapuskan pencemaran air dengan nitrobencene. Mihai-cosmin pascariu [cc by-sa (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons. Kaedah mikroelektrik juga telah berjaya diuji dengan pemangkin besi (iman) dan tembaga (CU) dalam seramik. Mikroelektrik membolehkan nitrobenzene untuk mengurai melalui arus elektrik.
Rujukan
- Atau.S. Perpustakaan Perubatan Negara. (2019). Nitrobenzene. Pulih dari pubchem.NCBI.NLM.NIH.Gov.
- Morrison, r.T. dan Boyd, r.N. (2002). Kimia organik. Edisi ke -6. Prentice-Hall.
- Moldoveanu, s.C. (2019). Pirolisis sebatian nitrogen lain. Dalam Pirolisis Molekul Organik (edisi kedua). Pulih dari Scientedirect.com.
- Smith, ms.W.G. et al. (1969). Sebatian nitrasi-nitro aromatik. Penggantian elektrofilik. Dalam kimia aromatik. Pulih dari Scientedirect.com.
- Windholz, m. et al. (editor) (1983). Indeks Merck. Eniklopedia bahan kimia, ubat, dan biologi. Edisi Kesepuluh. Merck & Co., INC.
- Ensiklopedia Kimia Perindustrian Ullmann. (1990). Edisi Kelima. Jilid A22. VCH Verlagsgellschaft MBH.
- Whang, t.-J. et al. (2012). Degradasi Photocatalytic UV Nitrobenzene oleh Titania mengikat pada tiub kuarza. Jurnal Antarabangsa PhotoEnergy, Volume 2012, Artikel ID 681941. Hyndawi pulih.com.
- Shikata, t. et al. (2014). Pembentukan dimer anti-selari nitrobenzene dalam pelarut bukan polar. AIP Kemajuan 4, 067130 (2014). Pulih dari Doaj.org.
- Krogul-Obczak, a. et al. (2019). Pengurangan nitrobenzene ke aniline oleh co/h2Atau menyaksikan nanopartikel paladium. Pemangkin 2019, 9, 404. MDPI pulih.com.
- Yang, b. et al. (2019). Pengeluaran Skala Pilot, Harta dan Penggunaan Fe/Cu Pemangkin-Pemancar Fe/Cu untuk Rawatan Air Sisa Nitrobenzene. Pemangkin 2019, 9, 11. MDPI pulih.com.
- « Formula Kelebihan Mekanikal, Persamaan, Pengiraan dan Contoh
- 110 frasa cinta abadi untuk teman lelaki dan suami »

