Penyelesaian hipertonik
- 2854
- 160
- Dallas Bernhard
Kami menerangkan apa penyelesaian hipertonik, ciri -ciri mereka, apakah penggunaannya, perbezaan dengan hipotonik dan memberi beberapa contoh
Ramai yang akan terkejut mengetahui bahawa tumbuhan cara menyerap air melalui akar mereka dan cara di mana jari tangan berkerut ketika mandi di air laut, mereka berkait rapat.
Kedua -dua perkara itu berlaku kerana kewujudan membran yang berfungsi sebagai penapis, dan penyelesaian hipertonik yang secara harfiah menghisap air melaluinya. Tetapi apakah penyelesaian hipertonik?
Dalam artikel ini, soalan ini akan dijawab, dan ciri -ciri penyelesaian hipertonik yang paling relevan juga akan dibentangkan, bagaimana mereka, bagaimana mereka dibezakan dari jenis penyelesaian lain dan beberapa contoh yang sama.
Apakah penyelesaian hipertonik?
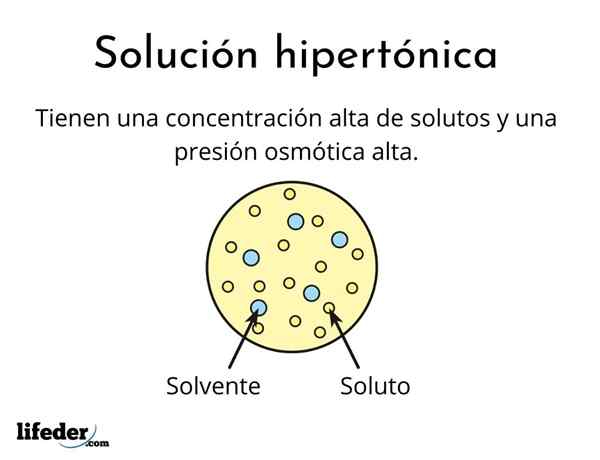
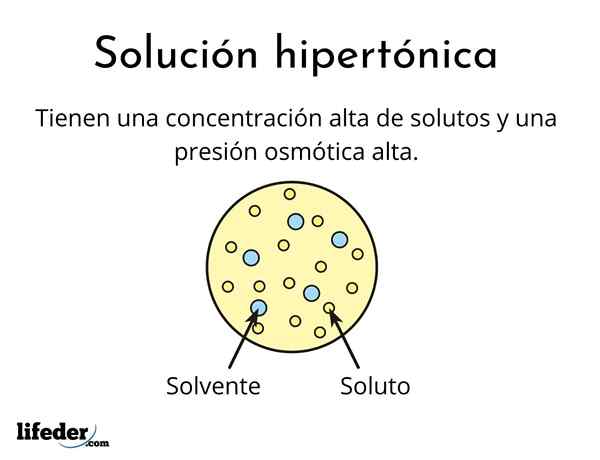
A penyelesaian hipertonik Ia adalah salah satu yang mengandungi kepekatan jumlah larutan aktif osmolarly lebih besar daripada penyelesaian rujukan lain. Osmolarily aktif bermaksud bahawa larutan tidak dapat menyeberangi jenis membran khas (serupa dengan kain) yang bertindak sebagai penapis atau penapis, iaitu, biarkan air lulus, dan bukannya zarah larut.
Kepekatan larutan yang tinggi ini menyebabkan penyelesaian hipertonik mempunyai tekanan osmotik yang tinggi. Tekanan ini adalah apa yang praktikal menghisap air melalui membran, yang dipanggil osmosis.
Kata hipertonik berasal dari awalan Yunani hiper-, yang bermaksud "di, atau ke atas" dan "nada", yang bermaksud ketegangan, atau tekanan, jadi hipertonik secara harfiah bermaksud "bahawa ia mempunyai tekanan atau ketegangan yang lebih besar".
Adalah penting untuk diingat bahawa, dalam biologi dan perubatan, dengan syarat terdapat perbincangan mengenai penyelesaian hipertonik, ia merujuk kepada penyelesaian yang lebih tertumpu daripada larutan yang terkandung dalam darah, yang dipanggil plasma darah.
Ciri -ciri penyelesaian hipertonik
Penyelesaian hipertonik mempunyai beberapa ciri asas:
Mereka dibentuk oleh pelarut dan sekurang -kurangnya satu larut
Tidak ada penyelesaian yang boleh menjadi hipertonik, walaupun begitu pekat. Larut mesti tidak dapat menyeberang membran, sementara air mesti dapat lulus tanpa masalah, jika tidak, tekanan osmotik tidak dihasilkan.
Mereka mempunyai kepekatan larutan yang tinggi
Inilah yang menjadikan mereka penyelesaian hipertonik. Seperti yang disebutkan sebentar tadi, penyelesaian hipertonik lebih tertumpu daripada darah.
Ia boleh melayani anda: penyulingan pecahan: proses, peralatan, aplikasi, contohMereka boleh mempunyai komposisi yang berbeza
Penyelesaian hipertonik boleh mengandungi satu larutan seperti garam, atau boleh mengandungi campuran larutan seperti garam dan gula, sebagai contoh.
Solutos boleh ionik, neutral, atau kedua -duanya
Jualan mengandungi ion dengan caj elektrik yang tidak membiarkan mereka menyeberang membran, jadi mereka kecil. Larutan lain tidak mempunyai ion, tetapi mereka besar dan gemuk dan tidak sesuai dengan lubang.
Mereka mempunyai tekanan osmotik yang tinggi
Seperti yang disebutkan di atas, penyelesaian hipertonik mempunyai tekanan osmotik yang lebih besar daripada darah.
Mereka boleh dehidrasi sel
Penyelesaian hipertonik mengekstrak air dari sel -sel yang meninggalkan mereka sebagai kismis. Itulah sebabnya tangan dan kaki kita berkedut ketika kita mandi di pantai.
Apakah penyelesaian hipertonik?
Penyelesaian hipertonik mempunyai banyak kegunaan dalam kehidupan seharian, dan juga dalam bidang perubatan. Beberapa kegunaan yang paling biasa adalah:
Mereka biasa menyimpan makanan
- Contoh: Peaches dalam sirap tidak reput kerana sirap mempunyai banyak gula terlarut dan merupakan penyelesaian yang sangat hipertonik. Dengan menghidrat sel, penyelesaian hipertonik tidak membenarkan kulat dan bakteria dalam makanan, kerana mereka mati akibat dahaga. Ini membolehkan makanan bertahan lebih banyak.
Mereka berkhidmat untuk mengurangkan keradangan
- Contoh: Apabila seseorang mengalami kemalangan dan memukul kepala, banyak kali keradangan di otak. Untuk menyembuhkan pesakit, doktor menyuntik penyelesaian penyelesaian garam sebanyak 7.5%. Penyelesaian ini praktikal menghisap air, mengurangkan keradangan di otak.
Mereka berkhidmat untuk menggantikan elektrolit.
- Contoh: Natrium adalah elektrolit yang kita perlukan untuk hidup, dan apabila pesakit mempunyai sedikit natrium dalam darah, larutan garam 7.5% disuntik untuk menambah natrium yang hilang.
Mereka digunakan untuk makanan parenteral
- Contoh: Apabila orang tidak dapat makan melalui mulut atau melalui tiub, mereka memberi makan dalam larutan hipertonik yang mengandungi jenis gula yang disebut glukosa.
Perbezaan dengan penyelesaian hipotonik dan isotonik
Sama seperti terdapat penyelesaian hipertonik, terdapat juga penyelesaian hipotonik dan isotonik. Perbezaan antara penyelesaian yang terakhir dan hipertonik adalah kepekatannya. Penyelesaian hipotonik adalah yang kurang tertumpu daripada darah, dan isotonik mempunyai kepekatan yang sama seperti darah.
Sebagai contoh, air tulen, kerana ia tidak mempunyai apa -apa larut, adalah hipotonik, sementara air kelapa mempunyai garam dan gula dengan kepekatan hampir sama dengan darah, jadi isotonik.
Selain membezakan dengan kepekatan mereka, hiper, hypo dan penyelesaian isotonik berbeza dengan cara mereka mempengaruhi sel.
Imej berikut menunjukkan kesan pelbagai jenis penyelesaian pada sel darah merah (sel kecil yang menjadikan darah merah).
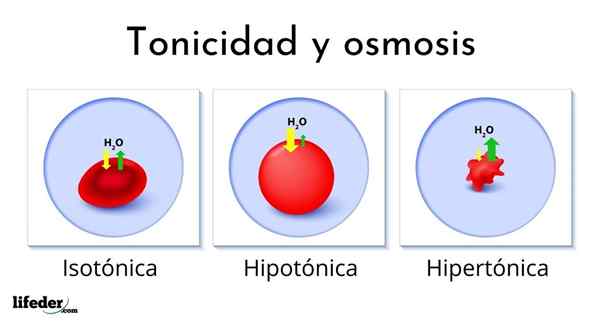
Sekiranya sel darah merah diperkenalkan menjadi larutan hipertonik, ia mengekstrak air, menghidangkannya dan meninggalkannya berkedut sebagai lulus.
Sebaliknya, jika ia diperkenalkan ke dalam larutan hipotonik, sel darah merah menyerap air dan membengkak, bahkan pecah seperti belon yang mengembang terlalu banyak. Akhirnya, jika mereka diperkenalkan ke dalam penyelesaian isotonik, air di dalam dan di luar sel darah merah akan seimbang sehingga tidak ada yang berlaku.
Contoh penyelesaian hipertonik
Sirap gula
 Peaches dalam sirap
Peaches dalam sirap Sirap di mana pic dan buah -buahan lain dipelihara mengandungi kepekatan gula yang sangat tinggi, jadi ia adalah penyelesaian hipertonik.
Air garam
Air garam adalah penyelesaian air dan garam dengan kepekatan yang sangat tinggi antara 3.5% dan 25%, yang boleh menjadi hampir 30 kali lebih tertumpu daripada darah (iaitu, sangat hipertonik).
Cuka
Cuka biasa adalah penyelesaian hipertonik, kerana ia mempunyai kepekatan antara 3% dan 5% asid asetik. Pengurangan cuka balsamic lebih tertumpu.
Boleh melayani anda: dimethylamine ((CH3) 2NH): struktur, sifat, kegunaan, risikoDarah yang sama dari urat kita, setelah berpeluh banyak.
Apabila bersenam dan berpeluh, badan menghilangkan air dan garam, tetapi menghilangkan lebih banyak air daripada garam (peluh adalah hipotonik) sehingga darah menumpukan perhatian dan menjadi hipertonik.
Air laut
Air laut mengandungi banyak garam terlarut, dengan jumlah kepekatan kira -kira 3.5%, yang menjadikannya hipertonik. Itulah sebabnya air laut berkedut jari kita.
Minuman manis
Minuman cola dan minuman manis lain boleh mengandungi sehingga 10% gula, serta garam dan larutan lain dengan kepekatan lebih besar daripada darah.
Penyelesaian Dextrose 5% dan 0.45% natrium klorida (D5 ½ ns)
Ini adalah contoh penyelesaian hipertonik yang digunakan untuk memberi makan kepada orang yang biasanya tidak dapat makan di mulut.
25% Mannitol
Ini adalah penyelesaian yang sering digunakan untuk merawat kejutan di kepala. Ia adalah empat kali lebih tertumpu daripada darah.
Penyelesaian salin 7.5%
Ia adalah penyelesaian garam yang cukup pekat yang juga disuntik dengan beberapa pesakit dengan penyakit tertentu di urat.
Jus komersial
Semua jus yang dibeli di pasar raya dan yang tidak semulajadi, mempunyai kepekatan gula yang sangat tinggi yang menjadikannya hipertonik.
Rujukan
- Sweeney J. Menguruskan hypernatremia. Kejururawatan. September 2010; 40 (9): 63.
- Air garam. Wikipedia. 2021. Diambil daripada.Wikipedia.org/wiki/air garam.
- Air laut. Wikipedia. 2021. Diambil daripada.Wikipedia.Org/wiki/air laut.
- Chavaltamrong B, Pidatcha P, Thavisri U. Elektrolit, gula, kalori, osmolariti dan pH minuman dan air kelapa. Kesihatan Awam Asia Tenggara. September 1982; 13 (3): 427-431.
- 5% dextrose dan 0.Suntikan natrium klorida 45%, USP. FDA. 2006. Diambil dari AccessData.FDA.Gov/Drugsatfda_docs/Label/2006/017607S123lbl.Pdf.
- Llorente G, Niño MC. Manitol berbanding larutan garam hipertonik dalam neuroanesthesia. Majalah Anestesiologi Kolombia. Januari-Mac 2015; 43 (1): 29-39.
- Orang Suci MM, E. Rawatan asidosis laktik rumen akut dengan natrium klorida hipertonik intravena atau penyelesaian bikarbonat Fucked oleh air intrauminal. Penyelidikan dalam Sains Veterinar. Februari 2020; 128: 24-34.
- Dini-G. E, Abreu-C. JD, López-M. Dan. Osmolality minuman penggunaan kerap. Kajian klinikal. Disember 2004; 45 (4).

