Kesan penggantian nukleofilik aromatik, contoh
- 4805
- 1488
- Clarence Greenholt DDS
The Penggantian nukleofilik aromatik (SNAR) adalah tindak balas yang berlaku dalam kimia organik, yang terdiri daripada anjakan kumpulan keluar yang baik oleh nukleofil masuk. Dari sudut pandangan mekanisme dan aspek elektroniknya, ia adalah wajah yang bertentangan dengan penggantian elektrofilik aromatik (SEAR).
Umumnya kumpulan keluar adalah halogen, yang keluar sebagai anion haluro x-. Reaksi ini hanya boleh berlaku jika cincin aromatik (kebanyakannya benzena) kekurangan elektron; iaitu, jika anda mempunyai kumpulan substituen menarik elektron.
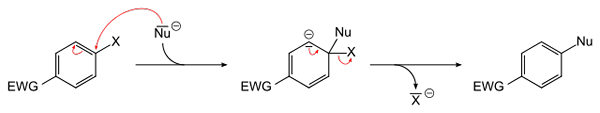
 Persamaan Am untuk penggantian nukleofilik aromatik. Sumber: Sponk [Domain Awam]
Persamaan Am untuk penggantian nukleofilik aromatik. Sumber: Sponk [Domain Awam] Imej Superior mencatatkan apa yang dikatakan dalam perenggan sebelumnya. Kumpulan Tarik Elektron EWG (untuk akronim dalam bahasa Inggeris: Kumpulan Pengeluaran Elektron), mengaktifkan cincin aromatik untuk serangan nukleofilik spesies NU negatif-. Dapat dilihat bahawa perantara terbentuk (di tengah), dari mana haluro X dibebaskan atau dibebaskan-.
Perhatikan bahawa dalam istilah x mudah ia digantikan oleh nu dalam cincin aromatik. Reaksi ini sangat serba boleh dan perlu dalam sintesis ubat -ubatan baru, serta dalam kajian kimia organik sintetik.
[TOC]
Ciri-ciri umum
Cincin aromatik boleh "dikenakan" atau "muat turun" dari elektron bergantung pada apa yang substituen mereka (mereka yang menggantikan pautan C-H yang asal).
Apabila substituen ini boleh mendermakan ketumpatan elektronik ke cincin, dikatakan bahawa mereka memperkayakannya dari elektron; Jika sebaliknya mereka adalah penarik ketumpatan elektronik (EWG yang disebutkan di atas), kemudian dikatakan bahawa mereka memusnahkan cincin elektron.
Walau apa pun, cincin diaktifkan untuk reaksi aromatik tertentu, sementara ia dinyahaktifkan untuk yang lain.
Sebagai contoh, cincin aromatik yang kaya dengan elektron dikatakan aktif untuk penggantian elektrofilik aromatik; Iaitu, anda boleh mendermakan elektron anda kepada spesies elektrofilasi, dan+. Walau bagaimanapun, ia tidak akan menderma elektron kepada spesies NU-, Oleh kerana caj negatif akan menangkis satu sama lain.
Boleh melayani anda: teori orbital molekulSekarang, jika cincin miskin di elektron, ia tidak mempunyai cara untuk memberikannya kepada spesies dan+ (Sear tidak berlaku); Sebaliknya, ketersediaan untuk menerima elektron spesies NU- (SNAR berkembang).
Perbezaan dengan penggantian elektrofilik aromatik
Menjelaskan aspek umum kemasukan, beberapa perbezaan antara SNAR dan sear kini boleh disenaraikan:
- Cincin aromatik bertindak sebagai elektrofil (elektron miskin) dan diserang oleh nukleofil.
- Kumpulan keluar X digantikan dari cincin; Bukan h+
- Tiada karbokati yang terbentuk, tetapi perantara dengan caj negatif yang boleh dipindahkan oleh resonans
- Kehadiran kumpulan yang lebih menarik di cincin mempercepat penggantian dan bukannya melambatkannya
- Akhirnya, kumpulan ini tidak menjalankan pengarah di mana (di mana karbon) penggantian akan berlaku. Penggantian akan selalu berlaku dalam karbon yang dikaitkan dengan kumpulan keluar x.
Titik terakhir juga digambarkan dalam imej: pautan c-x dipecahkan untuk membentuk pautan c-nu baru.
Kesan
Bilangan substituen
Sememangnya, yang lebih miskin dalam elektron adalah cincin, semakin cepat SNAR dan yang paling drastik akan menjadi syarat yang diperlukan untuk berlaku. Pertimbangkan contoh berikut yang diwakili dalam imej yang lebih rendah:
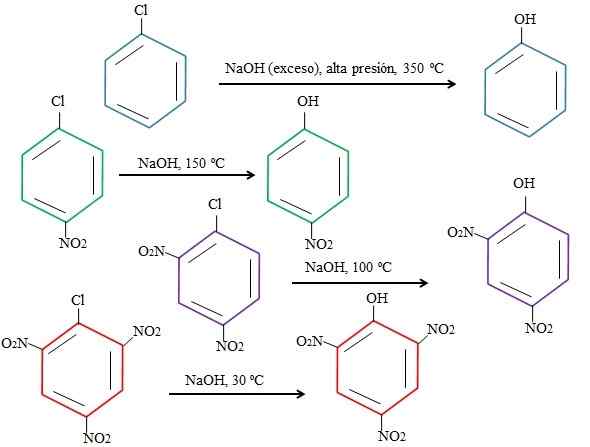 Kesan substituen pada penggantian 4-nitroclorobenzene. Sumber: Gabriel Bolívar.
Kesan substituen pada penggantian 4-nitroclorobenzene. Sumber: Gabriel Bolívar. Perhatikan bahawa 4-nitroclorobenzene (cincin biru) memerlukan keadaan drastik (tekanan tinggi dan suhu 350 ºC) kepada penggantian CL dengan. Dalam kes ini, klorin adalah kumpulan keluar (CL-), dan hidroksida nukleofil (OH-).
Ia dapat melayani anda: 4 tempoh kimia: dari prasejarah hingga hari iniApabila kumpulan tidak muncul2, yang merupakan penarik elektron (cincin hijau), penggantian boleh dilakukan pada suhu 150 ºC pada tekanan ambien. Oleh kerana bilangan kumpulan meningkat tidak2 Hadir (cincin ungu dan merah), penggantian berlaku pada suhu yang semakin rendah (100 ºC dan 30ºC, masing -masing).
Oleh itu, kumpulan tidak2 Mereka mempercepatkan Snar dan Latihan dari Elektron ke Cincin, menjadikannya lebih mudah terdedah kepada serangan OH-.
Kedudukan relatif CL tidak akan dijelaskan di sini berkenaan dengan tidak2 dalam 4-nitroclorobenzene, dan bagaimana mereka mengubah kelajuan reaksi; Sebagai contoh, kelajuan tindak balas 2-nitroclorobenzene dan 3-nitrochlorobenzene berbeza, yang terakhir adalah yang paling lambat berbanding dengan isomer lain.
Kumpulan keluar
Kembali ke 4-nitroclorobenzene, tindak balas penggantiannya lebih perlahan jika anda membandingkan rakan sejawat anda:
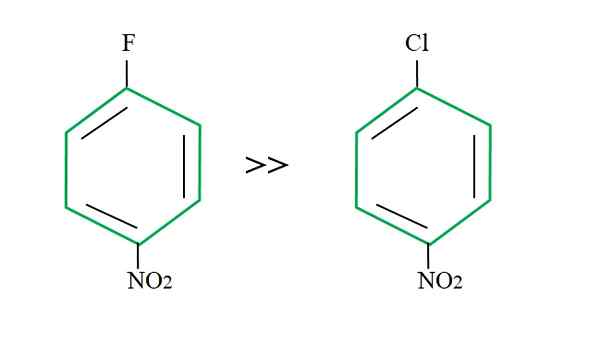 Kesan kumpulan keluar pada tindak balas SNAR. Sumber: Gabriel Bolívar.
Kesan kumpulan keluar pada tindak balas SNAR. Sumber: Gabriel Bolívar. Penjelasan ini tidak boleh terletak pada pemboleh ubah lain yang perbezaan antara f dan cl. Fluorine adalah kumpulan keluar yang buruk, kerana pautan C-F lebih sukar untuk dipecahkan daripada pautan C-CL. Oleh itu, pecahan pautan ini bukanlah langkah menentukan kelajuan untuk SNAR, tetapi penambahan NU- ke cincin aromatik.
Fluorin untuk menjadi lebih elektronegatif daripada klorin, atom karbon yang dikaitkan dengannya mempunyai kekurangan elektronik yang lebih besar (cδ+-Fδ-). Oleh itu, karbon pautan C-F lebih cenderung diserang oleh NU- daripada pautan c-cl. Itulah sebabnya pengganti f oleh oh jauh lebih cepat daripada cl oleh oh.
Boleh melayani anda: tembaga sulfida: struktur, sifat, kegunaanContoh
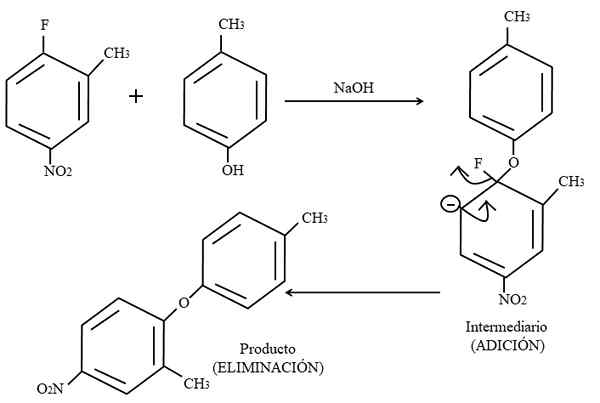 Menggantikan elektrofilik aromatik. Sumber: Gabriel Bolívar.
Menggantikan elektrofilik aromatik. Sumber: Gabriel Bolívar. Akhirnya, contoh tindak balas organik jenis ini dalam imej yang lebih tinggi ditunjukkan di bawah. Para-Coresol tidak memberikan penampilan sebagai nukleofil; Tetapi mempunyai medium asas, kumpulan OH tidak dilindungi, meninggalkan anion phenoxide, yang menyerang 2-methyl-4-nitrofluorzene.
Apabila serangan ini berlaku, dikatakan bahawa nukleofil ditambah ke elektrofil. Langkah ini dapat dilihat di sebelah kanan imej, di mana kompaun perantara dengan kedua -dua substituen milik cincin terbentuk.
Dengan menambahkan para-coresol, beban negatif muncul yang berpindah resonans di dalam cincin (notis yang berhenti menjadi aromatik).
Dalam imej, struktur resonans terkini hampir tidak ditunjukkan, dari mana fluorida selesai sebagai f-; Tetapi pada hakikatnya beban negatif ini menjadi disoccupy walaupun dalam atom oksigen kumpulan2. Selepas penambahan penghapusan, yang terakhir, iaitu ketika produk akhirnya terbentuk.
Komen akhir
Kumpulan tidak2 baki dapat dikurangkan kepada kumpulan NH2, Dan dari sana ada kemungkinan untuk membuat lebih banyak reaksi sintesis untuk mengubah suai molekul akhir. Ini menunjukkan potensi sintetik SNAR, dan mekanisme itu, sebagai tambahan, terdiri daripada dua langkah: salah satu penambahan dan salah satu penghapusan.
Walau bagaimanapun, pada masa ini terdapat bukti eksperimen dan pengiraan yang pada hakikatnya reaksi berlaku berikutan mekanisme bersepadu, di mana kedua -dua langkah berlaku serentak melalui kompleks yang diaktifkan dan bukan perantara.
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2019). Penggantian aromatik nukleofilik. Diperoleh dari: dalam.Wikipedia.org
- James Ashenhurst. (6 September 2019). Penggantian aromatik nukleofilik (NAS). Pulih dari: masterorganicchemistry.com
- Kimia Librettexts. (5 Jun, 2019). Penggantian aromatik nukleofilik. Pulih dari: chem.Libretxts.org

