Ciri -ciri Tyrosine, Struktur, Fungsi, Manfaat
- 3297
- 377
- Clarence Greenholt DDS
The Tyrosine (Tyr, y) adalah salah satu daripada 22 asid amino yang membentuk protein semua sel yang hadir dalam makhluk hidup. Tidak seperti asid amino lain seperti valine, treonine, tryptophan, leucine, lysine dan lain -lain, tyrosine adalah asid amino yang penting ".
Nama "Tyrosine" berasal dari perkataan Yunani "Menembak", yang bermaksud keju, kerana asid amino ini pertama kali ditemui dalam makanan ini. Istilah ini dicipta pada tahun 1846 oleh Liebig, yang bercampur keju dengan kalium hidroksida dan memperoleh sebatian yang tidak diketahui, tidak larut dalam air.
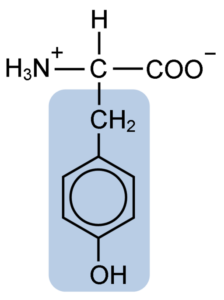 Struktur Kimia Asid Amino Tyrosine (Sumber: Clavecin [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)] melalui Wikimedia Commons)
Struktur Kimia Asid Amino Tyrosine (Sumber: Clavecin [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)] melalui Wikimedia Commons) Selepas penerangan awal, penyelidik lain seperti Warren de la Rue dan Hinterberger yang diperolehi daripada serangga kokoid dan protein tanduk, masing -masing. Pemisahannya dari hidrolisis protein lain dengan asid hidroklorik diterangkan pada tahun 1901 oleh Mörner.
Umumnya, asid amino ini diperolehi dalam mamalia berkat hidroksilasi fenilalanin, walaupun ia juga diserap dalam usus dari protein yang digunakan dengan makanan.
Tyrosine mempunyai pelbagai fungsi dalam tubuh manusia dan antara yang paling relevan adalah, mungkin, substrat untuk pengeluaran neurotransmitter dan hormon seperti adrenalin dan hormon tiroid.
[TOC]
Ciri -ciri
Tyrosine berat kira -kira 180 g/mol dan kumpulan rantaian r atau sampingannya mempunyai 10 -dissociation tetap 10.07. Kelimpahan relatifnya dalam protein sel tidak melebihi 4%, tetapi mempunyai pelbagai fungsi penting untuk fisiologi manusia.
Asid amino ini tergolong dalam kumpulan asid amino aromatik, di mana fenilalanin dan tryptophan juga. Ahli -ahli kumpulan ini mempunyai cincin aromatik dalam rantai r r atau sampingan mereka dan, biasanya, mereka adalah asid amino hidrofobik atau apolar.
Seperti tryptophan, tirosin menyerap cahaya ultraviolet dan merupakan salah satu sisa asid amino yang bertanggungjawab untuk penyerapan cahaya hingga 280 nm dari banyak protein, jadi berguna untuk penciriannya.
Ia dianggap sebagai asid amino "syarat" penting kerana biosintesisnya dalam manusia bergantung kepada fenilalanin, asid amino penting. Sekiranya badan memenuhi keperluan harian fenilalanin, tirosin dapat disintesis tanpa masalah dan bukan asid amino yang mengehadkan.
Walau bagaimanapun, jika diet kurang phenylalanine, badan bukan sahaja akan mempunyai ketidakseimbangan asid amino ini, tetapi juga tirosin. Ia juga penting untuk menunjukkan bahawa tindak balas sintesis tirosin dari fenilalanin tidak boleh diterbalikkan, jadi tirosin tidak dapat memenuhi keperluan selular fenilalanin.
Tyrosine juga tergolong dalam kumpulan asid amino dengan fungsi ganda dalam pengeluaran perantara metabolik glucogenic dan ketogenik, yang mengambil bahagian dalam sintesis glukosa untuk otak dan dalam pembentukan badan keton di hati.
Struktur
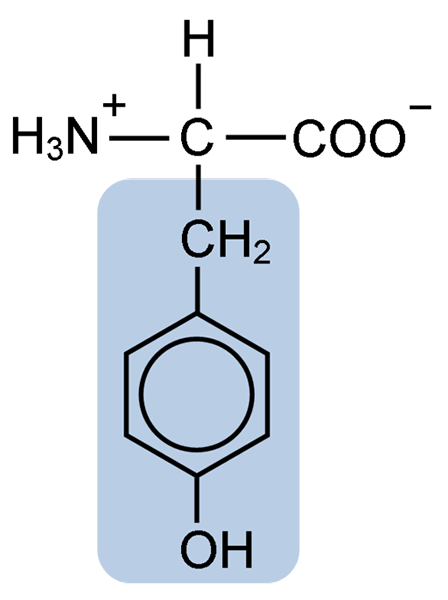
Seperti asid amino yang lain, tirosin, atau asid propionik β-parahydroxyphenyl-α-amino, ia adalah asid α-amino yang mempunyai atom karbon pusat, yang dipanggil karbon α dan yang kiral, kerana ia dikaitkan dengan dikaitkan dengan dikaitkan Empat atom atau molekul substituen yang berbeza.
Karbon quiral ini dikaitkan dengan dua kumpulan ciri asid amino: kumpulan amino (NH2) dan kumpulan karboksil (COOH). Dia juga berkongsi salah satu ikatannya dengan atom hidrogen dan baki ikatan diduduki oleh r atau rantaian sampingan setiap asid amino.
Dalam kes tirosin, kumpulan ini terdiri daripada cincin aromatik yang berkaitan dengan kumpulan hidroksil (OH), yang memberikan keupayaan untuk membentuk jambatan hidrogen dengan molekul lain dan yang memberikan ciri -ciri fungsi penting untuk enzim tertentu.
Ia boleh melayani anda: BaroreceptorsFungsi
Tyrosine adalah komponen asas banyak protein dengan kepelbagaian aktiviti dan fungsi biologi yang besar.
Pada manusia dan mamalia lain, asid amino ini dimanfaatkan dalam saraf dan tisu buah pinggang untuk sintesis dopamin, adrenalin dan norepinephrine, tiga catecholaminergik yang berkaitan dengan neurotransmitter yang berkaitan dengan kepentingan badan.
Ia juga penting untuk sintesis pelindung radiasi ultraviolet (UV) seperti melanin; beberapa analgesik seperti endorfin dan molekul antioksidan seperti vitamin E.
Begitu juga, asid amino ini berfungsi untuk sintesis tiramine, oktopamin dan hormon tiroid melalui organisasi yodium dalam sisa tirosin thyoglobulin.
Tiramine adalah molekul vasoaktif yang terdapat dalam tubuh manusia dan oktopamin adalah amina yang berkaitan dengan noreprenaline.
Semua fungsi tirosin ini mungkin terima kasih dari protein diet atau oleh hidroksilasi fenilalanin dengan hati sebagai sistem utama bekalan sistemik asid amino tersebut.
Fungsi dalam tumbuhan
Tyrosine dan beberapa perantara yang dihasilkan semasa biosintesis mereka memberi makan laluan biosintetik metabolit khusus dalam pertahanan, dalam tarikan pendebunga, dalam pengangkutan elektronik dan sokongan struktur.
Biosintesis
Dalam manusia, tirosin diperolehi dari diet atau disintesis dalam satu langkah oleh sel hati dari fenilalanin, asid amino penting, melalui tindak balas yang dikatalisis oleh kompleks enzimatik fenilalanin hidroksilase.
Kompleks ini mempunyai aktiviti oksigenase dan hanya terdapat di hati manusia atau mamalia lain. Reaksi sintesis tyrosine menunjukkan, maka, pemindahan atom oksigen ke kedudukan untuk cincin aromatik fenilalanin.
Reaksi ini berlaku pada masa yang sama bahawa molekul air dibentuk kerana pengurangan atom oksigen molekul yang lain dan kuasa pengurangan disumbangkan secara langsung oleh NADPH yang konjugasi dengan molekul tetrahydropterine, yang sama dengan asid folik.
Biosintesis dalam tumbuhan
Dalam tumbuhan, tirosin disintesis daripada Novo Hiliran laluan "shikimato", yang memberi makan laluan biosintetik lain asid amino aromatik lain seperti phenylalanine dan tryptophan.
Dalam organisma ini, sintesis didasarkan pada sebatian yang dikenali sebagai "corismato", yang merupakan produk akhir dari laluan shikimato dan, sebagai tambahan, prekursor umum untuk semua asid amino aromatik, vitamin dan hormon tumbuhan tertentu.
Corismate diubah menjadi pendahuluan oleh tindakan pemangkin enzim mutasa corismate dan ini adalah langkah pertama yang "komited" dalam sintesis tirosin dan fenilalanin dalam tumbuhan.
Predeneate ditukar menjadi tirosin oleh decarboxylation oksidatif dan transaminasi, yang boleh berlaku dalam sebarang urutan.
Di salah satu laluan biosintetik, langkah-langkah ini boleh dipangkin oleh enzim tertentu yang dikenali sebagai dehidrogenase (PDH) prefenat (PDH) (yang menukarkan kata pengantar kepada 4-hydroxyphenylpyphenylpyruvate (HPP) masing -masing.
Satu lagi jalan sintesis tirosin dari pendahuluan membayangkan transaminasi predeneate kepada asid amino bukan proteinogenik yang dipanggil L-arogenat, dikatalisis oleh enzim aminotransferase preenate.
L-arogenat kemudiannya tertakluk kepada decarboxylation oksidatif untuk membentuk tiroksin, tindak balas yang diarahkan oleh enzim tyrosine arogenate spesifik dehidrogenase, juga dikenali sebagai ADH.
Tumbuhan secara sengaja menggunakan laluan arenate, sementara kebanyakan mikrob mensintesis tirosin dari HPP yang diperoleh dari predenesate.
Peraturan
Seperti yang berlaku untuk kebanyakan laluan biosintetik asid amino, tumbuh -tumbuhan mempunyai sistem yang ketat peraturan sintesis asid amino aromatik, termasuk tirosin.
Boleh melayani anda: raksasa yang lazat: ciri, habitat, penjagaan, sifatDalam organisma ini, peraturan berlaku di banyak peringkat, kerana mekanisme yang mengawal laluan shikimato juga mengawal pengeluaran tirosin, laluan yang mana terdapat juga mekanisme peraturan mereka sendiri.
Walau bagaimanapun, keperluan tirosin dan, oleh itu, ketegaran dalam peraturan biosintesis mereka, khusus untuk setiap spesies tumbuhan.
Degradasi
Degradasi atau katabolisme tirosin mengakibatkan pembentukan fumarate dan acetoacetate. Langkah pertama laluan ini terdiri daripada penukaran asid amino menjadi 4-hydroxyphenylpypate oleh enzim sitosolik yang dikenali sebagai aminotransferase tyrosine.
Asid amino ini juga boleh ditransmisikan dalam mitokondria hepatosit oleh enzim aspartat aminotransferase, walaupun enzim ini tidak begitu penting dalam keadaan fisiologi biasa.
Melalui kemerosotan tirosin, succinyl-acetoacetate boleh berlaku, yang boleh decarboxylated ke succinyl-acetate. Succinyl-acetate adalah inhibitor enzim yang paling kuat yang bertanggungjawab untuk sintesis kumpulan hemo, dehidratase asid asid 5-aminolevulin.
Sintesis adrenalin dan norepinephrine
Seperti yang disebutkan, tirosin adalah salah satu substrat utama untuk sintesis dua neurotransmiter yang sangat penting untuk tubuh manusia: adrenalin dan norepinephrine.
Ini pada mulanya digunakan oleh enzim yang dikenali sebagai hydroxylase tyrosine, yang mampu menambahkan kumpulan hidroksil tambahan ke cincin aromatik kumpulan Ri tyrosine R, yang membentuk sebatian yang dikenali sebagai DPA.
DOPA menimbulkan dopamin apabila ia diproses secara enzim dengan enzim dopboxilas.
Dopamin kemudiannya diubah menjadi noreprenaline oleh tindakan β -oxidase dopamine enzim, yang memangkinkan penambahan kumpulan hidroksil kepada -ch yang merupakan sebahagian daripada kumpulan R tirosin dan yang bekerja sebagai "jambatan" antara cincin aromatik dan karbon α.
Adrenalin berasal dari norepinephrine dengan tindakan phenythanolamine N-methyltransferase, yang bertanggungjawab untuk pemindahan yang bergantung kepada S-adenosil-metionin kumpulan metil (-CH3) kepada kumpulan amino percuma norepinephrine.
Makanan yang kaya dengan tirosin
Seperti yang disebutkan di atas, tirosin adalah asid amino yang penting, kerana ia disintesis dalam tubuh manusia dengan hidroksilasi phenylalanine, asid amino penting.
Oleh itu, jika pengambilan fenilalanin meliputi tuntutan badan, tirosin bukanlah faktor yang mengehadkan untuk fungsi normal sel. Tyrosine, bagaimanapun, juga diperoleh dari protein yang dimakan dengan makanan harian.
Sesetengah kajian melaporkan bahawa pengambilan harian minimum kedua -dua tirosin dan fenilalanin mestilah antara 25 dan 30 mg per kilogram berat, jadi orang biasa harus mengambil lebih kurang 875 mg tirosin setiap hari.
Makanan dengan kandungan tirosin yang lebih tinggi adalah keju dan kacang soya. Antaranya juga daging lembu, kambing, daging babi, ayam dan ikan.
Beberapa biji dan kacang seperti kacang juga memberikan sumbangan penting dari asid amino ini, serta telur, produk tenusu, bijirin dan bijirin.
Faedah pengambilan anda
Tyrosine biasanya digunakan dalam bentuk makanan tambahan atau pemakanan, khususnya untuk rawatan patologi yang dikenali sebagai phenylcetonuria, yang dialami oleh pesakit yang tidak dapat memproses fenilalanin dengan betul dan, oleh itu, tidak menghasilkan tirosin.
Ia dapat melayani anda: fungsi hubunganDianggap bahawa peningkatan jumlah tyrosine yang digunakan setiap hari dapat meningkatkan fungsi kognitif yang berkaitan dengan pembelajaran, ingatan dan keadaan berjaga -jaga dalam keadaan tekanan, kerana katabolismenya berkaitan dengan sintesis neurotransmiter adrenalin dan norepinenal.
Sebilangan orang mengambil tablet tirosin untuk berjaga -jaga pada siang hari jika mereka kehilangan sejumlah besar waktu tidur.
Oleh kerana asid amino ini mengambil bahagian dalam pembentukan hormon tiroid, penggunaannya boleh memberi kesan positif terhadap peraturan metabolik sistemik.
Gangguan kekurangan
Albinisme dan Alcaptonuria adalah dua patologi yang berkaitan dengan metabolisme tirosin. Keadaan pertama berkaitan dengan sintesis melanin yang cacat dari tirosin dan yang kedua berkaitan dengan kecacatan dalam degradasi tirosin.
Albinisme dicirikan oleh kekurangan pigmentasi dalam kulit, iaitu, pesakit yang menderita mempunyai rambut putih dan kulit merah jambu, kerana melanin adalah pigmen yang bertanggungjawab untuk memberikan warna kepada struktur ini.
Patologi ini mempunyai kaitan dengan kekurangan dalam tyrosinase spesifik melanocytes, yang bertanggungjawab untuk menukar tirosin menjadi dopa-quinone, perantara dalam sintesis melanin.
Gejala alcaptonuria terbukti sebagai pigmentasi air kencing yang berlebihan (gelap) dan arthritis perkembangan lewat.
Patologi metabolik lain
Di samping itu, terdapat gangguan lain yang berkaitan dengan metabolisme tirosin, antaranya:
- Tyrosinemia keturunan jenis I: dicirikan oleh degenerasi hati yang progresif dan disfungsi buah pinggang
- Tyrosinemia keturunan jenis II atau sindrom Richner-Hanhart: yang terbukti sebagai keratitis dan lesi ampular di telapak tangan dan tapak kaki kaki
- Type Type Tyrosinemia: yang boleh menjadi asimtomatik atau hadir sebagai kelewatan mental
- "Hawkinsinuria": dicirikan oleh asidosis metabolik pada zaman kanak -kanak dan ketidakupayaan untuk berjaya dalam pertumbuhan
Terdapat juga kecacatan semula jadi yang lain dalam metabolisme metrosin yang berkaitan dengan kekurangan enzim yang bertanggungjawab terhadap kemerosotan mereka, seperti hidroksilase tyrosine, yang bertanggungjawab terhadap langkah pertama sintesis dopamin dari tirosin.
Rujukan
- Aders plimmer, r. (1908). Perlembagaan kimia protein. Saya pergi. London, UK: Longmans, Green, dan Co.
- Chakrapani, a., Gissen, ms., & McKiernan, p. (2012). Gangguan Metabolisme Tyrosine. Dalam Keinginan metabolik yang lahir: diagnosis dan rawatan (ms. 265-276).
- Kretchmer, n., Levine, s., McNamara, h., & Barnett, h. (1956). Aspek tertentu metabolisme tirosin pada golongan muda. Yo. Perkembangan sistem pengoksidaan tirosin di hati manusia. Jurnal Penyiasatan Klinikal, 35(10), 1089-1093.
- Du, b., Zannoni, v., Laster, l., & Seegmiller, e. (1958). Sifat kecacatan dalam metabolisme tirosin di Alkaptonuria. Jurnal Kimia Biologi, 230, 251-260.
- Murray, r., Bender, d., Botham, k., Kennelly, ms., Rodwell, v., & Weil, p. (2009). Biokimia Illustrated Harper (Edisi ke -28.). McGraw-Hill Medical.
- Nelson, d. L., & Cox, m. M. (2009). Prinsip Biokimia Lehninger. Edisi Omega (Edisi ke -5.).
- Schenck, c. Ke., & Maeda, h. Ke. (2018). Biosintesis Tyrosine, Metabolisme, dan Katabolisme di Tumbuh. Phytochemistry, 149, 82-102.
- Slominski, a., ZMijewski, m. Ke., & Paweley, J. (2012). L-Tyrosine dan L-dihydroxyphenylalanine sebagai pengawal selia seperti hormon fungsi melanocyte. Penyelidikan sel pigmen dan melanoma, 25(1), 14-27.
- Van de, g. (2018). Garis kesihatan. Diperoleh pada 16 September 2019, dari www.HealthLine.com
- MD Web. (n.d.). Diperoleh pada 15 September 2019, dari www.Webmd.com
- Whitbread, d. (2019). Data makanan saya. Diperoleh pada 15 September 2019, dari www.Myfooddata.com

