Sifat klorin oksida (iii), struktur, kegunaan
- 4612
- 835
- Kerry Schmitt
Dia klorin oksida (iii) Ia adalah sebatian bukan organik yang formula kimia adalah cl2Sama ada3. Sepadan dengan anhydride asid chloro, HCLO2. Ia adalah pepejal coklat gelap, sangat meletup walaupun pada suhu di bawah 0ºC, dan kurang dicirikan. Itulah sebabnya ia tertakluk kepada minat untuk kajian komputer.
Secara kimia ia adalah oksida kovalen, jadi terdapat ikatan cl-o dan molekul diskret Cl2Sama ada3 (gambar yang lebih rendah). Molekul ini mungkin membentuk dehidrasi HCLO2, atau dengan menundukkannya kepada suhu rendah. Perinciannya ialah ia mengurai menghasilkan Cl2, Sama ada2, atau lain -lain oksida klorin yang lebih stabil.
 Dicloro molekul trioksida. Sumber: Jynto [CC0].
Dicloro molekul trioksida. Sumber: Jynto [CC0]. Oleh kerana ikatan CL-O sedikit kutub, e-mel CL2Sama ada3 Ia mempunyai momen dipole kecil; Oleh itu, ia tidak membubarkan dengan baik di dalam air atau berinteraksi dengan pelarut kutub yang lain. Ketidakstabilannya sedemikian rupa sehingga tidak diketahui kegunaan komersial atau berpotensi (atau sebagai letupan kebolehgunaannya akan menjadi berdaya maju).
Sebab utama ketidakstabilannya mungkin disebabkan oleh ciri -ciri elektronik yang dikatakan Cl3+ (dengan mengandaikan watak ionik semata -mata). Malah, pengoksidaannya +1 dan +5 negeri adalah yang paling stabil apabila bentuk klorin sebatian dengan oksigen.
[TOC]
Sifat
Kerana penciriannya miskin dan tidak didokumenkan, tidak banyak yang mengatakan sifatnya kecuali perkara berikut:
-Ia mempunyai jisim molekul 118,903.
-Ia adalah coklat gelap yang padat; Walaupun anda boleh menyemai klorin gas, mengatakan wap hijau kekuningan.
-Ia tidak mempunyai titik mendidih dan gabungan, kerana pada 0ºC ia meletup (dan pada suhu yang lebih sejuk juga).
Boleh melayani anda: Dihydroxyacetone fosfat (DHAP): Ciri dan aplikasi-Kelarutannya di dalam air dianggarkan sekitar 3.42 g/100 ml, yang membuktikan bahawa ia adalah molekul kovalen yang rendah polaritas.
-Bertindak balas dengan air (sedikit yang larut) untuk menjadi HCLO2:
Cl2Sama ada3 + H2Atau 2hclo2
Struktur oksida klorin (iii)
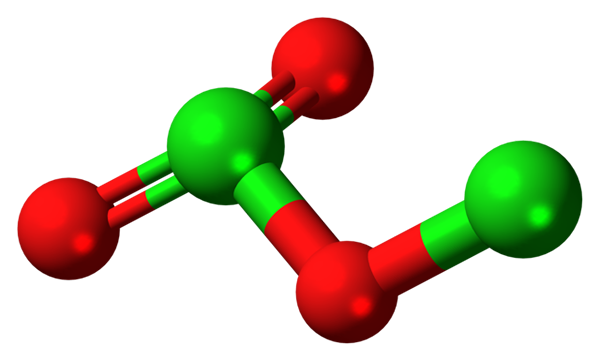
Dalam imej struktur molekul CL ditunjukkan2Sama ada3 Dengan model sfera dan bar. Walaupun nampaknya tidak mata kasar, implikasi tersirat dari hubungan dan pengaturan spatial mereka lebih rumit daripada yang muncul. Struktur ini sepadan dengan salah satu daripada banyak isomer yang mungkin untuk sebatian ini.
Sfera merah sesuai dengan atom oksigen, dan yang hijau ke atom klorin. Klorin di sebelah kiri membentangkan geometri piramid trigonal, dengan beberapa elektron bebas; Oleh itu, dapat diandaikan bahawa hibridisasi anda mestilah sp SP3. Atom oksigen bertindak sebagai jambatan antara dua kloros, cl-o-cl.
Isomer
Apakah isomer yang lain? Dalam teori sembilan dikira, yang mana empat adalah yang paling stabil (termasuk imej). Tiga yang lain akan mempunyai struktur seperti:
-Clclo3. Sangat serupa dengan yang dijelaskan, tetapi dengan pautan CL-CL.
-Clooocl (1). Di dalam isomer ini terdapat jambatan tiga oksigen yang memisahkan dua atom klorin (ingat geometri sudut H2Atau untuk menggambarkannya).
-Clooocl (2). Jambatan oksigen yang sama juga terdapat di dalam isomer ini, kecuali kedua -dua atom klorin dilepaskan di ruang angkasa; satu di hadapan yang lain, sementara di isomer sebelumnya mereka jauh.
Ia boleh melayani anda: AlquinosNomenclature
Namanya, klorin oksida (iii), sepadan dengan yang ditetapkan mengikut tatanama saham. Di sini diandaikan bahawa klorin mempunyai keadaan pengoksidaan +3; Tetapi itu tidak bermaksud bahawa3+ mungkin hadir. Ia adalah molekul, bukan rangkaian ion.
Nama lain yang mana CL juga dikenali2Sama ada3 Ia adalah dicloro trioksida, menurut tatanama sistematik.
Dan akhir. Nama ini disebabkan oleh hakikat bahawa, seperti yang telah dijelaskan, CL2Sama ada3 Ia berlaku apabila HCLO2 Ia memendekkan air.
Aplikasi
Kerana ia adalah oksida klorin, penggunaan paling segera yang boleh difikirkan untuk CL2Sama ada3 Ia seperti ejen pengoksidaan, mampu meneutralkan kekotoran dan mikrob organik. Walau bagaimanapun, ia sangat tidak stabil, sebagai tambahan kepada bahan letupan, sehingga untuk tujuan ini dianggap berguna.
Pasti tidak ada maklumat walaupun CL akan berkelakuan2Sama ada3 di bawah tekanan besar (jika ia tidak meletup dalam proses). Dalam keadaan biasa, nampaknya tidak lebih daripada perantara yang agak stabil dan berbeza di antara lain oksida klorin yang lebih stabil.
Walau bagaimanapun, secara komputasi, ia telah tertakluk kepada kajian untuk menentukan mekanisme oleh radikal bebas yang melibatkan beberapa spesies klorin dan oksigen.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2019). Diklorin trioksida. Diperoleh dari: dalam.Wikipedia.org
- Beri dia l. Perry. (2011). Buku panduan sebatian bukan organik. (Edisi kedua). CRC Press Taylor & Francis Group.
- Richard c. Ropp. (2013). Ensiklopedia sebatian Bumi Alkali. Elsevier.
- Kim k. H., Han dan.K., dan membaca dan. S. (1999). Kesan set asas pada kestabilan isomer Cl2O3 menggunakan kaedah B3P86 dan B3LYP teori fungsi ketumpatan. Jurnal Struktur Molekul Theochem 460 (1-3): 19-25.

