Natrium Karbonat (Na2CO3)
- 2329
- 529
- Anthony Breitenberg
Kami menerangkan apa natrium karbonat, sifat fizikal dan kimia, struktur dan aplikasinya
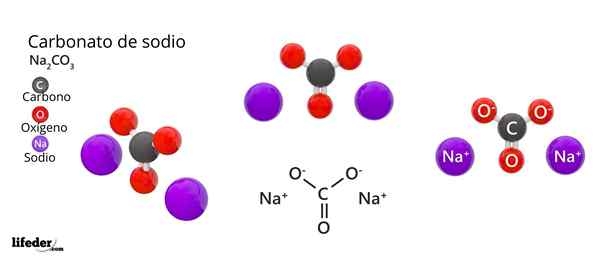
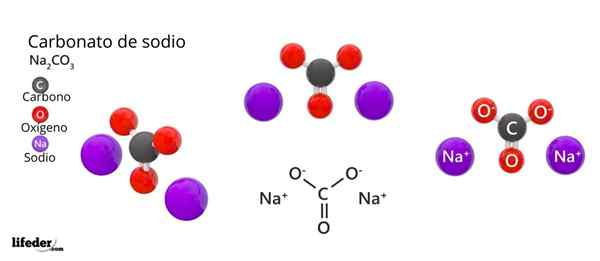 Struktur dan formula natrium karbonat
Struktur dan formula natrium karbonat Apa itu Natrium Karbonat?
Dia Natrium karbonat (NA2Co3) Ia adalah garam tak organik, logam alkali dan asid karbonik. Dia juga dikenali di seluruh dunia sebagai Sosa Ash. Tasik dan aktiviti gunung berapi memperkaya tanah natrium, di mana tumbuh -tumbuhan dipelihara; Kemudian, selepas api, tumbuh -tumbuhan ini menyebarkan abu karbonat.
Bagaimana garam natrium logam ini timbul? Natrium tulen mempunyai konfigurasi Valencia [NE] 3S1. Elektron orbital 3s1 Ia mudah dipisahkan oleh unsur -unsur alam semula jadi (seperti sulfur, oksigen, klorin, fluorin, dll.), membentuk sebatian mineral di mana ion stabil na mengambil bahagian+.
Na+ Ia disertai oleh spesies ionik lain dalam pepejal ini; Daripada jumlah ini, natrium karbonat hanya satu lagi yang hadir. Sejak itu ia telah digunakan dalam semua tamadun sepanjang masa. Tamadun ini mendapati dalam sifat debu kelabu yang bermanfaat untuk rumah dan orang mereka.
Ciri -ciri ini menandakan kegunaan mereka, yang hari ini mengekalkan aspek tradisional masa lalu, dan yang lain menampung keperluan semasa.
Natrium Karbonat sangat banyak, dan mungkin juga di wilayah lain di luar planet Bumi, seperti beberapa bulan sistem suria.
Formula
Formula kimia natrium karbonat adalah na2Co3. Bagaimana ia ditafsirkan? Itu bermaksud bahawa, dalam pepejal kristal, untuk setiap co -ion32- Terdapat dua ion na+.
Struktur natrium karbonat
Di bahagian atas, struktur NA diwakili2Co3 Anhydride (juga dikenali sebagai Sosa Calcinada). Sfera ungu sesuai dengan ion na+, manakala hitam dan merah ke ion co32-.
Ion karbonat mempunyai struktur trigonal rata, dengan atom oksigen di simpang mereka.
Ia boleh melayani anda: asid sinam: struktur, sifat, mendapatkan, menggunakanImej memberikan panorama yang dilihat dari pesawat yang lebih tinggi. Ion na+ Mereka dikelilingi oleh enam atom oksigen, dari co -ion32-. Iaitu, di NA2Co3 Anhydride Natrium memenuhi geometri koordinasi octahedral (ia terkunci di tengah octahedron).
Walau bagaimanapun, struktur ini juga dapat menempatkan molekul air, berinteraksi dengan jambatan hidrogen dengan simpang segitiga.
Malah, Na menghidrat2Co3 (NA2Co3· 10h2Atau, na2Co3· 7h2Atau, na2Co3· H2Atau, dan yang lain) adalah lebih banyak daripada garam anhidrid.
Thermonatrite (na2Co3· H2O), natron (na2Co3· 10h2O) dan trona (na3(HCO3) (Co3) · 2h2Atau merupakan sumber semula jadi natrium karbonat, terutama mineral trona, yang diwakili dalam imej pertama.
Penggunaan/aplikasi natrium karbonat
Natrium karbonat memenuhi pelbagai fungsi dalam orang, isi rumah dan industri, di antara fungsi -fungsi ini yang berikut menonjol:
- Natrium Karbonat digunakan dalam pelbagai produk pembersihan. Ini disebabkan oleh kapasiti pembasmi kuman, kuasa untuk membubarkan lemak dan harta mereka untuk melembutkan air. Ia adalah sebahagian daripada detergen yang digunakan dalam laundri, mesin basuh pinggan mangkuk automatik, kaca bersih, bintik -bintik, peluntur, dll.
- Disinfektan karbonat boleh digunakan pada permukaan keras yang tidak berat, seperti lantai, dinding, porselin dan tab mandi, kecuali pengecualian Gentian kaca dan aluminium, yang boleh digores olehnya.
- Ia digunakan dalam beberapa makanan untuk mengelakkan cawan yang mungkin berlaku dalam hal ini.
- Ia terdapat dalam beberapa produk penjagaan diri, seperti mandi gelembung, pasta gigi dan sabun.
- Ia digunakan dalam industri kaca kerana keupayaannya untuk memecahkan silikat.
- Ia digunakan dalam penyelenggaraan kolam renang, di mana ia memenuhi fungsi disinfektan dan pengawalseliaan pH.
- Pada manusia secara terapeutik digunakan dalam rawatan keasidan dan dermatitis.
- Dalam Perubatan Veterinar Ia digunakan dalam rawatan cacing dan pembersihan kulit.
Sintesis natrium karbonat

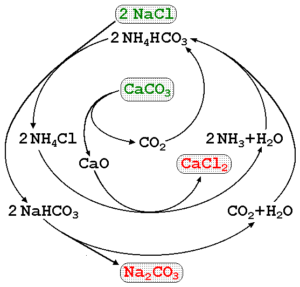
Natrium Karbonat boleh dihasilkan menggunakan air garam laut dan batu kapur (Caco3) Dalam proses solvay. Dalam imej unggul, gambarajah proses digambarkan menunjukkan laluan pengeluaran, serta reagen, perantara dan produk. Reagen ditulis dengan huruf hijau, dan produk dengan huruf merah.
Pemantauan tindak balas ini boleh menjadi agak rumit, tetapi persamaan global yang menunjukkan hanya reagen dan produk adalah:
2nacl (aq) + Caco3(s) na2Co3(s) + CACL2(Ac)
Caco3 Ia mempunyai struktur kristal yang sangat stabil, jadi ia sentiasa menuntut banyak tenaga untuk menguraikannya2. Di samping itu, proses ini menjana jumlah besar CACL2 (kalsium klorida) dan kekotoran lain, yang pelepasannya mempengaruhi kualiti air dan alam sekitar.
Terdapat juga kaedah pengeluaran natrium karbonat lain dalam bidang perindustrian, seperti proses Hou dan LeBlanc.
Hari ini diperoleh dari mineral semulajadinya adalah mampan, Trona menjadi yang paling banyak.
Sebaliknya, kaedah paling tradisional terdiri daripada penanaman dan pembakaran tumbuhan dan alga yang kaya dengan natrium. Kemudian, abu dimandikan dengan air dan tertakluk kepada pemanasan sehingga produk. Dari sini muncul abu terkenal Sosa.
Sifat natrium karbonat
Na2Co3 Ia adalah pepejal putih hygroscopic, tandas, dengan berat molekul 106 g/mol dan ketumpatan 2.54 g/ml pada 25 ° C.
Ciri -cirinya berubah sebagai molekul air dimasukkan ke dalam struktur kristalnya. Oleh kerana air dapat membentuk jambatan hidrogen dan "ruang terbuka" ion di antara mereka, jumlah kaca meningkat dan ketumpatan hidrat berkurangan. Contohnya, untuk NA2Co3· 10h2Atau, ketumpatannya ialah 1.46 g/ml.
Boleh melayani anda: Reaksi boleh diterbalikkan: Ciri dan contohNa2Co3 mencairkan pada 851 ºC, menguraikan mengikut persamaan berikut:
Na2Co3(s) => na2Atau (s) + co2(g)
Sekali lagi, walaupun ada ion32- dan na+ Mereka berbeza dalam saiz, interaksi elektrostatik mereka sangat berkesan dan mengekalkan rangkaian kristal yang stabil.
Molekul air "menghalang" interaksi ini dan, akibatnya, hidrat lebih mudah terdedah kepada penguraian daripada anhidrida.
Ia adalah garam asas; iaitu, dibubarkan dalam air menghasilkan penyelesaian dengan pH lebih besar daripada 7. Ini disebabkan oleh hidrolisis CO32-, yang reaksi melepaskan oh- di tengah:
Co32-(Ac) + h2Atau (l) HCO3-(Ac) + oh-(Ac)
Ia sangat larut dalam pelarut air dan kutub, seperti gliserol, gliserin, aseton, asetat, dan ammonia cecair.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. Dalam elemen Kumpulan 1. (Edisi Keempat., p. 265). MC Graw Hill.
- Scifun.org. (2018). Natrium hidrogen karbonat & natrium karbonat. Pulih dari Scifun.org
- Wikipedia. (2018). Natrium karbonat. Diambil dari.Wikipedia.org
- Pubchem. (2018). Natrium karbonat. Pulih dari pubchem.NCBI.NLM.NIH.Gov
- Ciner Resources Corporation. (2018). Soda Ash. Ciner pulih.kita.com
- Peltier k. (3 Julai 2018). Semua yang anda perlu tahu mengenai natrium karbonit. Diperoleh pada 8 April 2018, dari: Thespruce.com
- Industri bersih. (2018). Natrium Karbonat - Kegunaan Natrium Karbonat. Diperoleh pada 8 April 2018, dari: Sains.Jank.org

