Sejarah fluoror, sifat, struktur, memperoleh, risiko, kegunaan
- 2843
- 196
- Horace Gulgowski
Dia Fluorin Ia adalah elemen kimia yang diwakili dengan simbol f dan kumpulan kepala 17, yang mana halogen itu tergolong. Ia dibezakan di atas unsur -unsur lain dalam jadual berkala, kerana menjadi yang paling reaktif dan elektronegatif; Reacts hampir dengan semua atom, jadi ia membentuk garam yang tidak terhitung dan sebatian organisasi.
Dalam keadaan biasa ia adalah gas kuning pucat, yang boleh dikelirukan dengan hijau kekuningan. Dalam keadaan cair, ditunjukkan dalam imej yang lebih rendah, warna kuningnya semakin sedikit, yang hilang sepenuhnya apabila ia menguatkan di titik pembekuannya.
 Fluorin cecair dalam tiub ujian. Sumber: Fulvio314 [CC BY-SA 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0)]
Fluorin cecair dalam tiub ujian. Sumber: Fulvio314 [CC BY-SA 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0)] Ia adalah kereaktifan sedemikian, walaupun tidak menentu gasnya, yang masih ditangkap di kerak bumi; terutamanya dalam bentuk mineral fluorit, yang dikenali dengan kristal violetnya. Begitu juga, kereaktifannya menjadikannya bahan yang berpotensi berbahaya; bertindak balas dengan kuat dengan semua yang menyentuh dan membakar api.
Walau bagaimanapun, banyak produk yang diperolehnya tidak berbahaya dan bermanfaat, bergantung pada aplikasi mereka. Sebagai contoh, penggunaan fluorida yang paling popular, ditambah dalam bentuk ionik atau mineralnya (seperti garam fluorida), terdiri daripada penyediaan pasta gigi dengan fluorida, yang membantu melindungi enamel pergigian.
Fluorin membentangkan keanehan bahawa bilangan yang tinggi atau keadaan pengoksidaan dapat menstabilkan untuk banyak elemen lain. Semakin besar bilangan atom fluorin, lebih banyak reaktif sebatian akan (kecuali jika ia adalah polimer). Begitu juga, kesannya dengan matriks molekul akan meningkat; untuk lebih baik atau lebih teruk.
[TOC]
Sejarah
Penggunaan fluorit
Pada tahun 1530, mineralogi Jerman Georgius Agricola mendapati bahawa mineral fluorspar boleh digunakan dalam pembersihan logam. Fluorspar adalah nama lain untuk fluorit, mineral fluorin yang terdiri daripada kalsium fluorida (CAF2).
Unsur fluorin tidak ditemui pada masa itu dan "fluoir" dalam fluorit datang dari perkataan Latin "fluere" yang bermaksud "aliran"; Oleh kerana ini adalah apa yang dilakukan oleh fluorspar atau fluorit dengan logam: ia membantu mereka meninggalkan sampel.
Penyediaan asid fluorik
Pada tahun 1764, Andreas Sigismud Margraff berjaya. Pulangan kaca cair oleh tindakan asid, jadi kaca digantikan oleh logam.
Ia juga dikaitkan dengan Carl Scheele pada tahun 1771, penyediaan asid dengan kaedah yang sama diikuti oleh Margraff. Pada tahun 1809, saintis Perancis Andre-Marie Ampere mencadangkan bahawa asid fluorik atau fluorik adalah sebatian yang dibentuk oleh hidrogen dan elemen baru yang serupa dengan klorin.
Para saintis cuba mengasingkan fluorin melalui penggunaan asid fluorhorical untuk masa yang lama; Tetapi bahayanya membuat kemajuan dalam hal ini.
Humphry Davy, Joseph Louis Gay-Lussac dan Jacques Thénard mengalami kesakitan yang kuat apabila menghirup fluorida hidrogen (asid fluorida tanpa air dan dalam bentuk gas)). Dalam keadaan yang sama, saintis Paulin Louyet dan Jerome Nickles meninggal dunia akibat keracunan.
Edmond Fréme, penyelidik Perancis, cuba mencipta asid fluorhoride kering untuk mengelakkan ketoksikan fluorida hidrogen dengan pengasidan kalium bifluoride (KHF2), Tetapi semasa elektrolisis tidak ada pengaliran arus elektrik.
Pengasingan
Pada tahun 1860, ahli kimia Inggeris George Gore mencuba. Walau bagaimanapun, terdapat letupan dengan menggabungkan semula hidrogen dengan fluorida. Gore menyebarkan letupan ke kebocoran oksigen.
Pada tahun 1886, ahli kimia Perancis Henri Moisson berjaya mengasingkan fluorida buat kali pertama. Sebelum ini, kerja Moisson terganggu empat kali disebabkan oleh keracunan serius dengan fluorida hidrogen, sambil cuba penebat elemen.
Moisson adalah pelajar frony dan berdasarkan eksperimennya untuk mengasingkan fluorida. Moisson yang digunakan dalam elektrolisis campuran kalium fluorida dan asid fluorhorhoric. Penyelesaian yang dihasilkan LED elektrik dan gas fluorin yang terkumpul dalam anod; iaitu, dalam elektrod yang dimuatkan secara positif.
Moisson menggunakan peralatan kakisan, di mana elektrod diperbuat daripada aloi platinum dan iridium. Dalam elektrolisis ia menggunakan bekas platinum dan menyejukkan larutan elektrolitik pada suhu -23 ºF (-31 ºC).
Akhirnya, pada 26 Jun 1886, Henri Moisson berjaya mengasingkan Fluoride, kerja yang membolehkannya memenangi Hadiah Nobel pada tahun 1906.
Minat dalam fluorida
Untuk sementara waktu minat penyiasatan dengan Fluoride hilang. Walau bagaimanapun, perkembangan projek Manhattan untuk pengeluaran bom atom.
Syarikat Amerika DuPont dibangunkan, antara 1930 dan 1940, produk fluorinated seperti chlorofluorocarbonates (freon-12), digunakan sebagai penyejuk; dan plastik polythetrafluoroethylene, yang paling terkenal dengan nama Teflon. Ini menghasilkan peningkatan pengeluaran dan penggunaan fluorin.
Pada tahun 1986, pada persidangan selama satu abad pengasingan fluorin, ahli kimia Amerika Karl atau. Christe membentangkan kaedah kimia untuk penyediaan fluorida dengan tindak balas antara k2Mnf6 dan SBF5.
Boleh melayani anda: alkohol polyvinylSifat fizikal dan kimia
Penampilan
Fluorin adalah gas kuning pucat. Dalam keadaan cair ia berwarna kuning terang. Sementara itu, pepejal boleh menjadi legap (alpha) atau telus (beta).
Nombor atom (z)
9.
Berat atom
18,998 u.
Takat lebur
-219.67 ºC.
Takat didih
-188.11 ºC.
Ketumpatan
Pada suhu bilik: 1,696 g/l.
Di titik lebur (cecair): 1,505 g/ml.
Haba pengewapan
6.51 kJ/mol.
Kapasiti kalori molar
31 j/(mol · k).
Tekanan wap
Pada suhu 58 K mempunyai tekanan wap 986.92 ATM.
Kekonduksian terma
0.0277 w/(m · k)
Urutan magnet
Diamagnetic
Bau
Bau ciri pedas dan menembusi, dapat dikesan walaupun pada 20 ppb.
Nombor pengoksidaan
-1, yang sepadan dengan anion fluorida, f-.
Tenaga pengionan
-Pertama: 1.681 kJ/mol
-Kedua: 3.374 kJ/mol
-Ketiga: 6.147 kJ/mol
Elektronegativiti
3.98 pada skala Pauling.
Ia adalah elemen kimia dengan elektronegativiti terbesar; iaitu, ia mempunyai pertalian yang tinggi untuk elektron atom yang dihubungkan. Oleh sebab itu, atom fluorin menjana momen dipole besar di kawasan tertentu molekul.
Elektronegativiti beliau juga mempunyai kesan lain: atom yang dikaitkan dengannya kehilangan banyak ketumpatan elektronik sehingga mereka mula memperoleh beban positif; Ini adalah nombor pengoksidaan positif. Atom fluorin yang lebih banyak dalam sebatian, atom pusat akan mempunyai nombor pengoksidaan yang lebih positif.
Contohnya, di2 Oksigen mempunyai bilangan pengoksidaan +2 (atau2+F2-); Di uf6, Uranium mempunyai bilangan pengoksidaan +6 (u6+F6-); Perkara yang sama berlaku untuk sulfur di SF6 (S6+F6-); Dan akhirnya adalah AGF2, di mana perak bahkan mempunyai bilangan pengoksidaan +2, tidak biasa di dalamnya.
Oleh itu, unsur -unsur berjaya mengambil bahagian dengan nombor pengoksidaan yang paling positif apabila mereka membentuk sebatian dengan fluorida.
Ejen pengoksidaan
Fluorin adalah elemen pengoksidaan yang paling kuat, jadi tiada bahan yang mampu mengoksidakannya; Dan atas sebab ini, dia tidak bebas.
Reaktiviti
Fluorin dapat bergabung dengan semua elemen lain, kecuali dengan helium, neon dan argon. Ia juga tidak menyerang keluli manis atau tembaga pada suhu biasa. Bertindak balas dengan ganas dengan bahan organik, seperti getah, kayu dan kain.
Fluorida boleh bertindak balas dengan xenon gas mulia untuk membentuk oksida difluoruro yang kuat dari xenon, xef2. Ia juga bertindak balas dengan hidrogen untuk membentuk halida, fluorida hidrogen, HF. Sebaliknya, fluorida hidrogen dibubarkan di dalam air untuk menghasilkan asid fluorhorhoric yang terkenal (makan kaca).
Keasidan asid hidrasi, diklasifikasikan dalam peningkatan urutan adalah:
Hf < HCl < HBr < HI
Asid nitrik bertindak balas dengan fluorida untuk membentuk nitrat fluorin, FNO3. Sementara itu, asid hidroklorik bertindak balas dengan kuat dengan fluorida untuk membentuk HF,2 dan Clf3.
Struktur dan konfigurasi elektronik

Molekul diatomik
 Molekul fluorida yang diwakili dengan model pengisian ruang. Sumber: Gabriel Bolívar.
Molekul fluorida yang diwakili dengan model pengisian ruang. Sumber: Gabriel Bolívar. Atom fluorin dalam keadaan basalnya mempunyai tujuh elektron Valencia, yang berada di orbital 2s dan 2p mengikut konfigurasi elektronik:
[Dia] 2s2 2 p5
Teori Link Valencia (TEV) menetapkan bahawa dua atom fluorin, f, kovalen dikaitkan dengan dapat menyelesaikan oktet mereka di Valencia masing -masing.
Ini berlaku dengan cepat kerana ia hampir tidak mempunyai elektron untuk menjadi isolektronik kepada gas neon mulia; Dan atomnya sangat kecil, dengan beban nuklear yang sangat kuat yang mudah menuntut elektron alam sekitar.
Molekul f2 (Imej Superior), mempunyai pautan kovalen yang mudah, F-F. Walaupun kestabilannya berbanding dengan atom F percuma, ia adalah molekul yang sangat reaktif; Homonuklear, apolar, dan bersemangat untuk elektron. Itulah sebabnya fluorida, seperti f2, Ia adalah spesies yang sangat toksik dan berbahaya.
Kerana f2 Ia adalah apolar, interaksinya bergantung pada jisim molekulnya dan daya penyebaran London. Pada satu ketika, awan elektronik di sekitar kedua -dua atom F mesti berubah bentuk dan berasal dari dipole segera yang mendorong satu lagi dalam molekul jiran; Jadi mereka perlahan dan lemah.
Cecair dan pepejal
Molekul f2 Ia sangat kecil dan merebak di angkasa dengan kelajuan relatif. Dalam fasa gasnya, ia mempamerkan warna kuning pucat (yang boleh dikelirukan dengan hijau kapur). Apabila suhu jatuh ke -188 ºC, daya penyebaran menjadi lebih berkesan dan menjadikan molekul f2 cukup perpaduan untuk menentukan cecair.
Fluorin cecair (imej pertama), kelihatan lebih kuning daripada gas masing -masing. Di dalamnya, molekul f2 Mereka lebih dekat dan berinteraksi dengan cahaya dalam tahap yang lebih tinggi. Menariknya, apabila kaca padu yang terdistorsi terbentuk dari fluorin hingga -220 ºC, warna pudar dan kekal pepejal telus.
Boleh melayani anda: Alkanes bercabangSekarang bahawa molekul m2 Mereka begitu dekat (tetapi tanpa putaran molekul mereka berhenti), nampaknya elektron mereka mendapat kestabilan dan, oleh itu, lompatan elektronik mereka terlalu besar untuk cahaya bahkan berinteraksi dengan kaca.
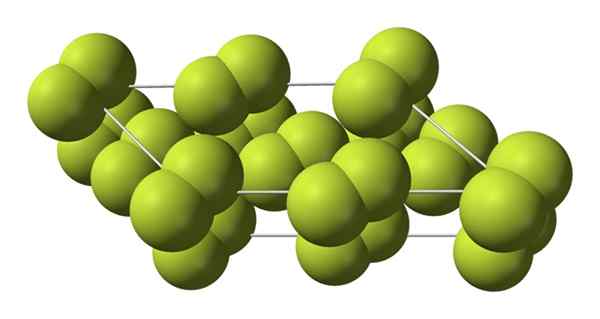
Fasa kristal
Kristal padu ini sepadan dengan fasa β (ia bukan alotropik kerana ia tetap sama f yang sama2). Apabila suhu jatuh lebih banyak, sehingga -228 ºC, fluorin pepejal mengalami peralihan fasa; Kaca padu berubah menjadi monoklinik, fasa α:
 Struktur kristal fasa alfa fluorin. Sumber: Benjah-bmm27 [domain awam].
Struktur kristal fasa alfa fluorin. Sumber: Benjah-bmm27 [domain awam]. Tidak seperti β-F2, Α-f2 adalah legap dan sukar. Mungkin kerana molekul m2 Mereka tidak lagi mempunyai kebebasan untuk berputar dalam kedudukan tetap mereka dalam kristal monoklinik; di mana mereka berinteraksi dengan tahap yang lebih tinggi dengan cahaya, tetapi tanpa merangsang elektron mereka (yang akan menerangkan kelegapan mereka secara dangkal).
Struktur kristal α-f2 Sukar untuk belajar melalui kaedah difraksi x -ray konvensional. Ini kerana peralihan dari fasa β hingga α sangat eksotermik; Jadi kristal praktikal dieksploitasi, sambil berinteraksi sedikit dengan radiasi.
Mereka menghabiskan masa kira-kira lima puluh tahun sebelum saintis Jerman (Florian Kraus dan kolaborator), sepenuhnya menguraikan struktur α-F2 dengan ketepatan yang lebih besar terima kasih kepada teknik difraksi neutron.
Di mana dan dapatkan
Fluorin menduduki elemen ke -24 yang paling biasa di alam semesta. Walau bagaimanapun, di bumi secara besar -besaran 13vo elemen, dengan kepekatan 950 ppm di kerak bumi, dan kepekatan 1.3 ppm dalam air laut.
Tanah mempunyai kepekatan fluorin antara 150 dan 400 ppm, dan di beberapa tanah kepekatan dapat mencapai 1.000 ppm. Di udara atmosfera ia terdapat dalam kepekatan 0.6 ppb; Tetapi ia telah didaftarkan di beberapa bandar sehingga 50 ppb.
Fluorin diperoleh terutamanya dari tiga mineral: fluorit atau fluorospar (kopi2), Fluoroapatita [ca5(PO4)3F] dan creole (na3Alf6).
Pemprosesan fluorit
Setelah mengumpul batu dengan mineral fluorit, ini tertakluk kepada penghancuran primer dan sekunder. Dengan penghancuran sekunder mendapatkan serpihan batu yang sangat kecil.
Kemudian, serpihan batu dibawa ke kilang bola untuk pengurangan habuk. Air dan reagen ditambah untuk membentuk pasta, yang diletakkan di dalam tangki pengapungan. Ia disuntik dengan tekanan untuk membentuk gelembung, dan oleh itu fluorit berakhir di permukaan berair.
Silicates dan karbonat adalah sedimen manakala fluorit dikumpulkan dan membawa kepada pengeringan ketuhar.
Sebaik sahaja fluorit diperoleh, ia bertindak balas dengan asid sulfurik untuk menghasilkan fluorida hidrogen:
Caf2 + H2SW4 => 2 hf +kes4
Elektrolisis fluorida hidrogen
Dalam pengeluaran fluorida, beberapa pengubahsuaian diikuti, dengan kaedah yang digunakan oleh Moisson pada tahun 1886.
Elektrolisis campuran kalium fluorida cair dan asid fluohidrik dibuat, dengan jejari molar 1: 2.0 hingga 1: 2.2. Suhu garam lebur ialah 70 - 130 ºC.
Katod terdiri daripada aloi monet atau keluli, dan anod adalah arang batu. Proses pengeluaran fluorin semasa elektrolisis boleh dijangkau seperti berikut:
2hf => h2 + F2
Air digunakan untuk menyejukkan ruang elektrolisis, tetapi suhu mesti berada di atas titik lebur elektrolit untuk mengelakkan pemejalan. Hidrogen yang dihasilkan dalam elektrolisis dikumpulkan dalam katod, manakala fluorida dalam anod.
Isotop
Fluorida mempunyai 18 isotop, menjadi 19F Satu -satunya isotop stabil dengan kelimpahan 100%. Dia 18F mempunyai separuh hayat 109.77 minit dan isotop radioaktif fluorin dengan separuh hayat yang paling besar. Dia 18F Ia digunakan sebagai sumber positron.
Kertas Biologi
Tiada aktiviti metabolik fluorin dalam mamalia atau tumbuhan atas diketahui. Walau bagaimanapun, beberapa tumbuhan dan span laut mensintesis monofluroacetate, sebatian beracun, yang digunakan sebagai perlindungan untuk mengelakkan kemusnahan.
Risiko
Penggunaan fluorin yang berlebihan telah dikaitkan dengan fluorosis tulang pada orang dewasa dan fluorosis pergigian pada kanak -kanak, serta dengan perubahan dalam fungsi buah pinggang. Atas sebab ini, Perkhidmatan Kesihatan Awam Amerika Syarikat (PHS) mencadangkan bahawa kepekatan fluorida dalam air minuman tidak boleh lebih besar daripada 0.7 mg/l.
Sementara itu, Agensi Perlindungan Enviromental AS (EPA) menegaskan bahawa kepekatan fluorida dalam air minuman tidak boleh lebih besar daripada 4mg/L, untuk mengelakkan fluorosis rangka, di mana fluorida berkumpul di tulang. Ini boleh menyebabkan kelemahan tulang dan patah tulang.
Fluorin telah dikaitkan dengan kerosakan kelenjar parathyroid, dengan penurunan kalsium dalam struktur tulang dan kepekatan kalsium yang tinggi dalam plasma.
Ia boleh melayani anda: perkara hidup: konsep, ciri dan contohAntara perubahan yang dikaitkan dengan fluorin yang berlebihan adalah berikut: fluorosis pergigian, fluorosis rangka dan kerosakan pada kelenjar paratiroid.
Fluorosis pergigian
Fluorosis pergigian dibentangkan dengan jalur kecil atau motosikal di enamel gigi. Kanak -kanak di bawah 6 tidak boleh menggunakan cuci mulut yang mengandungi fluorida.
Fluorosis rangka
Dalam fluorosis rangka, kesakitan dan kerosakan kerosakan boleh didiagnosis, serta di sendi. Tulang boleh mengeras dan kehilangan keanjalan, yang meningkatkan risiko patah tulang.
Aplikasi
Ubat gigi
 Beberapa garam tak organik fluorida digunakan sebagai bahan tambahan dalam perumusan pasta gigi, yang menunjukkan bahawa mereka membantu melindungi enamel pergigian. Sumber: Pxhere.
Beberapa garam tak organik fluorida digunakan sebagai bahan tambahan dalam perumusan pasta gigi, yang menunjukkan bahawa mereka membantu melindungi enamel pergigian. Sumber: Pxhere. Kami mulakan dengan bahagian kegunaan fluoride dengan yang paling terkenal: untuk berfungsi sebagai komponen dari banyak pasta pergigian. Ini bukan satu -satunya penggunaan di mana perbezaan antara molekulnya dapat dilihat2, sangat beracun dan berbahaya, dan anion f-, yang bergantung kepada persekitarannya boleh bermanfaat (walaupun kadang -kadang tidak).
Apabila kita makan makanan, terutamanya gula -gula, bakteria merendahkannya dengan meningkatkan keasidan air liur kita. Kemudian, ada titik di mana pH sudah cukup untuk merendahkan dan demineralize enamel pergigian; Hydroxiapatite datang "turun".
Walau bagaimanapun, dalam proses ini ion f- berinteraksi dengan ca2+ untuk membentuk matriks fluorapatite; lebih stabil dan berkekalan daripada hidroksiapatit. Atau sekurang -kurangnya, ini adalah mekanisme yang dicadangkan untuk menjelaskan tindakan anion fluorida pada gigi. Ia mungkin lebih kompleks dan terdapat hidroksiapatit-fluorapatite bergantung pada pH.
Anion ini f- Mereka boleh didapati dalam PAPA pergigian dalam garam; seperti: naf, snf2 (Stine Fluoride yang terkenal) dan Napof. Walau bagaimanapun, kepekatan f- Ia mesti rendah (kurang daripada 0.2%), kerana sebaliknya ia menyebabkan kesan negatif pada badan.
Fluorisasi air
Sangat serupa dengan bagaimana dengan pasta pergigian, garam fluorida telah ditambah kepada sumber air minuman untuk memerangi kemunculan karies pada mereka yang meminumnya. Kepekatan mesti masih jauh lebih rendah (0.7 ppm). Walau bagaimanapun, amalan ini biasanya tidak percaya dan kontroversi, mungkin kesan karsinogenik telah dikaitkan.
Ejen pengoksidaan
Gas f2 Ia berkelakuan seperti ejen pengoksidaan yang sangat kuat. Ini menjadikan banyak sebatian mengatur lebih daripada apabila terdedah kepada oksigen dan sumber haba. Itulah sebabnya ia telah digunakan dalam campuran bahan api roket, di mana mereka juga boleh menggantikan ozon.
Polimer
Dalam banyak kegunaan, sumbangan fluorida tidak disebabkan oleh f2 atau f-, tetapi terus ke atom elektronegatifnya yang membentuk sebahagian daripada sebatian organik. Oleh itu, dalam intipati pautan c-f.
Bergantung pada struktur, polimer atau serat dengan ikatan C-F biasanya hidrofobik, jadi mereka tidak basah atau menahan serangan asid fluorhoric; Atau lebih baik lagi, mereka boleh menjadi penebat elektrik yang sangat baik, dan bahan yang berguna dengan objek seperti paip dan sendi dihasilkan. Teflon dan Navion adalah contoh polimer fluorinasi ini.
Ahli farmasi
Kereaktifan fluorida dipanggil penggunaannya untuk sintesis pelbagai fluorin, sebatian organik atau bukan organik. Dalam organik, khususnya mereka yang mempunyai kesan farmakologi, menggantikan salah satu heteroátomos mereka dengan atom F meningkat (positif atau negatif) tindakannya terhadap objektif biologi mereka.
Itulah sebabnya dalam industri farmaseutikal pengubahsuaian beberapa ubat selalu di atas meja dengan menambahkan atom fluorin.
Sangat serupa berlaku dengan herbisida dan racun racun. Fluorin di dalamnya dapat meningkatkan tindakan dan keberkesanannya terhadap serangga dan perosak kulat.
Ukiran kaca
Asid fluorhoric, kerana agresifnya dengan kaca dan seramik, telah digunakan untuk merekodkan kepingan -bahan nipis dan halus dari bahan -bahan ini; Biasanya dimaksudkan untuk pembuatan mikrokomponen komputer, atau untuk mentol elektrik.
Pengayaan Uranium
Salah satu kegunaan fluorida asas yang paling relevan adalah untuk membantu memperkayakan uranium sebagai 235Atau. Untuk melakukan ini, mineral uranium dibubarkan dalam asid fluorhoric, menghasilkan uf4. Fluorida tak organik ini kemudian bertindak balas dengan f2, Untuk berubah menjadi UF6 (235Phew6 dan 238Phew6).
Seterusnya, dan melalui sentrifugasi gas, 235Phew6 Ia memisahkan dari 238Phew6 dan kemudian dioksidakan dan disimpan sebagai bahan api nuklear.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Krämer Katrina. (2019). Struktur Fluorin Beku Dihidupkan selepas 50 tahun. Persatuan Kimia Diraja. Pulih dari: dunia kimia.com
- Wikipedia. (2019). Fluorin. Diperoleh dari: dalam.Wikipedia.org
- Pusat Kebangsaan Maklumat Bioteknologi. (2019). Fluorin. Pangkalan data PUBCHEM. CID = 24524. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Dr. Doug Stewart. (2019). Fakta elemen fluorin. Chemicool. Pulih dari: chemicool.com
- Batul Nafisa Baxamusa. (21 Februari 2018). Penggunaan fluorin yang sangat menghairankan. Pulih dari: Sciencestruck.com
- Paola Opazo Sáez. (4 Februari 2019). Fluorida dalam ubat gigi: Adakah baik atau buruk untuk kesihatan? Pulih dari: nacionfarma.com
- Karl Christe & Stefan Schneider. (8 Mei 2019). Fluorin: elemen kimia. Encyclopædia Britannica. Pulih dari: Britannica.com
- Lentech b.V. (2019). Jadual Tempoh: Oksigen. Pulih dari: lentech.com
- Gagnon Steve. (s.F.). Fluorin elemen. Jefferson Lab. Pulih dari: pendidikan.Jlab.org
- Pasukan Kandungan Perubatan dan Editorial Persatuan Kanser Amerika. (28 Julai 2015). Fluoridasi air dan risiko kanser. Pulih dari: barah.org
- « Ciri -ciri sains yang tepat, apa yang anda pelajari, contohnya
- Tiada sejarah logam, sifat, kumpulan, kegunaan »

