Struktur, AIP) Aluminium (AIP) Struktur, Kegunaan, Risiko

- 4525
- 83
- Ismael Turner
Dia Aluminium fosfida Ia adalah sebatian bukan organik yang dibentuk oleh atom aluminium (Al) dan atom fosforus (p). Formula kimianya ALP. Ia adalah pepejal kelabu gelap atau, jika sangat murni, kuning. Ia adalah sebatian yang sangat toksik untuk makhluk hidup.
Fosfuro aluminium bertindak balas dengan kelembapan untuk membentuk fosfin atau ph fosfano pH3, yang merupakan gas beracun. Atas sebab ini, ALP tidak boleh menghubungi air. Bertindak balas dengan kuat dengan asid dan penyelesaian alkali.
 Aluminium fosfida. همان [GFDL (http: // www.gnu.Org/copyleft/fdl.html)]. Sumber: Wikimedia Commons.
Aluminium fosfida. همان [GFDL (http: // www.gnu.Org/copyleft/fdl.html)]. Sumber: Wikimedia Commons. Ia digunakan pada masa lalu untuk menghapuskan perosak seperti serangga dan tikus di tempat di mana bijirin bijirin dan produk pertanian lain disimpan. Walau bagaimanapun, disebabkan oleh bahaya yang tinggi ia telah dilarang di kebanyakan negara di dunia.
Pada masa ini, kegunaannya di kawasan elektronik secara teorinya disiasat melalui komputer yang mengira kemungkinan mendapatkan nanotube ALP semikonduktor, iaitu, tiub yang sangat kecil yang boleh menghantar elektrik hanya dalam keadaan tertentu.
Aluminium Phosphuro adalah sebatian yang sangat berbahaya, ia mesti dimanipulasi dengan alat keselamatan seperti sarung tangan, kanta, peralatan pernafasan dan pakaian pelindung.
[TOC]
Struktur
ALP aluminium phosphuro dibentuk oleh kesatuan atom aluminium pada fosforus p atom p. Hubungan antara keduanya adalah kovalen dan tiga, oleh itu ia sangat kuat.
Aluminium di ALP mempunyai keadaan pengoksidaan +3 dan fosforus mempunyai valensi -3.
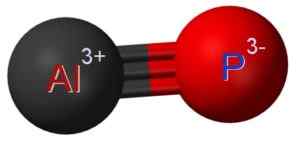 Struktur fosfuro aluminium di mana anda dapat melihat hubungan tiga antara aluminium (Al) dan atom fosforus (p) (P). Claudio Pistilli [CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons.
Struktur fosfuro aluminium di mana anda dapat melihat hubungan tiga antara aluminium (Al) dan atom fosforus (p) (P). Claudio Pistilli [CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons. Nomenclature
- Aluminium fosfida
Sifat
Keadaan fizikal
Pepejal kristal kelabu gelap atau kuning gelap. Kristal padu.
Berat molekul
57,9553 g/mol
Takat lebur
2550 ºC
Ketumpatan
2.40 g/cm3 pada 25 ° C
Kelarutan
Ia terurai di dalam air.
Sifat kimia
Bertindak balas dengan kelembapan untuk memberikan pH fosfin atau phosphano pH3 yang merupakan kompaun mudah terbakar dan beracun. Fosfin atau phosphaan.
Boleh melayani anda: Gadolinio: struktur, sifat, mendapatkan, menggunakanReaksi fosfuro aluminium dengan air adalah seperti berikut:
Fosfuro aluminium + air → aluminium hidroksida + fosfin
ALP + 3 jam2O → ke (oh)3 + Ph3↑
Persembahan komersial mempunyai aluminium karbonat ke2(Co3)3 Untuk mengelakkan diri sendiri -arah fosfin yang berlaku apabila ALP bersentuhan dengan kelembapan udara.
ALP stabil apabila kering. Bertindak balas dengan ganas dengan asid dan penyelesaian alkali.
ALP Aluminium Phosphuro tidak mencairkan, atau sublimal atau terurai secara termal pada suhu setinggi 1000 ° C. Walaupun pada suhu ini tekanan wapnya sangat rendah, iaitu, ia tidak menguap pada suhu itu.
Apabila dipanaskan pada penguraiannya memancarkan oksida fosforus toksik. Hubungan dengan logam, anda boleh memancarkan gas hidrogen mudah alih h2.
Sifat lain
Apabila ia murni ia menunjukkan warna kekuningan, apabila ia bercampur dengan sisa reaksi penyediaan yang memberikan warna dari kelabu ke hitam.
Volatiliti yang rendah tidak termasuk bahawa ia mempunyai bau, jadi bau bawang putih yang kadang -kadang memancarkan disebabkan oleh pH fosfin3 yang terbentuk dengan kehadiran kelembapan.
Memperoleh
Fosfuro aluminium boleh diperolehi dengan memanaskan campuran serbuk logam aluminium (Al) dan elemen fosforus merah (P).
Disebabkan pertalian fosforus (p) oleh oksigen (atau2) dan aluminium (al) oleh oksigen dan nitrogen (n2), Tindak balas mesti dilakukan dalam suasana bebas gas ini, seperti atmosfera hidrogen (h2) atau gas asli.
Reaksi bermula dengan cepat memanaskan kawasan campuran sehingga tindak balas bermula, yang eksotermik (haba berlaku semasa yang sama). Dari saat itu, reaksi berjalan dengan cepat.
Aluminium + fosforus → aluminium phosphuro
4 hingga + p4 → 4 Alp
Aplikasi
Dalam Penghapusan Perosak (Penggunaan Dihentikan)
Phosphuro aluminium digunakan pada masa lalu sebagai insektisida dan sebagai pembasmi tikus. Walau bagaimanapun, walaupun telah dilarang oleh ketoksikannya, ia masih digunakan di beberapa bahagian dunia.
Boleh melayani anda: .Asid Stearic (CH3 (CH2) 16COOH): Struktur, sifat, kegunaanIa digunakan untuk pengasapan di ruang tertutup di mana produk makanan yang diproses atau tidak diproses ditemui (seperti bijirin), makanan untuk produk haiwan dan bukan makanan.
Objektifnya adalah untuk mengawal serangga dan tikus yang menyerang artikel yang disimpan, sama ada boleh dimakan atau tidak.
Ia membolehkan mengawal tikus dan serangga di kawasan bukan domestik, pertanian atau bukan pertanian, memusnahkan di luar rumah atau di burrows dan sarang mereka untuk mengelakkan penyakit tertentu dari menghantar.
 Tikus dan tikus adalah perosak yang menyerang tempat penyimpanan bijirin. Beberapa tahun yang lalu mereka bertempur dengan aluminium Phosphuro. Pengarang: Andreas N. Sumber: Pixabay.
Tikus dan tikus adalah perosak yang menyerang tempat penyimpanan bijirin. Beberapa tahun yang lalu mereka bertempur dengan aluminium Phosphuro. Pengarang: Andreas N. Sumber: Pixabay.  Tikus dikawal dengan meletakkan fosfuro aluminium di lubang mereka. Pengarang: Photo-Rabe. Sumber: Pixabay.
Tikus dikawal dengan meletakkan fosfuro aluminium di lubang mereka. Pengarang: Photo-Rabe. Sumber: Pixabay. Bentuk penggunaannya terdiri daripada pendedahan ALP di udara atau kelembapan, kerana pH fosfin atau phosphaan dikeluarkan3 yang menghasilkan kerosakan kepada banyak organ wabak untuk menghapuskan.
 Serangga juga dihapuskan dengan ALP Aluminium Phosphuro. Pengarang: Michael Power. Sumber: Unspash.
Serangga juga dihapuskan dengan ALP Aluminium Phosphuro. Pengarang: Michael Power. Sumber: Unspash. Dalam aplikasi lain
ALP Aluminium Phosphuro digunakan sebagai sumber phosphine atau phosfano pH3 dan sedang digunakan dalam penyelidikan semikonduktor.
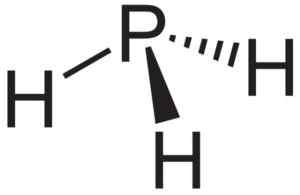 Phosphaano atau pH fosfin3, Kompaun yang terbentuk ketika ALP Aluminium Phosphuro bersentuhan dengan air. Neuroteker [domain awam]. Sumber: Wikimedia Commons.
Phosphaano atau pH fosfin3, Kompaun yang terbentuk ketika ALP Aluminium Phosphuro bersentuhan dengan air. Neuroteker [domain awam]. Sumber: Wikimedia Commons. Penyelidikan Teoritis Nanotube ALP
Kajian teori telah dijalankan dalam pembentukan nanotube fosfuro aluminium ALP. Nanotube adalah silinder yang sangat kecil dan sangat nipis yang boleh dilihat hanya dengan mikroskop elektronik.
Nanotube ALP dengan boron
Kajian teori yang dijalankan melalui pengiraan pengiraan menunjukkan bahawa kekotoran yang boleh ditambah kepada nanotube ALP dapat mengubah sifat -sifat teoritis ini.
Sebagai contoh, dianggarkan bahawa menambah atom boron (b) kepada nanotube ALP boleh menjadikannya semikonduktor jenis-p. Semikonduktor adalah bahan yang bertindak sebagai konduktor elektrik atau sebagai penebat bergantung pada medan elektrik yang mana ia tertakluk.
Boleh melayani anda: keadaan plasma: ciri, jenis dan contohDan semikonduktor jenis-p Ia adalah apabila bahan itu ditambah kekotoran, dalam hal ini ALP adalah bahan permulaan dan atom boron akan menjadi kekotoran. Semikonduktor berguna untuk aplikasi elektronik.
Nanotube ALP dengan struktur yang diubah
Sesetengah saintis telah menjalankan pengiraan untuk menentukan kesan mengubah struktur rangkaian kristal nanotube ALP dari heksagon ke octahedral.
Mereka mendapati bahawa manipulasi struktur rangkaian kristal boleh digunakan untuk menyesuaikan kekonduksian dan kereaktifan nanotube ALP dan mereka bentuknya supaya mereka berguna untuk aplikasi elektronik dan optik.
Risiko
Hubungi dengan fosfuro aluminium boleh merengsakan kulit, mata dan membran mukus. Sekiranya ia ditelan atau dihirupnya, ia adalah toksik. Ia dapat diserap melalui kulit dengan kesan toksik.
Jika ALP bersentuhan dengan reaksi air dan bentuk fosfin atau pH phosphane3 yang sangat mudah terbakar kerana ia terbakar bersentuhan dengan udara. Oleh itu ia dapat mengeksploitasi. Di samping itu fosfin menyebabkan kematian manusia dan haiwan.
Oleh kerana racun perosak ekonomi adalah fosfuro aluminium, penggunaannya adalah penyebab biasa keracunan rakyat dan memerlukan kadar kematian yang tinggi.
 Fosfuro aluminium sangat berbahaya. Pengarang: OpenClipart-Vectors. Sumber: Pixabay.
Fosfuro aluminium sangat berbahaya. Pengarang: OpenClipart-Vectors. Sumber: Pixabay. Bertindak balas dengan kelembapan membran mukus dan dengan asid hidroklorik HCl dari perut yang membentuk gas pH phosphane yang sangat toksik3. Oleh itu, dengan penyedutan dan pengambilan, fosfin terbentuk di dalam badan, dengan kesan maut.
Pengambilannya menyebabkan pendarahan saluran gastrousus, keruntuhan kardiovaskular, gangguan neuropsychiatrik, kegagalan pernafasan dan buah pinggang dalam beberapa jam.
ALP sangat beracun untuk semua haiwan terestrial dan akuatik.
Rujukan
- Atau.S. Perpustakaan Perubatan Negara. (2019). Aluminium fosfida. Pulih dari pubchem.NCBI.NLM.NIH.Gov.
- Sjögren, b. et al. (2007). Aluminium. Sebatian aluminium lain. Dalam Buku Panduan mengenai Toksikologi Logam (Edisi Ketiga). Pulih dari Scientedirect.com.
- Gupta, r.C. dan Crissman, J.W. (2013). Penilaian keselamatan termasuk isu semasa dan muncul dalam patologi toksikologi. Risiko manusia. Dalam Buku Panduan Toksikologi Haschek dan Rousseaux (edisi ketiga). Pulih dari Scientedirect.com.
- Putih, w.Dan. dan bushey, ke.H. (1944). Aluminium Phhosphide - Penyediaan dan Komposisi. Jurnal American Chemical Society 1944, 66, 10, 1666-1672. Pulih dari pub.ACS.org.
- Mirzaei, Maryam dan Mirzaei, Mahmoud. (2011). Kajian teoretikal boron-due aluminium fosfida nanotube. Kimia Komputasi dan Teoritis 963 (2011) 294-297. Pulih dari Scientedirect.com.
- Takahashi, l. Dan Takahashi, k. (2018). Menala struktur elektronik nanotube fosfida aluminium ini. ACS Appl. Nano Mater. 2018, 1, 501-504. Pulih dari pub.ACS.org.
- Gupta, ms.K. (2016). Kesan toksik pesisida (agrokimia). Aluminium fosfida. Dalam dana toksikologi. Pulih dari Scientedirect.com.
- « Koordinat Rectangular Contoh dan Latihan Diselesaikan
- Ijazah polinomial bagaimana ia ditentukan, contoh dan latihan »

