Orang India

- 1104
- 137
- Ms. Micheal Rippin
 Sekeping India Metalik. Sumber: Hi-Res Imej Elemen Kimia [CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)]
Sekeping India Metalik. Sumber: Hi-Res Imej Elemen Kimia [CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)] Apa itu India?
Dia Orang India Ia adalah logam yang dimiliki oleh kumpulan 13 jadual berkala dan mempunyai simbol kimia di. Nombor atom anda ialah 49, 49Dalam, dan dibentangkan sebagai dua isotop: 113Dalam dan 115Dalam, yang terakhir menjadi yang paling banyak. Di bumi atom India didapati sebagai kekotoran dalam zink dan mineral utama.
Ia adalah logam tertentu, kerana ia adalah yang paling lembut yang dapat disentuh tanpa banyak risiko kesihatan; Tidak seperti litium dan rubidium, yang akan membakar kulit dengan sangat teruk apabila bertindak balas dengan kelembapannya. Sekeping India boleh dipotong dengan pisau dan patah dengan daya jari, memancarkan masalah tersendiri.
Sesiapa yang mendengar logam ini pasti akan teringat India, tetapi namanya berasal dari warna indigo, yang diperhatikan ketika ujian api dilakukan. Dalam pengertian ini, ia kelihatan agak banyak kalium, membakar logamnya atau sebatiannya dengan api yang sangat ciri, di mana India dikesan buat kali pertama di mineral sphenset.
Orang India berkongsi banyak kualiti kimia dengan aluminium dan gallium, yang membentangkan kebanyakan sebatian dengan bilangan pengoksidaan +3 (dalam3+). Ia menggabungkan dengan baik dengan Gaul membentuk aloi dengan titik lebur yang rendah, salah satunya adalah Galinstan.
Aplikasi India berdasarkan lapisan bahan dengan aloi mereka, menjadikannya konduktor elektrik dan fleksibel. Orang India mempunyai beberapa gelas untuk memberi mereka lebih besar, menggantikan perak. Di dunia teknologi, India ditemui di skrin sentuhan dan LCD.
Penemuan
Pada tahun 1863, ahli kimia Jerman Ferdinand Reich sedang mencari jejak elemen Talio, menggunakan garis hijau spektrum pelepasannya, di Cinc Mineral; Sampel sphalerite (ZnS) secara khusus di sekitar Saxony. Setelah memanggang mineral, keluarkan kandungan belerang mereka, mencerna mereka dalam asid hidroklorik, dan suling zink klorida, memperoleh pendakian pajizo.
Memandangkan penemuan itu, Reich memutuskan untuk melakukan analisis spektroskopi; Tetapi kerana dia tidak mempunyai mata yang baik untuk memerhatikan warna, dia pergi ke rakannya Hariomus Theodor Richter untuk membantunya dalam tugas ini. Richter adalah orang yang memerhatikan garis spektrum kebiruan, yang tidak sepadan dengan spektrum unsur lain.
Ia boleh melayani anda: asid iodose (HiO2): sifat dan kegunaanKedua -dua ahli kimia Jerman menghadapi elemen baru, yang dipanggil warna India untuk warna indigo api ketika sebatian mereka dibakar; Dan pada gilirannya, nama warna ini berasal dari perkataan Latin Indicum, Apa maksud India.
Setahun kemudian, pada tahun 1864, teruja dan selepas siri hujan dan pembersihan yang berpanjangan, mereka mengasingkan sampel metalik India melalui elektrolisis garam terlarut mereka di dalam air.
Struktur India
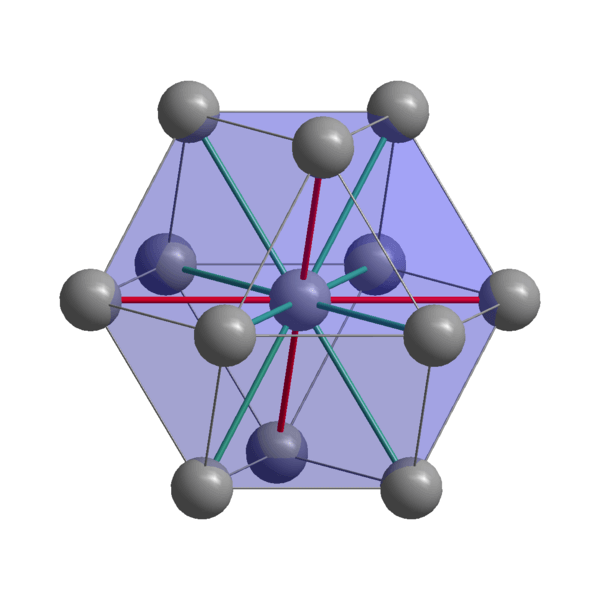 Struktur Kristal India
Struktur Kristal India India, dalam, atom perpaduan menggunakan elektron valensi mereka untuk menubuhkan ikatan logam. Oleh itu, mereka akhirnya diperintahkan dalam struktur tetragonal yang diputarbelitkan yang berpusat pada badan. Interaksi antara atom in-in-in-in-neighbor agak lemah, yang menjelaskan mengapa India mempunyai titik lebur yang rendah (156 ºC).
Sebaliknya, kekuatan yang menyatukan dua atau lebih kristal India tidak kuat sama ada, jika tidak, mereka tidak akan bergerak di atas satu sama lain, memberikan kelembutan ciri logam.
Hartanah India
Penampilan fizikal
Ia adalah logam perak yang sangat lembut. Ia dapat merobek dengan tekanan kuku, potong dengan pisau, atau gores dalam strok cerah di atas kertas. Ia juga mungkin untuk mengunyahnya dan mengubahnya dengan gigi, dengan syarat ia diratakan. Ia juga sangat mulur dan mudah dibentuk, mempunyai sifat plastik.
Apabila orang India dipanaskan dengan obor menolak api warna indigo, bahkan lebih cerah dan lebih berwarna daripada kalium.
Jisim molar
114.81 g/mol
Takat lebur
156.60 ºC
Takat didih
2072 ºC.
Seperti Gaul, India mempunyai selang suhu yang besar di antara titik gabungannya dan mendidih. Ini mencerminkan fakta bahawa interaksi dalam dalam cecair adalah lebih kuat daripada yang mendominasi dalam kaca; Dan oleh itu, lebih mudah untuk mendapatkan setitik India daripada wap mereka.
 Lokasi India dalam jadual berkala. Sumber: Daniel Mayer atau GreatPatton Vectorization: Sushant Savla, CC By-SA 3.0, melalui Wikimedia Commons
Lokasi India dalam jadual berkala. Sumber: Daniel Mayer atau GreatPatton Vectorization: Sushant Savla, CC By-SA 3.0, melalui Wikimedia Commons Ketumpatan
Pada suhu bilik: 7.31 g/cm3
Betul -betul di titik lebur: 7.02 g/cm3
Elektronegativiti
1.78 pada skala Pauling
Tenaga pengionan
Pertama: 558.3 kJ/mol
Kedua: 1820.7 kJ/mol
Ketiga: 2704 kJ/mol
Kekonduksian terma
81.8 w/(m · k)
Resistiviti elektrik
83.7 nΩ · m
Kekerasan mohs
1.2. Hampir tidak lebih sukar daripada talc (tidak membingungkan ketabahan keras).
Reaktiviti
Orang India larut dalam asid untuk menyebabkan garam, tetapi tidak larut dalam larutan alkali, walaupun dengan kalium hidroksida panas. Bertindak balas secara langsung dengan sulfur, oksigen dan halogen.
Boleh melayani anda: pencairan: konsep, bagaimana ia dilakukan, contoh, latihanOrang India agak amphoterik, tetapi berkelakuan lebih sebagai asas daripada asid, sebagai penyelesaian berair yang sedikit asas. In (oh)3 Ia redisolve dengan penambahan lebih banyak alkali menyebabkan kompleks indiat, dalam (OH)4-, seperti aluminates.
Konfigurasi Elektronik
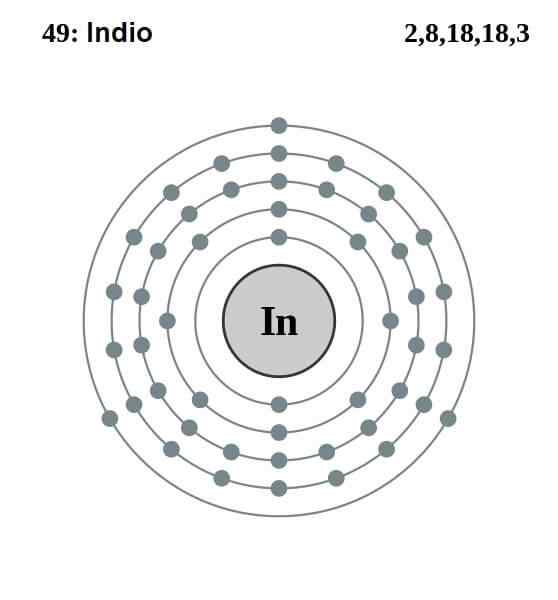 Konfigurasi India Elektronik
Konfigurasi India Elektronik Konfigurasi elektronik India adalah seperti berikut:
[KR] 4D10 5s2 5 p1
Daripada tiga belas elektron, tiga orbital 5s dan 5p terakhir adalah Valencia. Dengan ketiga -tiga elektron atom India ini menetapkan ikatan logam mereka, seperti aluminium dan gallium, dan membentuk ikatan kovalen dengan atom lain.
Nombor pengoksidaan
Di atas digunakan untuk berdiri seketika bahawa orang India dapat kehilangan tiga elektron Valencia, atau memenangi lima untuk menjadi isolektronik kepada xenon gas mulia.
Sekiranya dalam sebatian kita mengandaikan bahawa ia telah kehilangan tiga elektronnya, ia akan kekal sebagai kation trivalen di3+ (Dalam analogi al3+ dan ga3+) dan, oleh itu, nombor pengoksidaan anda akan +3. Sebilangan besar sebatian India berada di (iii).
Antara bilangan pengoksidaan lain yang dijumpai untuk India yang kita ada: -5 (dalam5-), -2 (dalam2-), -1 (dalam-), +1 (dalam+) dan +2 (dalam2+).
Beberapa contoh sebatian dalam (i) adalah: INF, INCBR, INI dan IN2Sama ada. Kesemua mereka adalah sebatian yang jarang berlaku, manakala yang ada di (iii) adalah yang utama: dalam (oh)3, Dalam2Sama ada3, Termasuk3, Inf3, dan lain-lain.
Dalam (i) sebatian adalah ejen pengurangan yang kuat, di mana masuk+ Sumbangkan dua elektron ke spesies lain untuk masuk3+.
Isotop
Orang India dibentangkan sebagai dua isotop: 113Dalam dan 115Dalam, masing -masing sebanyak 4.28% dan 95.72%. Oleh itu, di bumi kita mempunyai lebih banyak atom 115Dalam 113Dalam. Dia 115Dalam mempunyai separuh hayat 4.41 · 1014 bertahun -tahun, begitu hebat bahawa ia praktikal dianggap stabil, walaupun menjadi radioisotop.
Pada masa ini, sejumlah 37 isotop buatan India, semua radioaktif dan sangat tidak stabil telah dibuat. Dari mereka semua, yang paling stabil adalah 111Dalam, yang mempunyai separuh hayat 2.8 hari.
Penggunaan/aplikasi
Aloi
Orang India bergaul dengan Gallium. Kedua -dua logam membentuk aloi yang mel. Juga, orang India juga mudah digabungkan, mempunyai kelarutan 57% dalam merkuri.
Boleh melayani anda: asid asetik (CH3COOH)Aloi India digunakan untuk merancang cermin perak tanpa menggunakan perak. Apabila mereka dituangkan di kawasan apa -apa bahan, ia bertindak sebagai penganut, supaya kaca, logam, kuarza dan seramik dapat dikumpulkan.
elektronik
 Tanpa India, skrin sentuh tidak akan pernah wujud
Tanpa India, skrin sentuh tidak akan pernah wujud Orang India juga bergaul dengan Germanio, jadi sebatiannya ditambah sebagai doping ke Nitruro Jerman dari LED, menghasilkan semula lampu biru ini, ungu dan hijau. Ia juga merupakan sebahagian daripada transistor, termistor dan sel fotovoltaik.
Yang paling penting dalam sebatiannya ialah timah dan oksida India, yang digunakan sebagai lapisan kaca untuk mencerminkan beberapa panjang gelombang. Ini membolehkan anda digunakan dalam gelas kimpalan, dan di kaca gores supaya mereka tidak memanaskan.
Kaca yang disalut dengan oksida ini adalah konduktor elektrik yang baik; Seperti yang dari jari kita. Dan itulah sebabnya ia ditakdirkan untuk pembuatan skrin sentuhan, lebih banyak aktiviti semasa kerana kemunculan lebih banyak telefon pintar.
Risiko
 India dalam keadaan pepejal. Sumber: w. OELEN, CC BY-SA 3.0, melalui Wikimedia Commons
India dalam keadaan pepejal. Sumber: w. OELEN, CC BY-SA 3.0, melalui Wikimedia Commons India tidak mewakili sebarang risiko kepada alam sekitar pada mulanya, seperti dalam ionnya3+ Mereka tidak disebarkan dalam kuantiti yang cukup. Tidak ada maklumat mengenai apa kesannya terhadap tanah, yang mempengaruhi tumbuhan, dan tidak di fauna atau laut.
Di dalam badan tidak diketahui jika ion masuk3+ Mereka mempunyai penyertaan penting dalam metabolisme dalam jumlah jejak. Walau bagaimanapun, apabila sebatian mereka ditelan, mereka berbahaya kepada beberapa organ, itulah sebabnya mereka dianggap sebagai bahan yang sangat toksik.
Malah, zarah ito (timah dan oksida India, kerana akronimnya dalam bahasa Inggeris: Indium Tin Oxide), sangat diperlukan untuk pembuatan skrin untuk komputer dan telefon pintar, mereka boleh memberi kesan negatif terhadap kesihatan pekerja, menyebabkan mereka penyakit yang dipanggil paru -paru India.
Pengambilan zarah -zarah ini berlaku di atas semua dengan penyedutan dan dengan bersentuhan melalui kulit dan mata.
Sebaliknya, zarah -zarah India logam halus terdedah untuk membakar dan menyebabkan kebakaran jika mereka pagar sumber haba.

