Potassium Permanganate (KMNO4)

- 1868
- 143
- Kerry Schmitt
 Potassium permanganat kristal
Potassium permanganat kristal Apa itu kalium permanganat?
Dia Potassium permanganat (Kmno4) Ia adalah sebatian bukan organik yang dibentuk oleh logam mangan -transisi kumpulan 7 (viib) -, oksigen dan kalium. Ia adalah pepejal vitreous ungu gelap. Penyelesaian berairnya juga berwarna ungu gelap; Penyelesaian ini menjadi kurang ungu kerana ia dicairkan dalam sejumlah besar air.
Secara komersial dicapai dalam persembahan tablet, kristal dan habuk. Ia dikenali dengan nama Condy atau Camaleón Mineral. Istilah "bunglon" merujuk kepada keupayaan mineral: jika ia mengubah warna bersentuhan dengan soda kaustik dan bahan organik, gula berlaku.
Kmno4 Ia mula mengalami pengurangan (keuntungan elektron) dalam penggantian warna mengikut urutan berikut: ungu> biru> hijau> kuning> tidak berwarna (dengan mno coklat coklat2). Reaksi ini menunjukkan harta penting permanganat kalium: ia adalah ejen pengoksidaan yang sangat kuat.
Formula
Formula kimianya adalah kmno4; iaitu, untuk setiap kation k+ Ada anion mno4- Berinteraksi dengan ini
Struktur kimia kalium permanganat
 Struktur kristal kmno4
Struktur kristal kmno4 Di bahagian atas, struktur kristal kmno diwakili4, yang jenis ortorrombik. Sfera ungu sesuai dengan kasi k+, manakala tetrahedron yang dibentuk oleh empat sfera merah dan sfera kebiruan sepadan dengan anion mno4-.
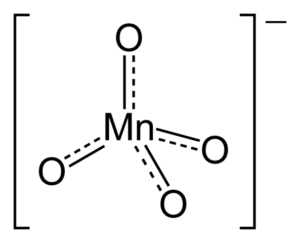
Mengapa Anion mempunyai geometri tetrahedral? Struktur Lewisnya menjawab soalan ini. Garis putus -putus bermaksud bahawa pautan berganda bergema antara Mn dan O. Untuk mengamalkan struktur ini, pusat logam mesti mempunyai hibridisasi sp3.

Oleh kerana mangan tidak mempunyai pasangan elektron yang luar biasa, ikatan Mn-O tidak ditolak ke arah pesawat yang sama. Begitu juga, beban negatif diedarkan di antara empat atom oksigen, yang bertanggungjawab untuk orientasi kasi+ Dalam pengaturan kristal.
Dapat melayani anda: tetap pengionanKmno menggunakan4
Perubatan dan Veterinar
Oleh kerana tindakan bakterisinya, ia digunakan dalam pelbagai penyakit dan keadaan yang menyebabkan lesi kulit, seperti: jangkitan kaki dengan kulat, impetigo, luka cetek, dermatitis dan ulser tropika.
Oleh kerana tindakannya yang berbahaya, kalium permanganat mesti digunakan pada kepekatan rendah (1: 10000), yang mengehadkan keberkesanan tindakannya.
Ia juga digunakan dalam rawatan parasitosis ikan dalam akuarium yang menghasilkan jangkitan keberanian kulit dan ulser.
Rawatan air
Ia adalah regenerasi kimia yang digunakan untuk mengeluarkan besi, magnesium dan hidrogen sulfida dari air (bau yang tidak menyenangkan), dapat digunakan untuk membersihkan air kumbahan.
Besi dan magnesium mendakan dalam bentuk oksida air yang tidak larut. Di samping itu, ia membantu menghilangkan karat yang ada di paip.
Pemeliharaan buah
Kalium permanganat menghilangkan etilena yang dihasilkan dalam pisang semasa penyimpanan, membolehkannya kekal selama lebih dari 4 minggu tanpa matang, termasuk pada suhu bilik bilik.
Di Afrika mereka menggunakannya untuk merendam sayur -sayuran, dengan tujuan meneutralkan dan menghapuskan ejen bakteria sekarang.
Tindakan Kebakaran
Potassium Permanganate digunakan untuk mengehadkan lanjutan kebakaran. Berdasarkan keupayaan permanganat untuk memulakan api, ia digunakan untuk membuat aliran balas di kebakaran hutan.
Tajuk redoks
Dalam kimia analisis penyelesaian berair yang diseragamkan digunakan sebagai tajuk oksidan dalam penentuan redoks.
Reagen Organik
Ia berfungsi untuk menukar alkenes menjadi dioles; iaitu, dua kumpulan OH ditambah kepada ikatan berganda c = c. Persamaan kimia berikut:

Juga, dalam larutan asid sulfurik dengan asid kromik (h2Cro4) Ia digunakan untuk pengoksidaan alkohol utama (R-OH) kepada asid karboksilik (R-COOH atau RCO2H).
Boleh melayani anda: ikatan kovalen bukan -polarKuasa pengoksidaannya cukup kuat untuk mengoksidakan kumpulan alkil primer atau sekunder dari sebatian aromatik "carboxyling mereka"; iaitu, mengubah rantaian sampingan r (contohnya, cho3) Dalam kumpulan COOH.
Penggunaan Sejarah
Ia adalah sebahagian daripada serbuk yang digunakan sebagai kilat dalam fotografi atau untuk memulakan reaksi rayap.
Ia digunakan dalam Perang Dunia II untuk penyamaran kuda putih pada siang hari. Untuk ini mereka menggunakan mangan dioksida (MNO2), yang berwarna coklat; Dengan cara ini mereka tidak disedari.
Sintesis KMNO4
Mineral Pyrolusite mengandungi mangan dioksida (MNO2) dan kalium karbonat (Caco3).
Pada tahun 1659 ahli kimia johann r. Glauber mencairkan mineral dan membubarkannya ke dalam air, memerhatikan penampilan warna hijau dalam larutan, yang kemudiannya berubah dalam warna ungu dan akhirnya menjadi merah. Warna terakhir ini sesuai dengan penjanaan kalium permanganat.
Pada pertengahan abad ke -15, Henry Condy mencari produk antiseptik dan pada mulanya merawat pyrolusit dengan NaOH dan kemudian dengan KOH, menghasilkan kristal Condy yang dipanggil; iaitu kalium permanganat.
Kalium permanganat dihasilkan secara industri dari mangan dioksida yang hadir di mineral pyrolusite. Mno2 Hadir di mineral bertindak balas dengan kalium hidroksida dan kemudiannya dipanaskan dengan kehadiran oksigen.
2 mno2 + 4 koh +atau2 => 2 k2Mne4 + 2 jam2Sama ada
Potassium Manganate (k2Mne4) ditukar menjadi kalium permanganat oleh pengoksidaan elektrolitik ke dalam medium alkali.
2 k2Mne4 + 2 jam2O => 2 kmno4 + 2 koh +h2
Dalam reaksi lain untuk menghasilkan kalium permanganat, kalium mangane bertindak balas dengan co2, Mempercepat Proses Ketidakhadiran:
3 k2Mne4 + 2 co2 => 2 kmno4 + Mne2 + K2Co3
Boleh melayani anda: teori orbital molekulKerana penjanaan MNO2 (mangan dioksida) Prosesnya tidak menguntungkan, KOH mesti dihasilkan dari k2Co3.
Sifat Kmno4
Ia adalah pepejal kristal ungu yang cair pada 240 ºC, yang mempunyai ketumpatan 2.7 g/ml, dan berat molekul kira -kira 158 g/mol.
Ia tidak terlalu larut dalam air (6.4 g/100 ml pada 20 ºC), yang menunjukkan bahawa molekul air tidak sebahagian besarnya menyelesaikan ion MNO4-, Kerana mungkin geometri tetrahedral mereka memerlukan banyak air untuk pembubaran mereka. Begitu juga, ia juga boleh membubarkan alkohol metil, aseton, asid asetik dan piridin.
Penguraian
Ia terurai pada 240 ºC, melepaskan oksigen:
2kmno4 => K2Mne4 + Mne2 + Sama ada2
Anda boleh mengalami penguraian dengan tindakan alkohol dan pelarut organik lain, serta tindakan asid kuat dan pengurangan ejen.
Kuasa pengoksidaan
Dalam garam ini, mangan mempamerkan keadaan pengoksidaannya yang paling besar (+7), atau apa yang sama, dengan jumlah maksimum elektron yang boleh hilang dengan cara ionik. Sebaliknya, konfigurasi mangan elektronik adalah 3d54s2; Oleh itu, dalam kalium permanganat seluruh lapisan Valencia atom mangan adalah "kosong".
Kemudian, atom mangan membentangkan kecenderungan semula jadi untuk mendapatkan elektron; iaitu, dikurangkan kepada keadaan pengoksidaan lain dalam media alkali atau berasid. Inilah penjelasan mengapa kmno4 Ia adalah ejen pengoksidaan yang kuat.
Rujukan
- F.Albert Cotton dan Geoffrey Wilkinson, FRS. (1980). Kimia bukan organik maju. Editorial Limusa, Mexico, edisi ke-2, halaman 437-452.
- Robin Wasserman. Penggunaan Perubatan untuk Permanganat Potassium. Livestrong pulih.com
- Clark d. 3 Ultimate menggunakan kalium permanganat. Pulih dari teknologi.org
- J.M. Cedardea, c. Arnáiz dan E. Díaz. Kalium permanganat: oksidan yang kuat dan serba boleh. Dept. Kejuruteraan Kimia dan Alam Sekitar. Sekolah Universiti Seville.

